
| A.等于0.90 mol | B.等于0.45 mol |
| C.小于0.45 mol | D.大于0.45 mol、小于0.90 mol |
科目:高中化学 来源:不详 题型:单选题
 Fe2O3+SO2↑+ SO3↑+ 14H2O
Fe2O3+SO2↑+ SO3↑+ 14H2O| A.有BaSO4生成 | B.有BaSO3生成 |
| C.同时有BaSO4和BaSO3生成 | D.有SO3逸出 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 o
o

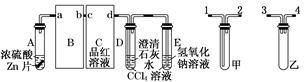
 酸性KMnO4溶液、饱和NaHCO3溶液、品红溶液、澄清石灰水
酸性KMnO4溶液、饱和NaHCO3溶液、品红溶液、澄清石灰水
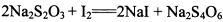 。为测定所制得晶体的纯度,该小组以淀粉作指示剂,用
。为测定所制得晶体的纯度,该小组以淀粉作指示剂,用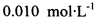 的碘水进行多次取样滴定,测得
的碘水进行多次取样滴定,测得 的含量约为102%。若所用试剂及操作均无不当,产生该结果最可能的原因是______________。
的含量约为102%。若所用试剂及操作均无不当,产生该结果最可能的原因是______________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 H2
H2 Cu,
Cu, CuSO4
CuSO4 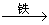 Cu。
Cu。| A.相等 | B.①多 | C.②多 | D.无法判断 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.都是无色气体 | B.都是非电解质 |
| C.通入Ba(OH)2溶液中都能产生白色沉淀 | D.都是形成酸雨的主要原因 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com