
ij�о���ѧϰС��ѧϰ�˹�ҵ�������Ƽ����ԭ����
��������⡿�ܷ���ʵ����ģ�⡰�����Ƽ������ȡNaHCO3�Ĺ����أ�
��ʵ��ԭ����д�������Ƽ��Ӧ�Ļ�ѧ����ʽΪ
��ʵ����֤����ͼ�Ǹ�ѧϰС�����ģ��ʵ��ʱ���õ��IJ�����Ҫװ�á�
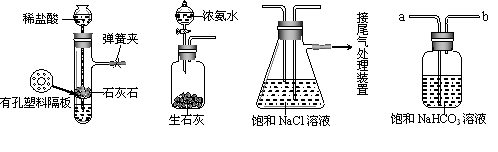
��ش��������⣺
�� ����Aװ�������Եķ����ǣ�����������©�����������н����ɼк�©��ע��һ������ˮ��ʹ©���ڵ�ˮ������Թ��ڵ�ˮ�棬ֹͣ��ˮ���� ��˵��װ�ò�©����
�� D��������װ��A��װ��C֮������徻��װ�ã��������� ����a��b����D�������dz�ȥ ���塣�ɷ�ƿ���Լ���Ϊ̼������Һ_____����ɡ�������
(3) ʵ��ʱ����NaCl��Һ��ͨ��϶�� ����ͨ�������� ����ԭ����_____��(��д���)
�� ʹCO2���ױ����� �� NH3��CO2������ȡ �� CO2���ܶȱ�NH3��
(4) �� �ķ��������ɵ�NaHCO3����ӻ�����з��������
���Ҫ�Ƶô�����跢���ķ�Ӧ�ǣ�д����Ӧ�Ļ�ѧ����ʽ��:
��
���ó����ۡ����á������Ƽ����ʵ���ҿ�����ȡNaHCO3 ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
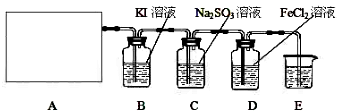
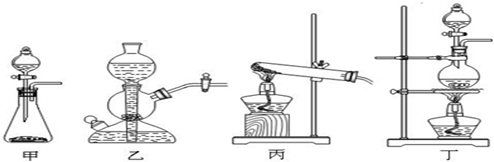
 ��2011?������һģ�����Ṥ����Χ�Ŀ������н϶�Ķ�������ij�о���ѧϰС��Ϊ�˲ⶨ�������ں�N2��O2��CO2��SO2�ȣ��ж������������������������ʵ�鷽������ͼ�������ڲⶨ��ʹ�õIJ���װ��ͼ��
��2011?������һģ�����Ṥ����Χ�Ŀ������н϶�Ķ�������ij�о���ѧϰС��Ϊ�˲ⶨ�������ں�N2��O2��CO2��SO2�ȣ��ж������������������������ʵ�鷽������ͼ�������ڲⶨ��ʹ�õIJ���װ��ͼ��| 22.4m |
| 233V |
| 22.4m |
| 233V |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
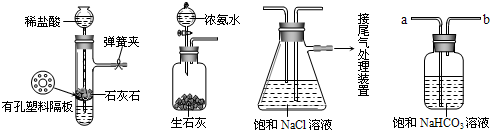
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| 8000��(15-cV2) |
| V1 |
| 8000��(15-cV2) |
| V1 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com