
【题目】有下列各组微粒或物质:
A.O2和O3
B.![]() 和
和![]()
C.CH3CH2CH2CH3和CH3CH2CH(CH3)CH3
D.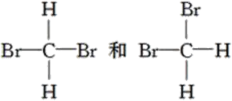
E.CH3CH2CH2CH3和![]()
(1)________组两种微粒互为同位素。
(2)________组两种物质互为同素异形体。
(3)________组两种物质属于同系物。
(4)________组两物质互为同分异构体。
(5)________组两物质是同一物质。
【答案】B A C E D
【解析】
质子数相同而中子数不同的两种核素互称为同位素;由同种元素组成的不同种分子互称为同素异形体;结构相似,分子组成上相差1个或多个CH2基团的有机物互称为同系物;分子式相同而结构不同的两种化合物互称同分异构体。
(1)根据分析中的定义,B中C元素的质子数相同而中子数不同,故二者互称同位素;
(2)根据分析中的定义,A中两种分子均由O元素构成,故二者互称同素异形体;
(3)根据分析中的定义,C中分子之间相差1个CH2基团,且结构相似,故二者互称为同系物;
(4)根据分析中的定义,E中两种有机物分子式相同且结构不同,故二者互称为同分异构体;
(5)D中两种结构为同一种物质,因为该有机物为四面体结构。


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】固定容积为2 L的密闭容器中发生反应xA(g)+yB(g) ![]() zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系。结合图像判断,下列结论正确的是
zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系。结合图像判断,下列结论正确的是
![]()
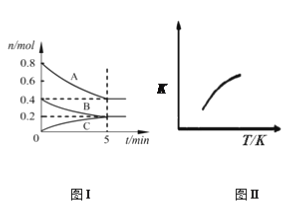
A. 200℃时,反应从开始到平衡的平均反应速率v(A)=0.08mol·L-1·min-1
B. 若0~5 min时容器与外界的热交换总量为m kJ,则该反应的热化学方程式可表示为:2A + B ![]() C ΔH = +5m kJ/mol
C ΔH = +5m kJ/mol
C. 200℃时,若在第6 min再向体系中加入1molAr,A的转化率不变
D. 200℃时,平衡后再充入2 mol B和2 mol C时,v正>v逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一定量的CuCl2产品投入Na2CO3溶液中,充分反应生得到一种仅含四种元素的不溶性盐X,并产生气体CO2。设计如下实验探究X的组成和性质。已知各步反应所需试剂均过量,请回答:

(1)混合气体的成分是______________;X的化学式为__________________。
(2)写出CuCl2与Na2CO3反应生成X的离子方程式______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.氨气具有还原性,在铜的催化作用下,氨气和氟气反应生成A 和B。A 为铵盐,B 在标准状况下为气态。在此反应中,若每有1体积氨气参加反应,同时有0.75 体积氟气参加反应;若每有8.96L 氨气(标准状况)参加反应,同时生成0.3 mol A。
(1) 写出氨气和氟气反应的化学方程式_____________________________________________________。
Ⅱ.某固体可能由Al、(NH4)2SO4、MgCl2、AlCl3、FeCl2中的一种或几种组成,现取该固体进行如下实验,所得现象和有关数据如下所示(气体体积的数据均已折算成标准状况下):
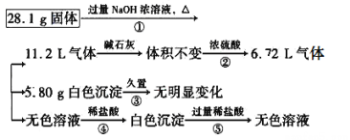
请回答下列问题:
(2)混合物中存在的物质有____________________(填化学式)。
Ⅲ.(3)测定硫酸铜晶体(CuSO4·xH2O)中结晶水的x值:称取2.41 g 硫酸铜晶体,在坩埚中加热至质量不再改变时,称量粉末的质量为1.6 g。则计算得x=____(计算结果精确到0.1)。
Ⅳ.称取3.60 g草酸亚铁晶体(FeC2O4·2H2O),用热重法对其进行热分解,得到剩余固体的质量随温度变化的曲线如下图所示。
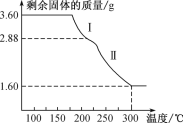
(4) 分析图中数据,写出过程Ⅰ发生反应的化学方程式______________。
(5) 300 ℃时剩余固体是铁的一种氧化物,通过计算确定该氧化物的化学式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为![]() ,下列关于该物质的说法中不正确的是
,下列关于该物质的说法中不正确的是
A. 该物质不能发生消去反应,但能在一定条件下发生加聚反应
B. 该物质不能和AgNO3溶液反应产生AgBr沉淀
C. 该物质在NaOH的醇溶液中加热可转化为醇类
D. 该物质可使溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.过氧化钠和水反应:![]()
B.氯化铝的溶液中加入过量氨水:![]()
C.单质铜与稀硝酸反应:![]()
D.向Fe2(SO4)3的酸性溶液中通入足量HI:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在A、B两个恒容密闭容器中发生反应:2NO2![]() 2NO +O2反应过程中NO2的物质的量随时间变化的状况如图所示。
2NO +O2反应过程中NO2的物质的量随时间变化的状况如图所示。
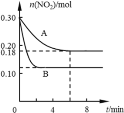
(1)若A容器的体积为5 L,反应经6 min达到平衡状态。0~6 min内用O2浓度变化表示的反应速率为___________________。
(2)写出该反应的化学平衡常数K的表达式:______________________。
(3)说明该反应已达到平衡状态的是_______。
a.v正(NO2)=v逆(NO) b.c(NO2)= c(NO)
c.气体的平均摩尔质量不变 d.气体的密度保持不变
(4)若A、B两容器中只有一个反应条件不同(温度),比较下列物理量。(填“>”、“=”或“<”)
温度 | 反应速率 | 反应的平衡常数 | 反应的热效应(△H) |
TA____TB | vA____vB | KA____KB | △H ____0 |
(5)任写两种能提高二氧化氮转化率的措施_________________、___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下存在反应:2SO2(g) + O2(g) ![]() 2SO3(g),Δ H<0。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按如如图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是
2SO3(g),Δ H<0。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按如如图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是

A. 容器I、III中平衡常数相同
B. 容器II、III中正反应速率相同
C. 容器II、III中的反应达平衡时,SO3的体积分数:II>III
D. 容器I中SO2的转化率与容器II中SO3的转化率之和小于1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置能达到实验目的是(夹持仪器未画出)
A. 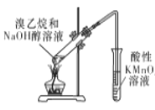 用于检验溴乙烷消去生成的乙烯
用于检验溴乙烷消去生成的乙烯
B. 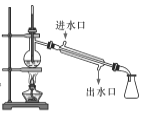 用于石油的分馏
用于石油的分馏
C. 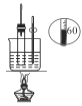 用于实验室制硝基苯
用于实验室制硝基苯
D. 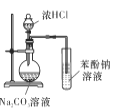 可证明酸性:盐酸>碳酸>苯酚
可证明酸性:盐酸>碳酸>苯酚
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com