
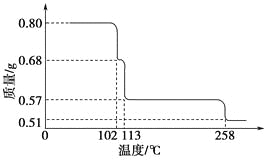
����Ŀ��0.80g CuSO4��5H2O��Ʒ������ˮ���̵���������(��Ʒ�������¶ȱ仯������)����ͼ��ʾ��
��ش��������⣺
��1����ȷ��200��ʱ�������ʵĻ�ѧʽ________(Ҫ��д���ƶϹ���)��
��2��ȡ270��������Ʒ����570�����յõ�����Ҫ�����Ǻ�ɫ��ĩ��һ�����������壬�÷�Ӧ�Ļ�ѧ����ʽΪ________���Ѹú�ɫ��ĩ�ܽ���ϡ�����У���Ũ������ȴ���о����������þ���Ļ�ѧʽΪ____________������ڵ�����¶���________��
��3������������������ˮ��Ӧ����һ�ֻ�����û������Ũ��Һ��Cu�ڼ���ʱ������Ӧ�Ļ�ѧ����ʽΪ________��
��4����0.10mol��L��1����ͭ��Һ�м�����������ϡ��Һ��ֽ��裬��dz��ɫ������ͭ�������ɣ�����Һ��pH��8ʱ��c(Cu2��)��________mol��L��1(Ksp��2.2��10��20)������0.1 mol��L��1����ͭ��Һ��ͨ�����H2S���壬ʹCu2����ȫ����ΪCuS����ʱ��Һ�е�H��Ũ����________mol��L��1��
���𰸡���1��CuSO4��H2O
CuSO4��5H2O![]() CuSO4��(5��n)H2O��nH2O
CuSO4��(5��n)H2O��nH2O
250 18n
0.80g 0.80g��0.57g��0.23g
�ɵ�n��4����200��ʱ�ù������ʵĻ�ѧʽΪCuSO4��H2O
��2��CuSO4![]() CuO��SO3����CuSO4��5H2O��102��
CuO��SO3����CuSO4��5H2O��102��
��3��2H2SO4(Ũ)��Cu![]() CuSO4��SO2����2H2O
CuSO4��SO2����2H2O
��4��2.2��10��8��0.2
�������������������1��CuSO45H2O���ȵ�102��ʱ��ʼ��ˮ�ֽ⣬113��ʱ�ɵõ����ȶ���һ���м����258��ʱ�Ż�����ֽ⣮��200��ʱʧȥ��ˮ������Ϊ0.80g-0.57g=0.23g��
���ݷ�Ӧ�Ļ�ѧ����ʽ��
CuSO45H2O![]() CuSO4(5-n)H2O+nH2O
CuSO4(5-n)H2O+nH2O
250 18n
0.80g 0.80g-0.57g=0.23g
![]() ��
��![]() �����n=4��200��ʱ�ù������ʵĻ�ѧʽΪCuSO4H2O���ʴ�ΪCuSO4H2O��
�����n=4��200��ʱ�ù������ʵĻ�ѧʽΪCuSO4H2O���ʴ�ΪCuSO4H2O��
��2���¶�Ϊ570�����յõ��ĺ�ɫ��ĩӦ��CuO��������������ΪSO3����Ӧ����ʽΪ��CuSO4![]() CuO+SO3����CuO��ϡ���ᷴӦ�IJ���������ͭ��ˮ������Ũ������ȴ�õ��ľ���ΪCuSO45H2O������ڵ����102�����ʴ�Ϊ��CuSO4
CuO+SO3����CuO��ϡ���ᷴӦ�IJ���������ͭ��ˮ������Ũ������ȴ�õ��ľ���ΪCuSO45H2O������ڵ����102�����ʴ�Ϊ��CuSO4![]() CuO+SO3���� CuSO45H2O��102����
CuO+SO3���� CuSO45H2O��102����
��3��SO3��ˮ��Ӧ�������ᣬŨ������ͭ���ȷ�Ӧ�Ļ�ѧ����ʽΪ��2H2SO4(Ũ)+Cu![]() CuSO4+SO2��+2H2O���ʴ�Ϊ��2H2SO4(Ũ)+Cu
CuSO4+SO2��+2H2O���ʴ�Ϊ��2H2SO4(Ũ)+Cu![]() CuSO4+SO2��+2H2O��
CuSO4+SO2��+2H2O��
��4���������Cu(OH)2���ܶȻ�����ȷ��pH=8ʱ��c(OH-)=10-6mol/L��Ksp[Cu(OH)2]=2.2��10-20����c(Cu2+)=2.2��10-8molL-1����0.1molL-1����ͭ��Һ��ͨ�����H2S���壬ʹCu2+��ȫ����ΪCuS����ʱ��Һ�е�����Ϊ���ᣬc(SO42-)���䣬Ϊ0.1molL-1���ɵ���غ��֪c(H+)Ϊ0.2molL-1���ʴ�Ϊ��2.2��10-8��0.2��


 ����ѧ����ϵ�д�
����ѧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B���������������Ϣ���£�
A ����ȫȼ�յIJ�����n��CO2����n��H2O��=2��1
��28��M ��A����60
�۲���ʹ������Ȼ�̼��Һ��ɫ��һ�ȴ���ֻ��һ�ֽṹ
B �ٱ���������ͨ������³���̬����ͬ���칹��
�۶������������
�ش��������⣺
��1����A��ʵ��ʽ�� ��
��2����A�Ľṹ��ʽ�� ��
��3����B�����ֶ������Ľṹ��ʽΪ �� �� ��
��4����CΪ��B��ͬϵ�������Ϊ��̬��ֻ��һ��һ��������C��һ�����Ľṹ��ʽΪ ����һ�ּ��ɣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ɫ��ҺX��ͨ������Y����Һ����ɫ�����ж�X��Y���ƶ���ȷ����( )
A����XΪƷ����Һ����Yһ����Cl2��SO2
B����XΪ����̪������������Һ����Y������SO2
C����XΪ��KSCN���Ȼ�����Һ����Yһ����HI
D����XΪ���������Ƶ�ʯ����Һ����Y������SO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����(��NA���������ӵ�������ֵ)
A���κ������£�16gCH4��18 g H2O�����е�������Ϊ10NA
B��19g��H3O+ �����к��еĵ�����Ϊ11NA
C��0.5mol/LH2SO4�е�H+��ΪNA
D��22.4 L��CO������1 mol N2�����ĵ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ1��ͭпԭ���ʾ��ͼ��ͼ2�У�x���ʾʵ��ʱ���������ĵ��ӵ����ʵ�����y���ʾ

A��ͭ�������� B��c(Zn2+)
C��c(H+) D��c(SO42-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����г��ӷ���������ǣ� ��
ѡ�� | ���ᴿ������ | ���� | �����Լ� | ���ӷ��� |
A | CO(g) | CO2(g) | NaOH��Һ��ŨH2SO4 | ϴ�� |
B | NH4Cl(aq) | Fe3+(aq) | NaOH��Һ | ���� |
C | Cl2(g) | HCl(g) | ����ʳ��ˮ��ŨH2SO4 | ϴ�� |
D | Na2CO3(s) | NaHCO3(s) | ���� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ���Ľ̲��ϵ��ܽ��Ա�ʱ���֣�CuCO3��Ӧ��Ϊ����������ʾ�����ڻ���ˮ�ͷֽ⡣��֪ͭ���ӵij�������ΪCu(OH)2����ɫ����Cu2(OH)2SO4(��ɫ)��Cu2(OH)2CO3����ɫ���ȣ����Ǿ������ᾧˮ��Ϊ��̽��CuSO4��Na2CO3��Ӧ����ijɷݣ���ͬѧ������ʵ�鷽���Ʊ������ֳ������������̽�������ɷݵ�ʵ�顣
ȡ2��С�ձ���2����ƿ����ÿ���ձ������50mL0.5mol/L��CuSO4��Һ������ƿ��ֱ����40mL ��50mL0.5mol/LNa2CO3��Һ������70��ˮ��ˮԡ���ȣ�Ȼ��CuSO4��Һ���뵽Na2CO3��Һ�У�����ˮԡ���������ݲ����������Ӻ�ֱ�õ�����ɫ����ɫ���������ˡ�ϴ�ӡ�����õ����ݹ��塣
I��������ɫ�����ɷݵ�̽����
ͨ���ұ�ʵ��֤ʵ�������к���Cu2(OH)2CO3��Cu2(OH)2SO4

��1��֤����Cu2(OH)2CO3���ڵ�����Ϊ____________��
��2���Լ���Ϊ__________��֤����Cu2(OH)2SO4���ڵ�����Ϊ______________��
II������ɫ�����ɷݵ�̽��
�ظ�Iʵ�飬����û��SO42-���ڣ���Cu2(OH)2CO3���ڣ�
ͨ������ʵ��֤ʵ��������ֻ��Cu2(OH)2CO3

��3����ͬѧ��ͨ����������ֽ����������������ȷ�������ijɷݣ�������˼·��װ��װ�ã�������Ӧ��ҩƷ����ָ������ҩƷ��Ŀ�ġ�

��4�����ո�ͬѧ�����˼·��ֻ��ⶨij����װ�õ������仯������m (_______������m(_______��=_______ʱ����������дװ�õ���ţ��Ϳ�ȷ��������Cu2(OH)2CO3��
��5�����ۣ�n(Cu2+):n(CO32-)>1ʱ�����ù��������Cu2(OH)2CO3��Cu2(OH)2SO4 ��n(Cu2+):n(CO32-)��1ʱ�����ù������ȫ����Cu2(OH)2CO3�����ɸó���������Ӧ�����ӷ���ʽΪ��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���٢ڢۢ����ֽ���Ƭ������������ϡ�����ж������ԭ��أ��٢�����ʱ�����·�����������������٢�����ʱ����Ϊ�������ڢ�����ʱ�������������ݳ����ۢ�����ʱ�������������١��ݴ��ж������ֽ�������ɴ�С��˳����
A���٢ۢڢ� B���٢ۢܢ� C���ۢܢڢ� D���ۢ٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��M��R��X��YΪԭ��������������Ķ���������Ԫ�أ�Z��һ�ֹ���Ԫ�ء�M��̬ԭ��L����p�����������s�����������2����R��ͬ����Ԫ��������õĽ���Ԫ�أ�X��M�γɵ�һ�ֻ������������������Ҫ������Ⱦ�Z�Ļ�̬ԭ��4s��3d������������ش��������⣺
��1��R��̬ԭ�ӵĵ����Ų�ʽ�� ��X��Y�е縺�Խϴ���� ����Ԫ�ط��ţ���
��2��X���⻯��ķе��������������Ƶ�M���⻯���ԭ����___________��
��3��X��M�γɵ�XM3���ӵĿռ乹����__________��
��4��M��R���γɵ�һ�����ӻ�����R2M����ľ�����ͼ��ʾ����ͼ�к��������������_________�������ӷ��ţ���

��5����ϡ�����У�Z����ۺ�����ļ��Σ���ɫ������M��һ���⻯�Z����ԭΪ+3�ۣ��÷�Ӧ�Ļ�ѧ����ʽ��____________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com