
【题目】已知强酸与强碱在稀溶液里反应的中和热可表示为:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1对下列反应:
CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) ΔH=-Q1kJ·mol-1
![]() H2SO4(浓)+NaOH(aq)=
H2SO4(浓)+NaOH(aq)=![]() Na2SO4(aq)+H2O(l) ΔH=-Q2kJ·mol-1
Na2SO4(aq)+H2O(l) ΔH=-Q2kJ·mol-1
HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-Q3kJ·mol-1
上述反应均在溶液中进行,则下列Q1、Q2、Q3的关系正确的是( )
A.Q2>Q3>Q1B.Q2>Q1>Q3C.Q1=Q2=Q3D.Q2=Q3>Q1
【答案】A
【解析】
强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)=H2O△H=一57.3kJ/mol;则热化学方程式HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(l)△H=-Q3kJmol-1 中的Q3=57.3kJ;而由于醋酸是弱电解质,电离吸热,故热化学方程式CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H=-Q1 kJmol-1 中的Q1<57.3KJ;而浓硫酸稀释放热,故热化学方程式![]() H2SO4(浓)+NaOH(aq)═
H2SO4(浓)+NaOH(aq)═![]() Na2SO4(aq)+H2O(l)△H=-Q2kJmol-1 中的Q2>57.3KJ,故放出的热量为Q2>Q3>Q1,故答案为A。
Na2SO4(aq)+H2O(l)△H=-Q2kJmol-1 中的Q2>57.3KJ,故放出的热量为Q2>Q3>Q1,故答案为A。


科目:高中化学 来源: 题型:
【题目】在一定条件下,向![]() 和过量C粉的混合物中通入氯气,可制得易水解的
和过量C粉的混合物中通入氯气,可制得易水解的![]() ,实验装置如图所示。下列说法不正确的是
,实验装置如图所示。下列说法不正确的是 ![]()
![]()
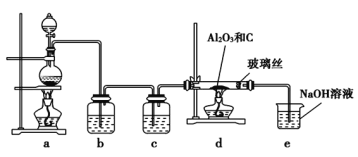
A.c中盛装的是浓硫酸
B.实验结束时,应先熄灭d处酒精灯,待装置冷却后再熄灭a处酒精灯
C.此反应中的尾气除氯气外都可直接排放到大气中
D.该装置不完善,其中应改进的一项是在d、e之间添加一个干燥装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在湿法炼锌的电解循环溶液中,较高浓度的![]() 会腐蚀阳极板而增大电解能耗。可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去
会腐蚀阳极板而增大电解能耗。可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去![]() 。根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是
。根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是

A. ![]() 的数量级为
的数量级为![]()
B. 除![]() 反应为Cu+Cu2++2
反应为Cu+Cu2++2![]() =2CuCl
=2CuCl
C. 加入Cu越多,Cu+浓度越高,除![]() 效果越好
效果越好
D. 2Cu+=Cu2++Cu平衡常数很大,反应趋于完全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列各溶液中,离子一定能大量共存的是( )
A. 室温下,pH=1的溶液中:Na+、Fe3+、NO![]() 、SO
、SO![]()
B. 含有0.1 mol·L-1 Fe3+的溶液中:K+、Mg2+、I-、NO![]()
C. 加入铝粉有气泡产生的溶液中:Na+、NH![]() 、Fe2+、NO
、Fe2+、NO![]()
D. 在AlCl3溶液中:K+、Na+、SiO![]() 、SO
、SO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3及其盐都是重要的化工原料。
(1)用NH4Cl和Ca(OH)2制备NH3,反应发生、气体收集和尾气处理装置依次为_____。
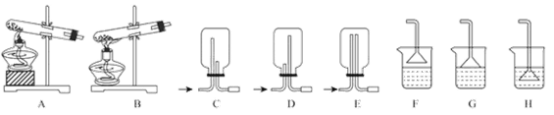
(2)按下图装置进行NH3性质实验。
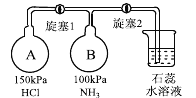
①先打开旋塞1,B瓶中的现象是_______,原因是__________,稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是_________________。
(3)设计实验,探究某一种因素对溶液中NH4Cl水解程度的影响。
限制试剂与仪器:固体NH4Cl、蒸馏水、100mL容量瓶、烧杯、胶头滴管、玻璃棒、药匙、天平、pH计、温度计、恒温水浴槽(可控制温度)
①实验目的:探究______对溶液中NH4Cl水解程度的影响。
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量及需拟定的数据,数据用字母表示;表中V(溶液)表示所配制溶液的体积)。_________________
物理量 | V(溶液)/mL | …… | |||
1 | 100 | ||||
2 | 100 |
③按实验序号I所拟数据进行实验,若读取的待测物理量的数值为Y,则NH4Cl水解反应得平衡转化率
为_____(只列出算式,忽略水自身电离的影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了使宇航员在飞船中得到一个稳定的、良好的生存环境,一般在飞船内安装盛有Na2O2或K2O2颗粒的装置,它的用途是产生氧气。下列关于Na2O2的叙述正确的是
①Na2O2中阴、阳离子的个数比是1∶1
②Na2O2分别与水及CO2反应产生等量氧气时,需水和CO2的质量相等
③Na2O2分别与水及CO2反应产生等量氧气时,转移电子的物质的量相等
④Na2O2的漂白原理与SO2的漂白原理相同
⑤Na2O2与SO2反应生成Na2SO3与O2
⑥Na2O2能与酸反应生成盐和水,所以Na2O2是碱性氧化物
⑦Na2O2与水反应,Na2O2既是氧化剂,又是还原剂
⑧Na2O2投入到紫色石蕊溶液中,溶液先变蓝,后褪色
A.①③⑥⑧B.③⑦⑧
C.②⑤⑥⑦D.①④⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧钒![]() 碱式碳酸铵
碱式碳酸铵![]() 难溶于水
难溶于水![]() 化学式为
化学式为![]() ,它是制备热敏材料
,它是制备热敏材料![]() 的原料。
的原料。![]() 价钒在弱酸性条件下具有还原性。一种制备氧钒
价钒在弱酸性条件下具有还原性。一种制备氧钒![]() 碱式碳酸铵方案如下:
碱式碳酸铵方案如下:
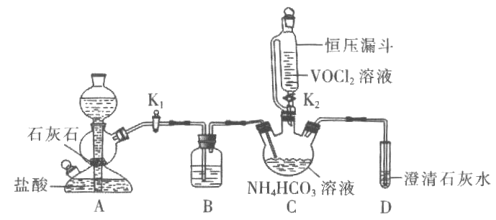
请回答下列问题:
(1)![]() 装置盛装的试剂是________
装置盛装的试剂是________![]() 填名称
填名称![]() 。A中反应的离子方程式为________。相对分液漏斗,恒压漏斗优点是________。
。A中反应的离子方程式为________。相对分液漏斗,恒压漏斗优点是________。
(2)实验时,先关闭![]() ,打开
,打开![]() ,当________
,当________![]() 填实验现象
填实验现象![]() 时,后________
时,后________![]() 填实验操作
填实验操作![]() 。
。
(3)实验完毕后,从C装置中分离产品的操作方法是________![]() 填操作名称
填操作名称![]() 。
。
(4)测定粗产品中钒的含量。实验步骤如下:
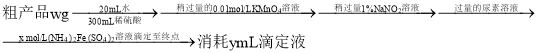
已知:滴定反应为![]()
![]() 该粗产品中钒的质量分数的表达式为________
该粗产品中钒的质量分数的表达式为________![]() 。
。
![]() 若滴定前仰视读数,终点时俯视读数,则测得结果________填“偏高”、“偏低”或“无影响”
若滴定前仰视读数,终点时俯视读数,则测得结果________填“偏高”、“偏低”或“无影响”![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式见图,下列说法正确的是( )
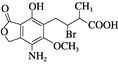
A. 分子式为C14H16O6NBr
B. 该分子中含有两个手性碳原子
C. 不能使酸性高锰酸钾溶液褪色
D. 在一定条件下与氢氧化钠溶液反应,1 mol该有机物最多消耗3 mol NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com