
【题目】下列离子方程式书写正确的是
A. 明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:2Ba2++3OH-+Al3++2SO42-=2BaSO4↓+Al(OH)3↓
B. 用惰性电极电解AlCl3溶液产生白色沉淀:2Al3++6Cl-+6H2O![]() Al(OH)3↓+3H2↑+3Cl2↑
Al(OH)3↓+3H2↑+3Cl2↑
C. 用酸性K2Cr2O7溶液检验酒精:3CH3CH2OH+2Cr2O72-+2H2O=4Cr(OH)3↓+3CH3COO-+OH-
D. 用足量的氨水处理硫酸工业的尾气:SO2+NH3·H2O=NH4++HSO3-
【答案】B
【解析】
A.明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀,明矾与氢氧化钡的物质的量之比为1:2,反应生成偏铝酸根离子,正确的离子方程式为:2Ba2++4OH-+Al3++2SO42-=2BaSO4↓+AlO2-+2H2O,故A错误;
B.用惰性电极电解AlCl3溶液,阴极周围的氢离子放电,产生氢氧根离子与铝离子反应生成氢氧化铝白色沉淀,方程式为2Al3++6Cl-+6H2O![]() 2Al(OH)3↓+3H2↑+3Cl2↑,故B正确;
2Al(OH)3↓+3H2↑+3Cl2↑,故B正确;
C.用酸性K2Cr2O7溶液检验酒精,生成的醋酸不能拆开,正确的离子方程式为:3CH3CH2OH+2Cr2O72-+16H+=4Cr3++11H2O+3CH3COOH,故C错误;
D.用足量的氨水处理硫酸工业的尾气,反应生成亚硫酸铵,正确的离子方程式为:SO2+2NH3H2O=2NH4++SO32-,故D错误;
答案选B。


 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,向容积固定为a L的密闭容器中充入1 mol X气体和2 mol Y气体,发生反应X(g)+2Y(g) ![]() 2Z(g),此反应达到平衡状态的标志是( )
2Z(g),此反应达到平衡状态的标志是( )
A. 容器内气体密度不随时间变化 B. 容器内各物质的浓度不随时间变化
C. 容器内X、Y、Z的浓度之比为1∶2∶2 D. 单位时间内消耗0.1 mol X,同时生成0.2 mol Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2H2(g)+ O2(g) = 2H2O(g),H—H、O=O和O—H键的键能分别为436 kJ·mol-1、496 kJ·mol-1和462 kJ·mol-1,则2mol H2完全燃烧放出的热量为
A. 480 kJ B. 916 kJ C. 960 kJ D. 190 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A.用金属钠可区分乙醇和乙醚B.用高锰酸钾酸性可区分乙烷和3-己烯
C.用水可区分苯和溴苯D.用新制的银氨溶液可区甲酸甲酯和乙醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100kPa时,1mol石墨转化为金刚石的能量变化如右图所示,下列说法正确的是
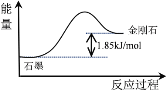
A. 石墨比金刚石更稳定
B. 金刚石比石墨更稳定
C. 石墨转化为金刚石的反应为放热反应
D. 破坏1mol石墨化学键所吸收的能量小于形成1mol金刚石化学键所放出的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组进行以下实验探究:


Ⅰ. 设计实验探究反应速率的测定和比较
实验步骤:
(1)取一套装置(装置如图所示),加入40 mL 1 mol·L-1的硫酸,测量收集10 mL H2所需的时间。
(2)取另一套装置,加入40 mL 4 mol·L-1的硫酸,测量收集10 mL H2所需的时间。
实验现象: 锌跟硫酸反应产生气泡,收集10 mL气体,(2)所用时间比(1)所用时间________(填“长”或“短”);
实验结论: 4 mol·L-1硫酸与锌反应比1 mol·L-1硫酸与锌反应速率______(填“大”或“小”)。
注意事项:① 锌粒的颗粒(即表面积)大小________________;
② 40 mL的硫酸要迅速加入;
③ 装置____________________,且计时要迅速准确;
④ 气体收集可以用排水量气装置代替。
实验讨论:除本实验测定反应速率的方法外,可行的方案还有(任写一种)
________________________________________________________________。
Ⅱ. 探究用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素,所用HNO3浓度为1.00 mol·L-1、2.00 mol·L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K。
请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
实验编号 | T(K) | 大理石规格 | HNO3浓度 (mol·L-1) | 实验目的 |
① | 298 | 粗颗粒 | 2.00 | (1)实验①和②探究HNO3浓度对该反应速率的影响 (2)实验①和_____探究温度对该反应速率的影响 (3)实验①和_____探究大理石规格(粗、细)对该反应速率的影响 |
② | _____ | ________ | _________ | |
③ | _____ | 粗颗粒 | _________ | |
④ | ______ | ______ | ________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由钠和氧组成的某种离子晶体含钠的质量分数是69/109,其阴离子只有过氧离子(O22-)和氧离子(O2-)两种。在此晶体中,氧离子和过氧离子的物质的量之比为
A. 2∶1 B. 1∶2 C. 1∶1 D. 1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,在20.00 mL 0.1 mol·L-1 C6H5COOH(苯甲酸)溶液中滴加0.1 mol·L-1 NaOH溶液,溶液中离子浓度与pH关系如图所示。下列说法正确的是
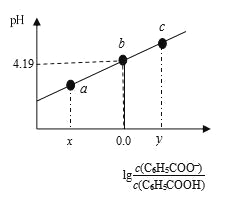
A. a点:溶液中c(Na+)>c(C6H5COO-)>c(H+)>c(OH-)
B. b点:对应的NaOH溶液体积为10 mL
C. 对b点溶液加热(不考虑挥发),实现曲线由b点向c点的变化
D. 298K时,C6H5COOH的电离常数为1×10-4.19
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列试剂的保存方法正确的是( )
A.浓硝酸保存在无色玻璃瓶中B.少量的白磷保存在冷水中
C.浓硫酸用橡胶塞细口瓶密闭保存D.烧碱溶液保存在玻璃塞试剂瓶中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com