
【题目】图中A为淡黄色固体,B的阳离子与A相同(其他物质均略去).

根据以上关系,回答下列问题:
(1)A的电子式为_____,D的结构式为_____(写化学式)
(2)请用化学方程式表示A在潜水艇中的一种重要用途_____.
(3)若A、B按物质的量之比1:1.5混合在密闭容器中加热充分反应后,排出气体,则剩余的固体为_________(写化学式)
(4)若A、B按物质的量之比1:2混合,写出A、B混合物中加足量水反应的化学反应方程式______________(用一个方程式表)
【答案】 ![]()
![]() 2Na2O2+2CO2═2Na2CO3+O2 NaOH、 Na2CO3 2Na2O2+ 4NaHCO3= 4Na2CO3+O2↑+2H2O
2Na2O2+2CO2═2Na2CO3+O2 NaOH、 Na2CO3 2Na2O2+ 4NaHCO3= 4Na2CO3+O2↑+2H2O
【解析】图中A为淡黄色固体,则A为Na2O2,A与B在加入稀硫酸或加热或加水都能产生气体C,结合D通入E能产生B,且B的阳离子与A相同,则B为NaHCO3,A、B和水反应生成的E为Na2CO3,气体为氧气,D为二氧化碳。则(1)A是Na2O2,其电子式为![]() ,D的结构式为
,D的结构式为![]() ;(2)A在潜水艇中的一种重要用途:2Na2O2+2CO2═2Na2CO3+O2;(3)若A、B按物质的量之比1:1.5混合在密闭容器中加热充分反应后,排出气体,可能发生的反应及各物质的量如下:
;(2)A在潜水艇中的一种重要用途:2Na2O2+2CO2═2Na2CO3+O2;(3)若A、B按物质的量之比1:1.5混合在密闭容器中加热充分反应后,排出气体,可能发生的反应及各物质的量如下:
2NaHCO3![]() Na2CO3+ CO2↑ + H2O、
Na2CO3+ CO2↑ + H2O、
1.5mol 0.75mol 0.75mol 0.75mol
2Na2O2+ 2CO2 ═ 2Na2CO3+O2、
1mol 0.75mol 0.75mol
2Na2O2+ 2H2O ═ 4NaOH+O2↑、
(1-0.75)mol 0.75mol 0.5mol
根据反应:Na2O2+ 1.5NaHCO3= 0.5NaOH + 1.5Na2CO3+ O2↑,则剩余的固体为NaOH、 Na2CO3;(4)若A、B混合加足量水反应的化学反应有Na2O2+ 2CO2 ═2Na2CO3+O2、NaOH +NaHCO3= Na2CO3+ H2O,若按物质的量之比1:2混合,则反应的化学方程式为2Na2O2+ 4NaHCO3= 4Na2CO3+O2↑+2H2O。


科目:高中化学 来源: 题型:
【题目】实验室欲用NaOH固体配制1.0mol/L的NaOH溶液240mL.一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤移液 ⑥洗涤 ⑦定容 ⑧冷却 ⑨摇动
(1)配制溶液时,其正确的操作顺序为(填序号).本实验必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、、 .
(2)某同学欲称量NaOH的质量,先用托盘天平称量烧杯的质量,托盘天平平衡后的状态如图所示.烧杯的实际质量为g,要完成本实验该同学应称量g NaOH. 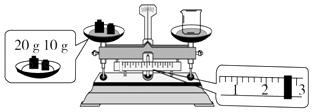
(3)使用容量瓶前必须进行的一步操作是 .
(4)配制过程中,下列操作会引起所配溶液浓度偏高的是(填序号).
A.转移溶液时,有少量溶液洒到容量瓶外面
B.定容时俯视刻度线
C.未冷却至室温就将溶液移入容量瓶中并定容
D.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加蒸馏水至刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应4CO+2NO2![]() N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
A. υ(CO)=1.5 mol·L-1·min-1 B. υ(NO2)=0.7 mol·L-1·min-1
C. υ(N2)=0.4 mol·L-1·min-1 D. υ(CO2)=1.1 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质的比较,结论正确的是
A. 碱性:LiOH<RbOH
B. 溶解度:Na2CO3<NaHCO3
C. 热稳定性:PH3<SiH4
D. 沸点:C2H5OH<C2H5SH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体化合物A不导电,但熔化或溶于水都能完全电离。下列关于物质A的说法中正确的是
A. A是共价化合物 B. A是离子化合物
C. A为非电解质 D. A为弱电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。

(1)实验室制氯气的化学方程式为____________________________。
(2)装置B中饱和食盐水的作用是______________;请写出装置B的另一个作用_________________________________。
(3)装置C的实验目的是验证氯气是否具有漂白性, 为此C中Ⅰ、Ⅱ、Ⅲ依次放入物质的组合是________(填编号)。
编号 | a | b | c | d |
Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是____________________,该现象_______(填“能”或“不能”)说明溴的非金属性强于碘,原因是_______________。
(5)有人提出,装置F中可改用足量的Na2SO3溶液吸收余氯,试写出相应的离子反应方程式:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生产和生活中有重要的应用,下列说法不正确的是
A. 小苏打在生活中可用做发酵粉
B. 过氧化钠可用于呼吸面具中氧气的来源
C. 可溶性铁盐或铝盐可用于净水
D. 碳酸钠常用于治疗胃病
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学键的说法正确的是
A. 任何非金属单质分子中一定含有共价键
B. 离子化合物中可能存在共价键,共价化合物中也可能存在离子键
C. 离子化合物中可能存在共价键,但共价化合物中一定不存在离子键
D. MgF2中既含有离子键又含有共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com