
【题目】将m g镁铝合金投入到500 ml 2 mol/L的盐酸中,固体完全溶解,收集到气体5.6L (标准状况下)。向反应所得溶液中加入4mol/L的氢氧化钠溶液,沉淀达到最大值为13.60 g,则m的值为
A. 11.48 B. 9.35 C. 8.50 D. 5.10
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下表是元素周期表中的一部分,根据A~M在周期表中的位置,回答下列问题:

(1)表中元素,化学性质最不活泼的是_______,氧化性最强的单质是________,还原性最强的单质是____。(写元素符号或化学式)
(2)表中元素的最高价氧化物对应的水化物中,碱性最强的化合物的化学式为________,酸性最强的化合物的化学式为___________,呈两性的化合物的化学式为___________。
(3)A分别与B、C、D、E、J、K、L、M形成的化合物中最稳定的是_______(写化学式)。
(4)写出D、G、L对应的离子半径由大到小的顺序________(用离子符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各溶液中,Na+浓度最大的是
A. 0.5 L 0.8 mol·L-1的Na2SO4溶液
B. 2 L 1 mol·L-1的NaOH溶液
C. 1 L 1.2 mol·L-1的NaCl溶液
D. 3 L 0.5 mol·L-1的Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaC1O、NaClO3的混合溶液,经测定,ClO-与ClO3-的物质的量浓度之比为1:3,则此反应中被还原的氯元素与被氧化的氯元素原子的物质的量之比是
A. 1: 4 B. 11:3 C. 3:1 D. 4:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某品牌化妆品的主要成分Z具有美白功效,原从杨树中提取,现可用如下图所示反应合成。下列对X、Y、Z的叙述,正确的是

A. X、Y和Z均能和NaOH溶液反应
B. X和Z均能和Na2CO3溶液反应,但不能和NaHCO3溶液反应
C. Y既能发生加聚反应,也能发生缩聚反应
D. Y分子中所有原子不可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种短周期主族元素,原子序数依次增大。其中B的单质在常温下为双原子分子,它与A的单质可形成分子X,X的水溶液呈碱性;D的简单阳离子与X具有相同电子数,且D是同周期中简单离子半径最小的元素;E元素的原子最外层比次外层少两个电子,C、F两种元素的原子最外层共有13个电子。则
(l)这六种元素分别为A_____、B_____、C _____、D_____、E_____、F_____(填元素名称)。
(2)E的离子结构示意图_____;X的电子式_____;
(3)B、C、E分别与A形成的化合物中最稳定的是_____(写化学式);
(4)DF3所含化学键类型_____、DF3与过量的强碱反应的离子反应方程式__________;
(5)F的单质在反应中常作_____剂,该单质的水溶液与E的低价氧化物反应的离子方程式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关,下列有关说法正确的是 ( )
A. 医院里的血液透析利用了胶体的性质
B. PM2.5中含有铅、铬、钒、砷等对人体有害的金属元素
C. 工业冶炼铝常用焦炭还原氧化铝
D. 煤经过气化和液化的物理变化可变为清洁燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;钴以Co2O3CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中.从废料中回收氧化钴(CoO)的工艺流程如下:
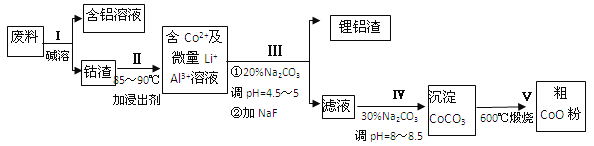
(1)过程I中采用NaOH溶液溶出废料中的Al,反应的离子方程式为 .
(2)过程II中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴.则浸出钴的离子反应方程式为 (产物中只有一种酸根).请从反应原理分析不用盐酸浸出钴的主要原因 .
(3)碳酸钠溶液在过程III和IV中所起作用有所不同,请分别用离子方程式表示在过程III、IV中起的作用: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列每组物质发生状态变化时所克服的微粒间的相互作用属于同种类型的是( )
A.食盐和蔗糖熔化
B.金刚石和硫熔化
C.碘和干冰升华
D.二氧化硅和氧化钠熔化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com