
【题目】用化学知识填空:
(1)丙烷通过脱氢反应可得丙烯。
已知:①C3H8(g)= CH4(g)+C2H2(g)+H2(g) ΔH1=+156.6 kJ·mol![]()
②C3H6(g)= CH4(g)+C2H2(g) ΔH2=+32.4 kJ·mol![]()
则相同条件下,反应C3H8(g)=== C3H6(g)+H2(g)的ΔH=__________kJ·mol![]() 。
。
(2)将煤转化为水煤气是通过化学方法将煤转化为洁净燃料的方法之一。煤转化为水煤气的主要化学反应为C(s)+H2O(g) ![]() CO(g)+H2(g)。C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为
CO(g)+H2(g)。C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为
C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol![]()
H2(g)+![]() O2(g)===H2O(g) ΔH2=-242.0 kJ·mol
O2(g)===H2O(g) ΔH2=-242.0 kJ·mol![]()
CO(g)+![]() O2(g)===CO2(g) ΔH3=-283.0 kJ·mol
O2(g)===CO2(g) ΔH3=-283.0 kJ·mol![]()
写出C(s)与水蒸气反应生成CO和H2的热化学方程式: ______________________。
(3)3mol甲烷燃烧时,生成液态水和二氧化碳,同时放出2 670.9kJ的热量,写出甲烷燃烧热的热化学方程式_________________________________________________
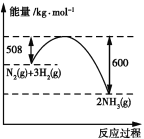
(4)如图是298 K、101 kPa时,N2与H2反应过程中能量变化的曲线图。该反应的热化学方程式为____________。
(5)已知:H2(g)+Cl2(g)===2HCl(g) ΔH=-185 kJ·mol![]() Cl—Cl 的键能为247 kJ·mol
Cl—Cl 的键能为247 kJ·mol![]() ,H—H的键能为436kJ·mol
,H—H的键能为436kJ·mol![]() 则H—Cl的键能为______________kJ·mol
则H—Cl的键能为______________kJ·mol![]()
【答案】+124.2 C(s)+H2O(g) === CO(g) +H2(g) ΔH=+131.5 kJ·mol-1 CH4(g)+2O2(g) === CO2(g) +2 H2O (l) ΔH=-890.3 kJ·mol-1 N2(g)+3H2(g) 2NH3(g) △H=-92 kJ·mol-1 434
【解析】
从盖斯定律、燃烧热的定义、反应热与焓变的关系角度进行分析;
(1)利用盖斯定律,根据目标反应方程式,因此有①-②得出△H=△H1-△H2=+156.6kJ·mol-1-(+32. 4kJ·mol-1)=+124.2kJ·mol-1,
故答案为+124.2kJ·mol-1;
(2)C(s)+H2O(g) ![]() CO(g)+H2(g) ①,H2(g)+
CO(g)+H2(g) ①,H2(g)+![]() O2(g)===H2O(g) ②,CO(g)+
O2(g)===H2O(g) ②,CO(g)+![]() O2(g)===CO2(g) ③,利用盖斯定律,得出①-②-③得出:△H=△H1-△H2-△H3=(-393.5kJ·mol-1)-(-242.0kJ·mol-1-283.0kJ·mol-1)=+131.5kJ·mol-1,则热化学反应方程式为C(s)+H2O(g) = CO(g) +H2(g) ΔH=+131.5 kJ·mol-1,
O2(g)===CO2(g) ③,利用盖斯定律,得出①-②-③得出:△H=△H1-△H2-△H3=(-393.5kJ·mol-1)-(-242.0kJ·mol-1-283.0kJ·mol-1)=+131.5kJ·mol-1,则热化学反应方程式为C(s)+H2O(g) = CO(g) +H2(g) ΔH=+131.5 kJ·mol-1,
故答案为C(s)+H2O(g) = CO(g) +H2(g) ΔH=+131.5 kJ·mol-1;
(3)根据燃烧热的定义,得出1mol甲烷完全燃烧放出的热量为![]() ==890.3kJ·mol-1,因此甲烷燃烧热的热化学方程式为CH4(g)+2O2(g) = CO2(g) +2 H2O (l) ΔH=-890.3 kJ·mol-1,
==890.3kJ·mol-1,因此甲烷燃烧热的热化学方程式为CH4(g)+2O2(g) = CO2(g) +2 H2O (l) ΔH=-890.3 kJ·mol-1,
故答案为CH4(g)+2O2(g) = CO2(g) +2 H2O (l) ΔH=-890.3 kJ·mol-1;
(4)根据图像,反应物总能量大于生成物的总能量,即该反应为放热反应,因此△H=(508kJ·mol-1-600kJ·mol-1)=92kJ·mol-1,热化学反应方程式为N2(g)+3H2(g) ![]() 2NH3(g) △H=-92 kJ·mol-1,
2NH3(g) △H=-92 kJ·mol-1,
故答案为N2(g)+3H2(g) ![]() 2NH3(g) △H=-92 kJ·mol-1;
2NH3(g) △H=-92 kJ·mol-1;
(5)利用△H=反应物键能总和-生成物键能总和,令H-Cl的键能为akJ·mol-1,则有:436kJ·mol-1+247kJ·mol-1-2akJ·mol-1=-185kJ·mol-1,解得a=434kJ·mol-1,
故答案为434kJ·mol-1。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】近年来,金属—空气电池的研究和应用取得很大进步,这种新型燃料电池具有比能量高、污染小、应用场合多等多方面优点。铝—空气电池工作原理如图所示。关于金属—空气电池的说法不正确的是( )

A.铝—空气电池(如上图)中,铝作负极,电子通过外电路到正极
B.为帮助电子与空气中的氧气反应,可使用活性炭作正极材料
C.碱性溶液中,负极反应为Al(s)+3OH-(aq)=Al(OH)3(s)+3e-,每消耗2.7 g Al(s),需耗氧6.72 L(标准状况)
D.金属—空气电池的可持续应用要求是一方面在工作状态下要有足够的氧气供应,另一方面在非工作状态下能够密封防止金属自腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列六种短周期元素(用字母x等表示)。最高正价或最低负价与原子序数关系如图所示。

根据判断出的元素回答问题:
(1)f在周期表中的位置是______。已知x为非金属元素,由x、e、g三种元素组成的离子化合物的电子式:______。
(2)上述元素简单离子半径最大的是(用化学式表示,下同):___;比较g、h的最高价氧化物对应水化物的酸性强弱:_____。
(3)已知1mole的单质在足量d2中燃烧,恢复至室温,放出255.5 kJ热量,写出该反应的热化学方程式:__________。
(4)x和d组成的化合物中,既含有极性共价键又含有非极性共价键的是____(填化学式),此化合物可将碱性工业废水中的CN-氧化,生成碳酸盐和氨气,相应的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室制备乙炔并进行性质验证的装置(夹持仪器己略去)。
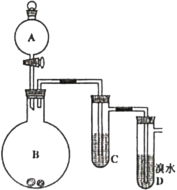
(1)实验室制备乙炔的方程式为___;
(2)仪器A的名称为___,为防止气体生成的速率过快,由A滴入B的试剂为___;
(3)装置C可选用的试剂为___(写出一种即可),其作用为___;
(4)反应开始后,D中的现象为___,所发生反应的反应类型为___;
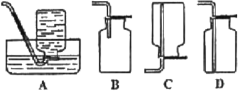
(5)D中验证实验结束后。B中反应仍在继续。此时可撤去装置D,在装置C之后连接收集装置,以下装置中最适合用于收集乙炔的是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将碳酸钠和碳酸氢钠的固体混合物Wg溶于水制成500mL溶液,钠离子的物质的量浓度为0.8mol·L-1,若将Wg该混合物用酒精灯加热至质量不再改变时,得到的固体物质的质量可能是
A. 21.2g B. 6.2g C. 8.4g D. 10.6g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是

A. 图1表示的反应为放热反应
B. 图1中Ⅰ、Ⅱ两点的速率v(Ⅰ)>v(Ⅱ)
C. 图2表示A(?)+2B(g)![]() 2C(g) ΔH<0,达平衡后,在t1、t2、t3、t4时都只改变了一种外界条件的速率变化,由图可推知A不可能为气体
2C(g) ΔH<0,达平衡后,在t1、t2、t3、t4时都只改变了一种外界条件的速率变化,由图可推知A不可能为气体
D. 图3装置的总反应为4Al+3O2+6H2O=4Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
A.光照新制的氯水时,溶液的pH逐渐减小
B.高温,使N2和H2转化为更多的NH3(△H<0)
C.可用浓氨水和氢氧化钠固体快速制取氨气
D.增大压强,有利于SO2和O2反应生成SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关硫元素及其化合物的说法或描述正确的是( )
A.硫黄矿制备硫酸经历两步:S![]() SO3
SO3![]() H2SO4
H2SO4
B.酸雨与土壤中的金属氧化物反应后,硫元素以单质的形式进入土壤中
C.在燃煤中加入石灰石可减少SO2排放,发生的反应为2CaCO3+2SO2+O2![]() 2CO2+2CaSO4
2CO2+2CaSO4
D.土壤中的闪锌矿(ZnS)遇到硫酸铜溶液转化为铜蓝(CuS),说明CuS很稳定,不具有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】网络趣味图片“一脸辛酸”,是在人脸上重复画满了辛酸的键线式结构。下列有关辛酸的叙述正确的是

A. 辛酸的羧酸类同分异构体中,含有三个“-CH3”结构,且存在乙基支链的共有7种
B. 辛酸的同分异构体(CH3)3CCH(CH3)CH2COOH的名称为2,2,3一三甲基戊酸
C. 正辛酸常温下呈液态而软脂酸常温下呈固态,故二者不符合同一通式
D. 辛酸的同分异构体中能水解生成相对分子质量为74的有机物的共有8种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com