
【题目】用下图所示装置除去含有CN-、Cl-废水中的CN-时,控制溶液的pH值为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是

A. 用石墨作阳极,铁作阴极
B. 阳极的电极反应式为:Cl-+2OH--2e-=== ClO-+H2O
C. 阴极附近碱性增强,阳极附近碱性减弱
D. 除去CN-的反应:5ClO-+2CN-+2H+ === N2↑+2CO2↑+5Cl-+H2O
【答案】D
【解析】A.根据题意,阳极上产生ClO-,只能是氯离子失电子发生氧化反应生成,需要用不活泼金属或导电的非金属作阳极,可以用较不活泼金属作阴极,所以可以用石墨作阳极、铁作阴极,故A正确;B.阳极上氯离子失电子生成次氯酸根离子和水,所以阳极反应式为Cl-+2OH--2e-═ClO-+H2O,故B正确;C.电解质溶液呈碱性,则阴极上水得电子生成氢气和氢氧根离子,电极反应式为2H2O+2e-═H2↑+2OH-,阴极附近碱性增强,阳极发生Cl-+2OH--2e-═ClO-+H2O,阳极附近碱性减弱,故C正确;D.阳极产生的ClO-将CN-氧化为两种无污染的气体,两种气体为二氧化碳和氮气,该反应在碱性条件下进行,不应该有氢离子参与反应,反应方程式为2CN-+5ClO-+H2O═N2↑+2CO2↑+5Cl-+2OH-,故D错误;故选D。


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】氯气是一种重要的化工原料,能与有机物和无机物进行反应生成多种氯化物。现用下图装置制取氯气并进行一系列的实验探究。
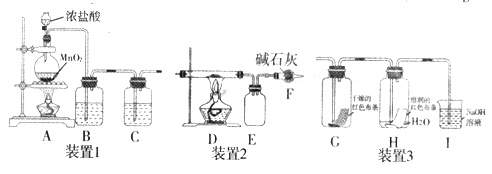
回答下列问题:
(1)装置1是用来制备纯净、干燥的氯气:
①装置A 中圆底烧瓶内发生反应的离子方程式是__________,反应中被氧化的HCl 与消耗的HCl物质的量之比为_______。
②装置B内试剂为__________,装置C的作用是_________。
(2)若将装置1与装置2连接制备少量氯化铁固体(氯化铁易吸水,在300℃时升华),则:
①D中发生反应的化学方程式为______________;
②D、E间导管短且粗的原因是______________;
③若在D装置的硬质玻璃管内装入硅藻土和碳粉,则发生如下反应:
SiO2+2C+2Cl2![]() SiCl4+2CO
SiCl4+2CO
当反应消耗6g碳时,反应转移的电子数为______,F装置之后还应添加一个装置用来_______。
(3)将装置1与装置3连接来探究氯气是否具有漂白性。
①将氯气依次通过盛有干燥红色布条的广口瓶和盛有湿润红色布条的广口瓶,可观察到的现象是________________。
②为防止氯气尾气污染空气,根据氯水显酸性的性质,可用氢氧化钠溶液吸收多余的氯气,原理是(用离子方程式表示___________。根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是_________(填化学式),长期露置于空气中的失效漂白粉,加稀盐酸后产生的气体是________(用字母代号填)。
A.O2 B.H2 C.CO2 D.HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关惰性电极电解AgNO3溶液一段时间后的说法,正确的是( )
A.电解过程中阴极质量不变
B.电解过程中溶液的pH不断升高
C.此时向溶液中加入适量的Ag2O固体可使溶液恢复电解前的状况
D.电解后两极产生的气体体积比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、Q、W、R六种短周期元素原子序数依次增大。化合物甲俗称苛性钠,由X、Z、Q三种元素组成。医学中常用QR溶液配制生理盐水。化合物乙由X、R两种元素组成。请回答下列问题:
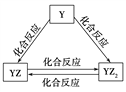
(1)Q的离子结构示意图为__。
(2)Y元素的单质及其化合物能发生如上图所示的转化,则Y元素为___(填元素符号)。在甲溶液中通入足量YZ2气体,写出该反应的离子方程式:______。
(3)W的单质既能与甲溶液反应,又能与乙溶液反应。
①常温下,将W的单质和甲溶液混合,发生反应的离子方程式为_______。
②Q、W两种元素金属性的强弱为Q____W(填“<”或“>”),下列表述中能证明这一事实的是____(填序号)。
a.Q单质的熔点比W单质的低
b.W的原子序数大
c.Q的最高价氧化物的水化物的碱性比W的最高价氧化物的水化物的碱性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器己略去,气密性已检验)。
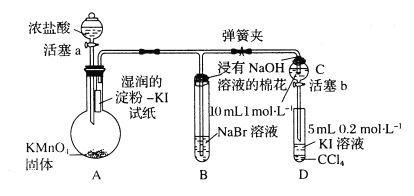
实验过程:
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
II.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
III.当B中溶液由黄色变为红棕色时,关闭活塞a。
IV.……
(1)A中产生黄绿色气体的化学反应方程式是___________。
(2)验证氯气的氧化性强于碘的实验现象是___________。
(3)B中溶液发生反应的离子方程式是___________。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作是___________,现象是___________。
(5)过程III实验的目的是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾在饮用水和工业污水处理领域的消费增长较快。实验室可用软锰矿(主要成分为MnO2)为原料制备高锰酸钾。其部分流程如下:
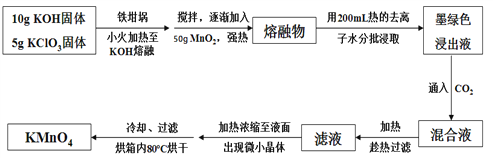
已知:墨绿色浸出液的成分为K2MnO4、KCl溶液
回答下列问题:
(1)实验中采用铁坩埚而不是瓷坩埚的原因是:(用化学反应方程式表示)___________________________________________________。
(2)写出生成K2MnO4和KCl反应的化学方程式:________________________;通入CO2,可使MnO42-发生反应,生成MnO![]() 及MnO2。若通入CO2太多,则在加热浓缩时,会有__________________晶体和KMnO4晶体一起析出。
及MnO2。若通入CO2太多,则在加热浓缩时,会有__________________晶体和KMnO4晶体一起析出。
(3)在加热、浓缩、烘干的过程中温度不宜过高,其原因是(用化学反应方程式表示)_________________________;过滤用到的玻璃仪器有烧杯、_________、_______;加热时用玻璃棒不断搅拌溶液的目的是_______________________________________;洗涤KMnO4晶体用冷水洗涤较好的原因是_______________________________________。
(4)计算12.25 g KClO3固体经过上述转化,最多可制得KMnO4的质量为___________(结果保留一位小数)。(相对原子质量:K—39 Cl—35.5 O—16 Mn—55)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关乙烯有下列叙述: ①乙烯能发生加聚反应
②乙烯溶于水后可得乙醇
③乙烯能与溴水发生加成反应
④可以用高锰酸钾溶液来鉴别乙烯和甲烷
⑤乙烯是无色易溶于水的气体
其中正确的是( )
A.②⑤
B.①③④
C.①②③
D.②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com