
【题目】难溶物氢化亚铜(CuH)可用CuSO4溶液和“另一种反应物”在40℃~50℃时反应生成.CuH不稳定,易分解;CuH在氯气中能燃烧;常温下跟盐酸反应能产生气体,以下有关它的推断中不正确的是()
A.“另一种反应物”一定具有氧化性B.CuH既可做氧化剂也可做还原剂
C.2CuH + 3Cl2![]() 2CuCl2 + 2HCl↑D.CuH+HCl=CuCl↓+H2↑
2CuCl2 + 2HCl↑D.CuH+HCl=CuCl↓+H2↑
科目:高中化学 来源: 题型:
【题目】2一氨-3—氯苯甲酸是白色晶体,其制备流程如下:
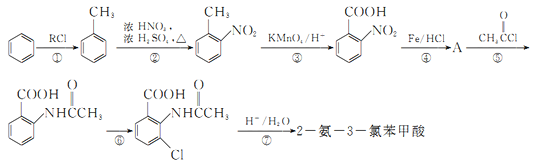
已知: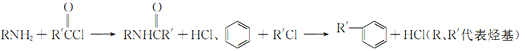
回答下列相关问题
(1)![]() 的名称是__________,2-氨-3-氯苯甲酸中含N官能团的电子式为__________。
的名称是__________,2-氨-3-氯苯甲酸中含N官能团的电子式为__________。
(2)反应①中R代表的是_____________,反应②的反应类型为_____________。
(3)如果反应③中KMnO4的还原产物为MnSO4,请写出该反应的化学方程式_____________。
(4)A的结构简式为_____________,⑥的反应条件为_____________。
(5)符合下列条件的同分异构体的结构简式为_____________。
a.式量比![]() 大42的苯的同系物;
大42的苯的同系物;
b.与酸性KMnO4反应能生成二元羧酸
c.仅有3种等效氢
(6)事实证明上述流程的目标产物的产率很低;据此,研究人员提出将步骤⑥设计为以下三步,产率有了一定提高。
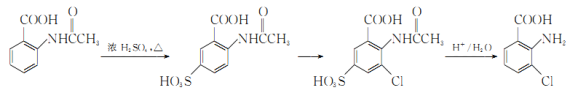
分析产率提高的原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国最近在太阳能光电催化一化学耦合分解硫化氢研究中获得新进展,相关装置如图所示。下列说法正确的是( )

A.该工艺中光能最终转化为化学能
B.该装置工作时,H+由b极区流向a极区
C.a极上发生的电极反应为Fe3++e-=Fe2+
D.a极区需不断补充含Fe3+和Fe2+的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向 20 mL 0.2 mol/LH2A溶液中滴加0. 2 mol/L NaOH溶液.有关微粒的物质的量变化曲线如图所示(其中I代表H2A.,II代表HA—,III表A2—)。根据图示.判断下列说法正确的是

A.当V(NaOH)=20 mL时.溶液中各离子浓度的大小关系为c(Na+)>c(HA—)>c(H+)>c(A2一)>c(OH—)
B.等体积、等物质的量浓度的NaOH溶液与H2 A溶液混合后,其溶液中水的电离程度比纯水中的大
C.NaHA溶液中:c(OH—)+2c(A2—) =c(H+) +c(H2A )
D.将Na2A溶液加水稀释.溶液中所有离子的浓度都减小.但部分离子的物质的量增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A.常温常压下,8 g O2含有4NA个电子
B.1 L 0.1 mol·L-1的氨水中有0.1NA个NH4+
C.标准状况下,22.4 L盐酸含有NA个HCl分子
D.1 mol Na被完全氧化生成Na2O2,失去2NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用乙醚、95%乙醇浸泡杜仲干叶,得到提取液,进步获得绿原酸粗产品的种工艺流程如下,下列说法错误的是
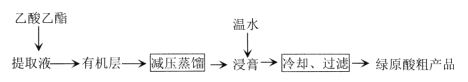
A.常温下,绿原酸易溶于水
B.浸膏的主要成分是绿原酸
C.减压蒸馏的目的是降低蒸馏温度,以免绿原酸变质
D.绿原酸粗产品可以通过重结晶进一步提纯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CoS2催化CO烟气脱硫具有广阔的工业化前景。回答下列问题:
(1)已知:
CoS2(s) +CO(g) ![]() CoS(s) +COS(g) H1
CoS(s) +COS(g) H1
2COS(g) +SO2(g) ![]() 3S(s) +2CO2(g) H2
3S(s) +2CO2(g) H2
S(s) +CoS(S) ![]() CoS2 (s) △H3
CoS2 (s) △H3
则2CO(g)+ SO2(g)![]() 2CO2(g)+S(s) H4=____。 (用H1、 H2、H3表示)
2CO2(g)+S(s) H4=____。 (用H1、 H2、H3表示)
(2)在恒温、恒压的容器中模拟回收硫,加入SO2起始量均为1mol,测得CO2的平衡体积分数随CO和SO2的投料比变化如图:

①当投料比为2时,t min 时测得SO2转化率为50%,则用S的生成速率表示的反应速率v=______g·min-1。
②当投料比为3时,CO2 的平衡体积分数对应的点是______________。
(3)向体积均为1L的恒温、恒客密团容器通入2 mol CO和| mol SO2。反应体系总压强随时间的变化如图:
①相对于I,II改变的外界条件是____________________。
②SO2的平衡转化率为______,平衡常数Kp =________(用平衡分压代替平衡浓度计算)。
(4)利用电解法处理SO2尾气可制备保险粉 (Na2S2O4).电解装置如图,则a____ b (填“>” “=”或“<”),生成S2O42-的电极反应式为____________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是可逆反应A+2B ![]() 2C + 3D 的化学反应速率与化学平衡随外界条件改变而变化的情况,由此推断错误的是
2C + 3D 的化学反应速率与化学平衡随外界条件改变而变化的情况,由此推断错误的是

A.A、B一定是气体
B.C可能是气体
C.D一定不是气体
D.正反应是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图所示,这种有机物可能具有的性质是
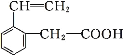
①能使酸性KMnO4溶液或溴水褪色
②能与醇发生酯化反应
③能与NaOH溶液或金属钠反应
④能发生水解反应
⑤能发生加聚反应生成高分子化合物
A. ①②③④⑤ B. ②③④⑤ C. ①③④⑤ D. ①②③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com