
【题目】用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如下图所示,则下列有关说法中不正确的是
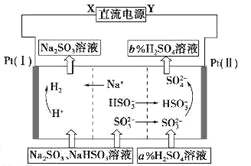
A. X为直流电源的负极,Y为直流电源的正极
B. 阳极区pH增大
C. 图中的b>a
D. 该过程中的产品主要为H2SO4和H2
 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
【题目】在下列溶液中,一定能够大量共存的离子组是( )
A.加入苯酚显紫色的溶液:Na+、Mg2+、Cl﹣、SO![]()
B.加入金属铝能放出大量H2的溶液:NH4+、K+、HCO![]() 、CH3COO﹣
、CH3COO﹣
C.使淀粉碘化钾试纸变蓝的溶液:Cu2+、Ba2+、S2﹣、I﹣
D.加入金属铁能放出大量H2的溶液:Na+、Al3+、ClO﹣、NO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列反应中,HCl作氧化剂的是( )
A.NaOH+HCl=NaCl+H2O
B.Zn+2HCl=ZnCl2+H2↑
C.MnO2+4HCl(浓) ![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
D.CuO+2HCl=CuCl2+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】资料显示:“氨气可在纯氧中安静燃烧…”.某校化学小组学生设计如下装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验.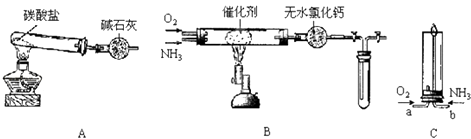
回答下列问题.
(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是;碱石灰的作用是 .
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:①氨催化氧化的化学方程式是;
②试管内气体变为红棕色,该反应的化学方程式是 .
(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气,可观察到氨气安静燃烧,此外无其它明显现象.①两气体通入的先后顺序是 , 其理由是 .
②由实验现象可知,氨气燃烧的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莫尔盐[(NH4)2SO4FeSO46H2O]在空气中比一般亚铁盐稳定,是化学分析中常用的还原剂.某研究性学习小组用如图所示的实验装置来制取莫尔盐,实验步骤如下: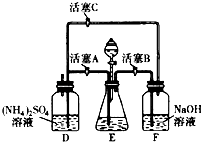
①用30%的NaOH溶液和废铁屑混合、煮沸、冷却、分离,将分离出的NaOH溶液装入F中;
②在E中用①处理过的铁屑和稀H2SO4反应制取FeSO4;
③将②制得的FeSO4溶液与(NH4)2SO4溶液混合,结晶得到莫尔盐.
试回答下列问题:
(1)利用铁屑和稀硫酸反应产生的氢气赶走装置中的氧气及硫酸铵溶液中溶解的氧,其目的是;铁屑和稀硫酸反应产生的氢气的另外一个作用是 .
(2)设计一个简单的实验证明产品中有Fe2+ .
(3)为了确定产品中亚铁离子的含量,研究小组用滴定法来测定.若取产品24.50g配成100mL溶液,取出10mL用0.10molL﹣1KMnO4酸性溶液滴定,消耗KMnO4溶液10.00mL.①试配平反应的离子方程式:
②试求产品中莫尔盐的质量分数(NH4)2SO4FeSO46H2O的相对分子质量为392).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸浸法制取硫酸铜的流程示意图如下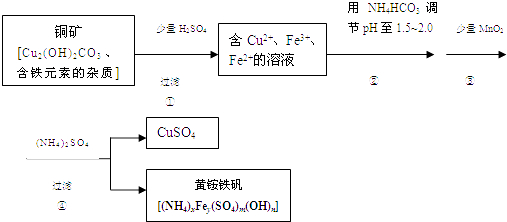
(1)步骤①中Cu2(OH)2CO3 发生反应的化学方程式为 .
(2)在步骤③发生的反应中,1mol MnO2转移2mol 电子,该反应的离子方程式为 .
(3)该小组为测定黄铵铁矾的组成,进行了如下实验:a.称取4.800g样品,加盐酸完全溶解后,配成100.00mL溶液A;
b.量取25.00mL溶液A,加入足量的KI,用0.2500molL﹣1Na2S2O3溶液进行滴定(反应方程式为I2+2Na2S2O3=2NaI+Na2S4O6),消耗30.00mLNa2S2O3溶液至终点.
b.量取25.00mL溶液A,加入足量的NaOH溶液充分反应后,过滤、洗涤、灼烧得红色粉末0.600g.
c.另取25.00mL溶液A,加足量BaCl2溶液充分反应后,过滤、洗涤、干燥得沉淀1.165g.
①用Na2S2O3溶液进行滴定时,滴定到终点的颜色变化为 △ .
②通过计算确定黄铵铁矾的化学式(写出计算过程).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5g 的CO与H2的混合气体和足量的氧气充分反应后,在150℃时将混合气体通过足量的Na2O2固体,则Na2O2固体增加的质量为( )
A.1.5g
B.3g
C.5g
D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子中的中心原子杂化轨道的类型相同的是( )
A. SO3与SO2 B. BF3与NH3 C. BeCl2与SCl2 D. H2O与SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将氯气用导管通入较浓的NaOH和H2O2的混和液中,在导管口与混和液的接触处有闪烁的红光出现.这是因为通气后混和液中产生的ClO﹣被H2O2还原,发生激烈反应,产生能量较高的氧分子,然后立即转变为普通氧分子,多余的能量以红光放出.本实验所用的仪器及导管如图1所示. 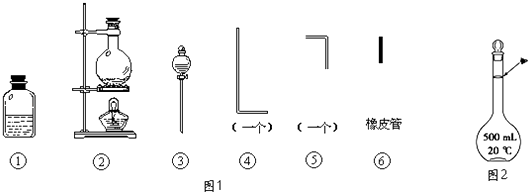
根据要求填写下列空白:
(1)组装氯气发生装置时,应选用的仪器及导管为(填写图中编号).
(2)本实验进行时,按气流方向从左到右的顺序,气体流经的各仪器及导管的编号依次为 .
(3)仪器①的橡皮塞上至少应有2个孔的原因是 .
(4)本实验需配置10molL﹣1的NaOH溶液500mL,用到的仪器除了托盘天平、烧杯外,还须用到的仪器有(填仪器名称),定容时操作如图2,则所配溶液浓度(填“偏高”或“偏低”).
(5)实验时仪器①中ClO﹣与H2O2反应的离子方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com