
【题目】已知物质A~I之间的转化关系符合下图所示.其中A、C、F、G、I为常见固体且焰色反应均为黄色;A为海水中主要溶质,B为常温下常见液体;E为黄绿色气体,H是无色无味且能使澄清石灰水变浑浊的气体.
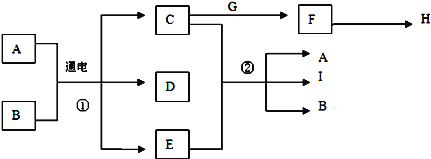
试回答下列问题:
(1)D的化学式为__________。
(2)反应①的化学方程式为:____________________________。
(3)反应②的离子方程式为:____________________________。
(4)写出镁条在H气体中燃烧的反应方程式为:___________________________。
(5)G在水中的电离方程式_____________________________。
(6)在A、I和B的混合物中加入稀硫酸,有黄绿色气体产生,写出该反应的化学方程式_____。
【答案】H2 2NaCl+ 2H2O ![]() H2↑ + Cl2↑ + 2NaOH Cl2 + 2OH- == Cl- + ClO- + H2O 2Mg +CO2
H2↑ + Cl2↑ + 2NaOH Cl2 + 2OH- == Cl- + ClO- + H2O 2Mg +CO2![]() 2MgO+C NaHCO3 = Na+ +HCO3- NaCl+NaClO+H2SO4== Cl2↑+ Na2SO4+ H2O
2MgO+C NaHCO3 = Na+ +HCO3- NaCl+NaClO+H2SO4== Cl2↑+ Na2SO4+ H2O
【解析】
A、C、F、G、I为常见固体且焰色反应均为黄色,说明均有钠元素,A为海水中主要溶质,则A为NaCl,B为常温下常见液体,则B为H2O;E为黄绿色气体,则E为Cl2,H是无色无味且能使澄清石灰水变浑浊的气体,则H为CO2,根据题中各物质转化关系,电解食盐水得C、D、E,C中含有钠元素,则C为NaOH,则D为H2,C与E反应生成A、I、B,则I为NaClO,C、F、G均含有钠元素,F能产生二氧化碳,则G为NaHCO3,F为Na2CO3。(1)D的化学式为H2;(2)反应①的化学方程式为:2NaCl+ 2H2O ![]() H2↑ + Cl2↑ + 2NaOH;(3)反应②的离子方程式为:Cl2 + 2OH- == Cl- + ClO- + H2O;(4)镁条在CO2气体中燃烧的反应方程式为:2Mg +CO2
H2↑ + Cl2↑ + 2NaOH;(3)反应②的离子方程式为:Cl2 + 2OH- == Cl- + ClO- + H2O;(4)镁条在CO2气体中燃烧的反应方程式为:2Mg +CO2![]() 2MgO+C;(5)G为NaHCO3,在水中的电离方程式为:NaHCO3 = Na+ +HCO3-;(6)在A、I和B的混合物中加入稀硫酸,有黄绿色气体产生,反应的化学方程式为:NaCl+NaClO+H2SO4== Cl2↑+ Na2SO4+ H2O。
2MgO+C;(5)G为NaHCO3,在水中的电离方程式为:NaHCO3 = Na+ +HCO3-;(6)在A、I和B的混合物中加入稀硫酸,有黄绿色气体产生,反应的化学方程式为:NaCl+NaClO+H2SO4== Cl2↑+ Na2SO4+ H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下图表示细胞中四种有机化合物的组成及主要功能。回答下列问题:
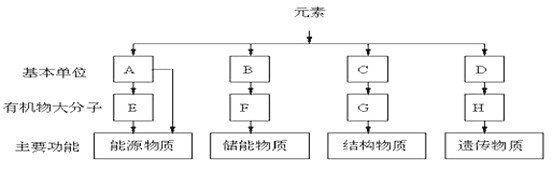
(1)图中的基本单位A是_________。利用A合成的E主要分布在人和动物的_________中,当人和动物血液中的A低于正常含量时,一些细胞中的E便分解产生A及时补充。
(2)与图中的E相比,F是细胞内更良好的储能物质,原因是其分子中氧的含量________,而氢的含量_________。分布在内脏器官周围的F还具有_________的作用,可以保护内脏器官。
(3)图中的C在生物体中约有20种,其中有一部分在人体细胞不能合成,必须从外界环境中直接获取,这部分C叫做_________。由C通过__________的方式结合在一起形成G,C分子之间通过_________(用化学结构简式表示)连接。
(4)图中H的中文名称是_________,烟草叶肉细胞的H彻底水解的产物是___________________________________________________________。
(5)上述生物大分子都以____________为骨架。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂用提取粗盐后的盐卤(主要成分为MgCl2)制备金属镁,其工艺流程如下,下列说法中,错误的是( )
![]()
A. 操作①发生的反应为非氧化还原反应
B. 若在实验室进行操作①只需要漏斗和烧杯两种玻璃仪器
C. 操作②是蒸发浓缩结晶
D. 在整个制备过程中,未发生置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)配平下列离子方程式:______
Ce3++ H2O2+ H2O === Ce(OH)4↓+_______H+
(2)已知某待测液由Ag+、Mg2+、K+、Ba2+、NH4+、NO3-中的若干种离子组成,进行如下实验:
第一步:加入过量的稀盐酸,有白色沉淀生成。
第二步:过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成。
第三步:再过滤,取少量滤液,逐渐滴入NaOH溶液至溶液呈碱性,在此过程中没有沉淀和气体产生,加热该溶液,可产生使湿润的红色石蕊试纸变蓝色的气体。
根据实验现象回答:
①写出第三步加热该溶液后,有气体生成的反应的离子方程式:_________________;
②待测液中一定含有_______和NO3-离子,一定不含有_________离子,还有一种离子不能确定其是否存在,要检验这种离子的实验方法是(填写实验名称)___________。
③往含等物质的量CO32-和HCO3-的溶液中滴入HCl溶液,下列表示产生的气体在标准状况下的体积与加入的HCl溶液体积关系图正确的是_________。
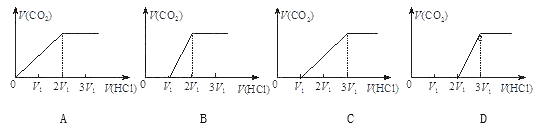
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】aLCO2气体通过足量Na2O2后,所得气体再与bLNO混合时,可得到cL气体(气体体积均在相同状况下测定),下列表达式中,错误的是( )
A. 若a则c<![]() (a+b) B. 若a则c>
(a+b) B. 若a则c>![]() (a+b)
(a+b)
C. 若a>b则c=![]() (a+b) D. 若a=b则c=
(a+b) D. 若a=b则c=![]() (a+b)
(a+b)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子或离子中中心原子价层电子对几何构型为四面体且分子或离子空间构型为V形的是( )
A. NH B. PH3 C. OF2 D. H3O+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、有一瓶澄清的溶液,其中可能含有H+、NH4+、Mg2+、Ba2+、Al3+、I﹣、NO3﹣、CO32﹣、SO42﹣、AlO2﹣,取该溶液进行以下实验:
(1)取pH试纸检验,溶液呈酸性,可以排除______________的存在.
(2)取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4呈紫红色,可以排除_______存在.
(3)另取出部分溶液逐渐加入NaOH溶液,使溶液从酸性逐渐变为碱性,反应过程中均无沉淀产生,则又可排除____________的存在.
(4)取出部分上述碱性溶液加Na2CO3溶液后,有白色沉淀生成,证明有_______的存在,又可以排除__________的存在.
(5)根据上述实验事实可以确定,该溶液中肯定存在的离子是____________,还不能确定是否存在的离子是_______________.
Ⅱ、某混合物 A,含有 KAl(SO4)2、Al2O3 和 Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
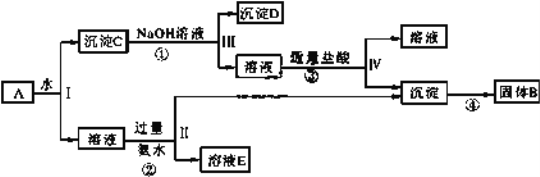
据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是__________。
(2)根据上述框图反应关系,写出下列B、C、D 所含物质的化学式(提示:可为混合物)。
固体 B_________;沉淀 C__________;沉淀 D _________;
(3)写出①、②反应离子方程式。
①___________________________________________;
②___________________________________________;
(4)步骤③较难操作,如何将实验方案进行改进?________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com