
【题目】(1)配平下列离子方程式:______
Ce3++ H2O2+ H2O === Ce(OH)4↓+_______H+
(2)已知某待测液由Ag+、Mg2+、K+、Ba2+、NH4+、NO3-中的若干种离子组成,进行如下实验:
第一步:加入过量的稀盐酸,有白色沉淀生成。
第二步:过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成。
第三步:再过滤,取少量滤液,逐渐滴入NaOH溶液至溶液呈碱性,在此过程中没有沉淀和气体产生,加热该溶液,可产生使湿润的红色石蕊试纸变蓝色的气体。
根据实验现象回答:
①写出第三步加热该溶液后,有气体生成的反应的离子方程式:_________________;
②待测液中一定含有_______和NO3-离子,一定不含有_________离子,还有一种离子不能确定其是否存在,要检验这种离子的实验方法是(填写实验名称)___________。
③往含等物质的量CO32-和HCO3-的溶液中滴入HCl溶液,下列表示产生的气体在标准状况下的体积与加入的HCl溶液体积关系图正确的是_________。
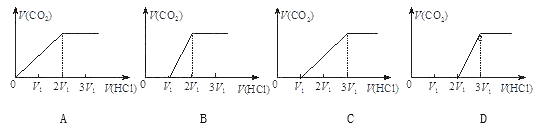
【答案】2,1,6==2,6 NH4++OH-![]() NH3↑+H2O Ag+、Ba2+、NH4+ Mg2+ 焰色反应 C
NH3↑+H2O Ag+、Ba2+、NH4+ Mg2+ 焰色反应 C
【解析】
(1)反应中Ce3+中Ce元素由+3价变为+4价,升高1,H2O2中氧元素由-1价降为-2价,降低1×2,最小公倍数为2,Ce3+、Ce(OH)4配2,H2O2配1,再结合质量守恒和电荷守恒配平得反应:2Ce3++H2O2+6H2O = 2Ce(OH)4↓+6H+,故答案为:2,1,6==2,6;(2)第一步:加入过量的稀盐酸,有白色沉淀生成,沉淀为AgCl,则一定含有Ag+;第二步:过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成,沉淀为硫酸钡,则一定含有Ba2+;第三步:再过滤,取少量滤液,滴入NaOH溶液至溶液呈碱性,在此过程中溶液无明显现象,加热该溶液,可产生使湿润的红色石蕊试纸变蓝色的气体,气体为氨气,说明一定含NH4+,一定没有Mg2+,①第三步加热该溶液后,有气体生成的反应的离子方程式为:NH4++OH-![]() NH3↑+H2O;②由上述分析可知,一定含有的阳离子为Ag+、Ba2+、NH4+,一定不含Mg2+,钾离子不能确定,可利用焰色反应来检验,方法为透过蓝色钴玻璃看是否呈紫色,呈紫色说明有K+,不呈紫色说明无K+;③由于CO32-与酸的反应是分步进行的:CO32-+H+=HCO3-、HCO3-+H+=H2O+CO2↑,开始是HCO3-离子不参加反应,只有CO32-反应,所以开始时没有二氧化碳气体生成,当CO32-完全生成HCO3-后,生成的HCO3-和原溶液中的HCO3-一起反应生成二氧化碳气体,反应前CO32-和HCO3-物质的量相等,设为nmol,则CO32-生成HCO3-消耗的氯化氢的物质的量为nmol,同时生成nmolHCO3-,溶液中此时总共含有2nmolHCO3-,完全反应生成二氧化碳,需要消耗氯化氢2nmol,即没有生成二氧化碳消耗盐酸的体积是生成二氧化碳消耗盐酸体积的一半,只有C符合,答案选C。
NH3↑+H2O;②由上述分析可知,一定含有的阳离子为Ag+、Ba2+、NH4+,一定不含Mg2+,钾离子不能确定,可利用焰色反应来检验,方法为透过蓝色钴玻璃看是否呈紫色,呈紫色说明有K+,不呈紫色说明无K+;③由于CO32-与酸的反应是分步进行的:CO32-+H+=HCO3-、HCO3-+H+=H2O+CO2↑,开始是HCO3-离子不参加反应,只有CO32-反应,所以开始时没有二氧化碳气体生成,当CO32-完全生成HCO3-后,生成的HCO3-和原溶液中的HCO3-一起反应生成二氧化碳气体,反应前CO32-和HCO3-物质的量相等,设为nmol,则CO32-生成HCO3-消耗的氯化氢的物质的量为nmol,同时生成nmolHCO3-,溶液中此时总共含有2nmolHCO3-,完全反应生成二氧化碳,需要消耗氯化氢2nmol,即没有生成二氧化碳消耗盐酸的体积是生成二氧化碳消耗盐酸体积的一半,只有C符合,答案选C。


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】常温下,下列不发生反应的一组物质是( ) ①铜与浓硫酸 ②二氧化硅与NaOH溶液 ③铜与浓硝酸 ④石英与纯碱 ⑤铁与液氧 ⑥一氧化氮与氧气 ⑦硅与氧气.
A.①②③⑥
B.②③⑤⑥
C.①④⑤⑦
D.①②③⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的NaHCO3分为三等份,第一份直接加入盐酸中,消耗盐酸物质的量为n1,第二份首先加热,使其完全分解后,再加入盐酸中,消耗盐酸物质的量为n2,第三份首先加热,使其部分分解后,再加入盐酸中,消耗盐酸物质的量为n3,假若与盐酸都完全反应,则n1、n2、n3的大小关系正确的是( )
A. n1=n2=n3 B. n2>n1>n3 C. n1>n2>n3 D. n1>n3>n2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知物质A~I之间的转化关系符合下图所示.其中A、C、F、G、I为常见固体且焰色反应均为黄色;A为海水中主要溶质,B为常温下常见液体;E为黄绿色气体,H是无色无味且能使澄清石灰水变浑浊的气体.
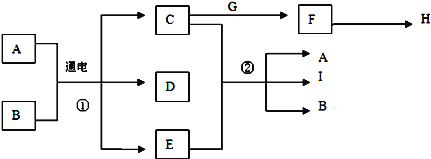
试回答下列问题:
(1)D的化学式为__________。
(2)反应①的化学方程式为:____________________________。
(3)反应②的离子方程式为:____________________________。
(4)写出镁条在H气体中燃烧的反应方程式为:___________________________。
(5)G在水中的电离方程式_____________________________。
(6)在A、I和B的混合物中加入稀硫酸,有黄绿色气体产生,写出该反应的化学方程式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应3S+6KOH ![]() 2K2S+K2SO3+3H2O,下列说法正确的是
2K2S+K2SO3+3H2O,下列说法正确的是
A. S是氧化剂,KOH是还原剂 B. 若3mol硫完全反应,则反应中共转移了4mol电子 C. 还原剂与氧化剂的质量比是2:1 D. 氧化产物和还原产物的物质的量之比为3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是一种重要金属:
(1)生产中曾用铝热反应焊接钢轨,则铝与氧化铁发生反应的化学方程式为: ___________ 。
(2)铝还用于冶炼熔点较高的金属如钒、铬、锰等,请配平下列用铝冶炼金属钒的化学反应方程式: V2O5 + Al ==== Al2O3 + V_____________
该反应中氧化剂是_____________ ,要得到1mol金属钒,需要纯铝的质量__________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com