
| A、0.1mol?L-1 |
| B、0.01mol?L-1 |
| C、0.2mol?L-1 |
| D、0.02mol?L-1 |
| KW |
| C(H+) |
| 10-14 |
| 10-11 |


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:
| A、CH3CH(OH)CH3 |
| B、CH2(OH)CH(OH)CH3 |
| C、CH3CH2CH2OH |
| D、CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.01mol/L |
| B、0.02mol/L |
| C、0.03mol/L |
| D、0.04mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、90ml | B、150ml |
| C、175ml | D、200ml |
查看答案和解析>>
科目:高中化学 来源: 题型:
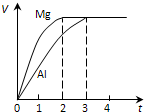 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图.关于反应中镁和铝的说法正确的是( )
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图.关于反应中镁和铝的说法正确的是( )| A、质量之比为3:2 |
| B、物质的量之比为2:3 |
| C、摩尔质量之比为2:3 |
| D、消耗硫酸的物质的量之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol S在足量O2中燃烧,转移的电子数为6 NA |
| B、标况下,22.4L氦气含有的原子数为2NA |
| C、28 g C2H4中含有2 NA个碳原子 |
| D、0.1 mol?L-1的碳酸氢钠溶液中含钠离子数为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com