
����Ŀ�������е�NO����O3Ԥ����������CaSO3����Һ����ȥ����Ԥ����ʱ������Ӧ��NO(g)��O3(g)![]() NO2(g)��O2(g)����ã�v����k��c(NO)��c(O3)��v����k��c(NO2)��c(O2)��k����k��Ϊ���ʳ��������¶�Ӱ�졣���ݻ���Ϊ2L�ļס��������ܱ������г���һ������NO��O3�����NO�����������ʱ��ı仯��ͼ��ʾ������˵����ȷ����(����)
NO2(g)��O2(g)����ã�v����k��c(NO)��c(O3)��v����k��c(NO2)��c(O2)��k����k��Ϊ���ʳ��������¶�Ӱ�졣���ݻ���Ϊ2L�ļס��������ܱ������г���һ������NO��O3�����NO�����������ʱ��ı仯��ͼ��ʾ������˵����ȷ����(����)
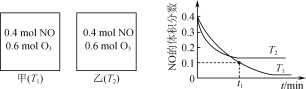
A.�������������������NO��ƽ��ת����
B.T1ʱ����Ӧ��t1min�ڵ�ƽ������v(O2)��![]() mol��L��1��min��1
mol��L��1��min��1
C.T1ʱ��NO(g)��O3(g)![]() NO2(g)��O2(g)��k����3k��
NO2(g)��O2(g)��k����3k��
D.T2ʱ����2L�ܱ������г���0.6molNO��0.4molO3������ƽ��ʱc(NO2)С����������ƽ��ʱc(NO2)
���𰸡�BC
��������
T2�¶����ȴﵽ��ѧƽ�⣬��T1��T2������ƽ��ʱ��T2�¶���NO�������������T1�¶���NO�����������˵�������¶ȣ�ƽ�������ƶ����ʸ÷�Ӧ������ӦΪ���ȷ�Ӧ��
A����Ϸ�����֪�������¶ȣ�ƽ�������ƶ���NO��ƽ��ת���ʼ�С��A����
B���ɷ�Ӧ����ʽ��֪����Ӧǰ����ϵ������������ʵ������䣬��t1ʱ��NO��С�����ʵ���=0.4mol-0.1��1mol=0.3mol������v(NO)=![]() =
=![]() mol��L��1��min��1��v(O2)=v(NO)=
mol��L��1��min��1��v(O2)=v(NO)=![]() mol��L��1��min��1��B��ȷ��
mol��L��1��min��1��B��ȷ��
C���ɷ�Ӧ����ʽ��֪����Ӧǰ����ϵ������������ʵ������䣬��ô������t1ʱ��NO��С�����ʵ���=0.4mol-0.1��1mol=0.3mol��������ʽ��

��ͼ��֪��t1ʱ��ƽ��������У�v����v������k��c(NO)��c(O3)��k��(NO2)��c(O2)��![]() ��
��![]() ��
��![]() =
=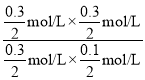 =3������
=3������![]() >3��C��ȷ��
>3��C��ȷ��
D����ƽ��ʱ��������c(NO2)=a�����ݷ���ʽ��֪c(O2)=a��c(NO)=(0.4-a)mol/L��c(O3)=(0.6-a)mol/L������ƽ�ⳣ��K=![]() �������0.6molNO��0.4molO3����ƽ��ʱc(NO2)=b����c(O2)=b��c(NO)=(0.6-b)mol/L��c(O3)=(0.4-b)mol/L��ƽ�ⳣ��K=
�������0.6molNO��0.4molO3����ƽ��ʱc(NO2)=b����c(O2)=b��c(NO)=(0.6-b)mol/L��c(O3)=(0.4-b)mol/L��ƽ�ⳣ��K=![]() ���¶Ȳ��䣬ƽ�ⳣ�����䣬����
���¶Ȳ��䣬ƽ�ⳣ�����䣬����![]() =
=![]() ������a=b�������������c(NO2)��ȣ�D����
������a=b�������������c(NO2)��ȣ�D����
��ѡBC��


 ��1����Ԫ�¿�������ĩϵ�д�
��1����Ԫ�¿�������ĩϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС��ͬѧ������ͼ��ʾװ��̽������������������ʡ�
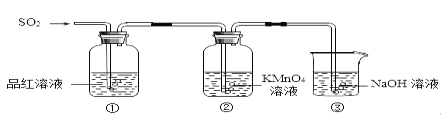
��ش�
(1)ʵ������ͭ��Ũ���Ṳ����ȡ��������Ӧ�Ļ�ѧ����ʽ��_________��
(2)���۲쵽������Һ��ɫ��dzʱ�����е�������_________��
(3)װ�â۵�������________��
(4)�١����е�����˵������������е�������_________��
(5)�����漰�Ļ�ѧ��Ӧ����ʽ��_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������������װ����ȡ�Ȼ�����ĩ����֪�Ȼ�����ĩ��������ˮ���ɽᾧ������FeCl3��6H2O = FeCl3��6H2O
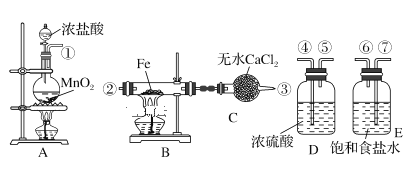
��1�������������������˳����������Ӧ��(�������ӿ�˳���ӿ���ż�������������)������_____��
��2����ƿA�з�Ӧ�����ӷ���ʽΪ________�����У���������________(����������)��
��3��B�з�Ӧ�Ļ�ѧ����ʽ��_____________��
��4��װ��C��������_______________��
��5��A��B�еľƾ���Ӧ�ȵ�ȼ____��(����A������B��)�ľƾ��ƣ�������__________��
��6��С��ͬѧ��Ϊ����ʵ��װ�ò����������벹��________װ�á�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ָ����Ӧ�����ӷ���ʽ��ȷ���ǣ�������
A.Na��ˮ��Ӧ��Na��2H2O=Na����2OH����H2��
B.��NaOH��Һ����NO2��2NO2��Na����2OH��=NaNO3��NO2-��H2O
C.��MnO2��Ũ���ᷴӦ�Ʊ�Cl2��MnO2��4H����2Cl��![]() Mn2����Cl2����2H2O
Mn2����Cl2����2H2O
D.NaHCO3��Һ�м�����Ba��OH��2��Һ��2HCO3-��Ba2����2OH��=BaCO3����CO32-��2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��N2H4��N2O4���������������ƽ������ƽ���������Ӧ��2N2H4��l����N2O4��l��=3N2��g����4H2O��g���������й�˵����ȷ���ǣ�������
A.��Ӧÿ����0.3 mol N2��ת�Ƶ��ӵ���ĿΪ1.6��6.02��1023
B.����N2O4���ܱ������д��ڣ�N2O4��g��![]() 2NO2��g������c��N2O4����c��NO2����1��2ʱ���ÿ��淴Ӧ������
2NO2��g������c��N2O4����c��NO2����1��2ʱ���ÿ��淴Ӧ������
C.����N2H4������ȼ�ϵ�ع���ʱ�������缫��ӦʽΪO2��2H2O��4e��=4OH��
D.N2H4��ˮ��Һ�д��ڣ�N2H4��H2O![]() N2H
N2H![]() ��OH������ϡ��Һ�м�ˮϡ�ͣ�
��OH������ϡ��Һ�м�ˮϡ�ͣ� ![]() ��ֵ���
��ֵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25�桢101kPaʱ������������ת��ͼ������˵������ȷ������ ��
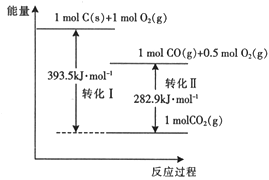
A. ת�������Ȼ�ѧ����ʽ2CO(g)+O2(g)=2CO2(g) ��H=-282.9 kJ��mol-1
B. ��ͬ������,1mol C(s )��0.5 mol O2(g)����������1mol CO(g)������
C. ��C��CO ���Ȼ�ѧ����ʽ2C(s)+O2(g)=2CO(g) ��H=-221.2 kJ��mol-1
D. CO2(g)�ֽ�ΪC(s)��O2(g)�����ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.��Ҫ��д�����з�Ӧ�ķ���ʽ
��1��������������������Һ��Ӧ�����ӷ���ʽ ______
��2������������ˮ��Ӧ�Ļ�ѧ����ʽ ____
��3�� ʵ�������������������ӷ���ʽ ________
��. �벹����������ƽ����ʽ���õ����ű������ת�Ʒ������Ŀ
��1��KI+KIO3+H2SO4�TI2+K2SO4+H2O��________________________
��2��MnO4-+NO2-+���������TMn2++NO3-+H2O��_________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Na2SO3��һ�ְ�ɫ��ĩ����ҵ�Ͽ�������ԭ�����������ȡ�ij��ѧС��̽����ͬpH��Na2SO3��Һ��ͬŨ��AgNO3��Һ��Ӧ�IJ����������ʵ�顣
I.��1������500mLһ��Ũ�ȵ�Na2SO3��Һ
���ܽ⣺ȷ��ȡһ��������Na2SO3���壬����е�����ˮ�ܽ⡣����ˮ����е�ԭ����___��
����Һ���������ܽ���Na2SO3��Һ���ձ�����ȴ��ת������A�У�������AΪ_��ͬʱϴ��___(����������)2~3�Σ���ϴ��Һһ��ת������A�У�
�۶��ݣ���ˮ���̶���1~2cm�������ý�ͷ�ιܵμ�����ˮ��Һ����̶������У��Ǻ�ƿ�����������µߵ���ҡ�ȡ�
��.̽����ͬpH��Na2SO3��Һ��pH=4��AgNO3��Һ��Ӧ�IJ���
�������ϣ�i.Ag2SO3Ϊ��ɫ���壬������ˮ�����ڹ���Na2SO3��Һ
ii.Ag2O���غ�ɫ���壬������ˮ������Ũ��ˮ��Ӧ
��2����pH=8��Na2SO3��Һ����pH=4��AgNO3��Һ�У���������ɫ������
����һ���ð�ɫ����ΪAg2SO3
��������ð�ɫ����ΪAg2SO4
���������ð�ɫ����ΪAg2SO3��Ag2SO4�Ļ����
��д������һ�����ӷ���ʽ__��
�����������Ŀ���������___��
����֤�������Ƿ������ʵ�������__��
��3����pH=4��AgNO3��Һ��ε���������pH=11��Na2SO3��Һ�У���ʼ������ɫ����A��Ȼ�����غ�ɫ���ʡ�Ϊ���о���ɫ����A�ijɷ֣�ȡ�غ�ɫ�����������ʵ�飺

����֪��Ӧ(b)�Ļ�ѧ����ʽΪAg(NH3)2OH+3HCl=AgCl��+2NH4Cl+H2O����Ӧ(a)�Ļ�ѧ����ʽΪ___��
�����ɰ�ɫ����A�ķ�ӦΪ��������ԭ��Ӧ����A����Ҫ�ɷ���__(д��ѧʽ)��
��4��������ʵ���֪������Һ��ķ�Ӧ���ڶ����ԡ�����֤����2����ʵ�����һ��������3����ʵ��IJ��ﲻͬ�ڣ�2��ʵ���������__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݷ�Ӧ��2Na2CO3+SnO2+4S![]() Na2SO4+Na2SnS3+2CO2���ش��������⣺
Na2SO4+Na2SnS3+2CO2���ش��������⣺
��1��������Ӧ�漰��Ԫ���У��ǽ�������ǿ��Ԫ�����������Ų�ʽΪ_____��
��������Ӧ���������У����ڷ��Ӿ���Ļ�����ĽṹʽΪ_____��
��2����������Ӧ�е������ʵ�ԭ�Ӻ����_____�ֲ�ͬ�˶�״̬�ĵ��ӣ���_____�ֲ�ͬ�����ĵ��ӡ�
��3��������Ӧ�У���������ǿ��Ԫ������Ԫ����Ƚϣ�������Ϊ�ж����߽�����ǿ�����ݵ���_____��ѡ���ţ���
a���ܷ��û�������ͭ��Һ�е�ͭ����
b��Al(OH)3�ܷ��ܽ��ڸ�Ԫ������������Ӧ��ˮ������
c����������������ʱʧȥ������Ŀ�Ķ���
d��������ͬŨ�ȵ�ϡ���ᷢ����Ӧ�ľ��ҳ̶�
��4��������Ӧ���������뻹ԭ�������ʵ���֮����_____��
��5�������£����Na2SnS3��ҺpH��7���������ӷ���ʽ������ԭ��_____
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com