
����Ŀ�����н�������A��B������ס��ҡ����Լ�����C��D��E��F������֮���ܷ������·�Ӧ��(ͼ����Щ��Ӧ�IJ���ͷ�Ӧ����û�б��)
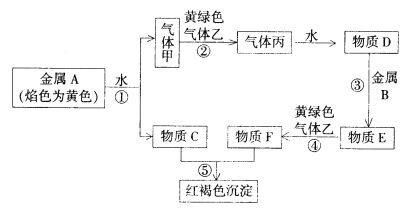
(1)A��ԭ�ӽṹʾ��ͼΪ_____________�����Ļ�ѧʽΪ_____________��
(2)����A��B������ס��ҡ����Լ�����C��D��E��F�в��ܵ������__________________ �����ڵ���ʵ���___________ ��(����A����B����������������������C����D����E����F��)
(3)д��ת���ٷ����Ļ�ѧ����ʽ��____________________,д��ת���ܷ��������ӷ���ʽ��____________________��
(4)��Na2O2Ͷ�뵽E��Һ�У����Թ۲쵽�������ǣ�_____________��
���𰸡�![]() HCl �ס��ҡ��� �� 2Na+2H2O=2NaOH+H2�� Cl2+2Fe2+=2Cl-+2Fe3+ �������ɫ������ͬʱ������ɫ����
HCl �ס��ҡ��� �� 2Na+2H2O=2NaOH+H2�� Cl2+2Fe2+=2Cl-+2Fe3+ �������ɫ������ͬʱ������ɫ����
��������
����A��ɫ��ӦΪ��ɫ����AΪ����Na���ɷ�Ӧ�ٿ�֪��CΪNaOH��Һ�������ΪH2������ɫ������ΪCl2����������Ӧ���ɱ�HCl��HCl����ˮ������DΪ���ᣬ���������B��Ӧ��������E������E��Cl2��Ӧ��������F��F��NaOH��Ӧ���ɺ��ɫ����ΪFe(OH)3��������F�к���Fe3+��������֪����BΪFe������EΪFeCl2��Һ������FΪFeCl3��Һ��
��1������A��ɫ��ӦΪ��ɫ����AΪ����Na��ԭ�ӽṹʾ��ͼΪ![]() ������ɫ������ΪCl2����������Ӧ���ɱ�ΪHCl���ʴ�Ϊ��
������ɫ������ΪCl2����������Ӧ���ɱ�ΪHCl���ʴ�Ϊ�� ![]() ��HCl��
��HCl��
��2��A��Na��B��Fe��C��NaOH��Һ��D�����ᡢE��FeCl2��Һ�� F��FeCl3��Һ���ף�H2����: Cl2����: HCl�����в��ܵ�����У��ס��ҡ��������ڵ���ʣ������ʴ�Ϊ���ס��ҡ���������
��3��ת����Ϊ����Na��ˮ�ķ�Ӧ�������ƺ���������Ӧ�Ļ�ѧ����ʽΪ��2Na+2H2O=2NaOH+H2����ת����ΪFeCl2��Cl2�ķ�Ӧ�����Ȼ�������Ӧ�����ӷ���ʽΪ��Cl2+2Fe2+=2Cl-+2Fe3+���ʴ�Ϊ��2Na+2H2O=2NaOH+H2����Cl2+2Fe2+=2Cl-+2Fe3+��
��4��EΪFeCl2����Na2O2Ͷ�뵽FeCl2��Һ�У�Na2O2����ǿ�����ԣ����������������������ӣ��������ɫ������ͬʱ������ɫ�����������ʴ�Ϊ���������ɫ������ͬʱ������ɫ���塣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Dz��ֶ�����Ԫ�صĵ��ʼ��仯����(������Һ)��ת����ϵ����֪�ڳ��³�ѹ�£�A�ǹ��壬B��C��D��E�Ƿǽ��������Ҷ������壬C�ʻ���ɫ��������F�ǵ���ɫ���壬������G����ɫ��ӦΪ��ɫ����������Jͨ��״���³���̬��D��E��Ӧ����һ�ִ̼�����ζ�����塣
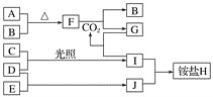
��ش��������⣺
(1)E��J�Ļ�ѧʽ�ֱ���________��________��
(2)д��F��CO2��Ӧ�Ļ�ѧ����ʽ���õ����ŷ���ʾ����ת�Ƶ������_________��
(3)����������Cͨ��ʢ�е��۵⻯����Һ���Թ��У���Һ����ɫ���÷�Ӧ�����ӷ���ʽΪ_________��
(4)�����3.36 L����B��A��ȫ��Ӧ��ת�Ƶ��ӵ���ĿΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ų������ı���[��Ҫ��BaCO3��BaSO3��Ba��FeO2��2��]��ij��Ҫ����BaCl2��BaCO3��BaSO4�Ļ����������ñ�����ȡBa��NO3��2���䲿�ֹ���������ͼ��
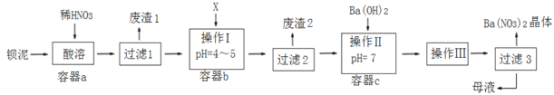
��֪����Fe��OH��3��Fe��OH��2��ȫ����ʱ����Һ��pH�ֱ�Ϊ3.2��9.7
��Ba��NO3��2����ˮ���ܽ�Ƚϴ�����ˮ���ܽ�Ƚ�С
�����й�˵������ȷ���ǣ� ��
A. ����2����Һ�к������ᣬ������������������к͵õ����ᱵ��Һ
B. X�Լ�Ӧѡ������H2O2��Ŀ����Ϊ��ʹ��Һ�е�Fe2+ת��ΪFe3+������ת��ΪFe��OH��3����
C. �����������ᾧ����ȴ�ᾧ
D. �˹��������������̻��е��������������ɴ�����Ⱦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£��� 20mL��c mol��L-1ij�� HR ��Һ�еμ� 0.1000mol��L-1����������Һ����Һ�� pH ������������Һ��� V��NaOH��֮���ϵ��ͼ��ʾ������˵��һ������ȷ���ǣ� ��
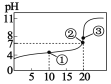
A.c��0.1
B.HR �ĵ��뷽��ʽΪ HR H+ +R-
C.�ٵ��Ӧ��Һ�д��� c��R-����c��Na+����c��H+����c��OH-��
D.�ڢ٢ڢ۵��Ӧ����Һ�ж����� c��OH-����c��H+����c��HR��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��һ�����������ʵ�ʵ��װ�á���װ���л���ͨ������X�����رջ���K����Ʒ����Һ�ޱ仯��������ʯ��ˮ����ǣ�������K����Ʒ����Һ��ɫ���ݴ��ж�����X��ϴ��ƿ��Һ��Y(����)������(����)
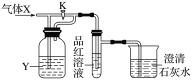
ѡ�� | A | B | C | D |
X | CO | SO2 | CO2 | Cl2 |
Y | ŨH2SO4 | NaHCO3������Һ | Na2SO3��Һ | NaHSO3������Һ |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�ķ��ӿ�����죬��ѧ��ChrisScotton���÷����������ȡ��ΪPenguinone�� �����й�Penguinone��˵������ȷ����
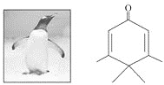
A.Penguinone�д������ֹ�����
B.Penguinone��һ�ַ���ͪ
C.Penguinone�д�������ϩ��ͬ�Ĺ����ţ�����������ϩ�����Ƶ�����
D.����÷����е�˫�����ܼӳɣ���1molPenguinone����3mol������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�����, ����˵����ȷ���ǣ� ��
A.18g ˮ�����еĵ�����ĿΪNA
B.2g ��������ԭ����ΪNA
C.����������ˮ��Ӧ���ɱ����11.2L��������ת�Ƶ���ĿΪNA
D.200 mL0.5mol/LNa2SO4��Һ����Na+��Ŀ0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���ܱ������з������·�Ӧ��2SO2(g) + O2(g) ![]() 2SO3(g)����Ӧ������ijһʱ�̲��SO2��O2��SO3��Ũ�ȷֱ�Ϊ��0.2 mol��L��1��0.2 mol��L��1��0.2 mol��L��1������Ӧ�ﵽƽ��ʱ�����ܳ��ֵ�������(����)
2SO3(g)����Ӧ������ijһʱ�̲��SO2��O2��SO3��Ũ�ȷֱ�Ϊ��0.2 mol��L��1��0.2 mol��L��1��0.2 mol��L��1������Ӧ�ﵽƽ��ʱ�����ܳ��ֵ�������(����)
A. c(SO3)��0.4 mol��L��1B. c(SO2)��c(SO3)��0.15 mol��L��1
C. c(SO2)��0.25 mol��L��1D. c(SO2) + c(SO3)��0.5 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±��Ǽ������᳣���µĵ���ƽ�ⳣ����
CH3COOH | H2CO3 | H2S | H3PO4 |
1.8��10-5 | K1=4.3��10-7 K2=5.6��10-11 | K1=9.1��10-8 K2=1.1��10-12 | K1=7.5��10-3 K2=6.2��10-8 K3=2.2��10-13 |
������˵���в���ȷ���ǣ�������
A. ̼�������ǿ��������
B. ��Ԫ�����������Ҫ�ɵ�һ���������
C. �����£���ˮϡ�ʹ��ᣬ![]() ����
����
D. ��������Һ�м�����NaOH��Һ�����볣������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com