
【题目】如下图所示,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是( )
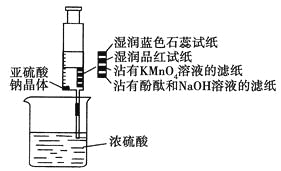
A.蓝色石蕊试纸先变红后褪色
B.沾有KMnO4溶液的滤纸褪色,证明了SO2的漂白性
C.品红试纸褪色,证明了SO2的漂白性
D.沾有酚酞和NaOH溶液的滤纸褪色,证明了SO2的漂白性
 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:
【题目】由乙烷和乙烯都能制得一氯乙烷。
(1)由乙烷制一氯乙烷的化学方程式为____________,反应类型为______________。
(2)在催化剂作用下,由乙烯制一氯乙烷的化学方程式为____________,反应类型为______________。
(3)以上两种方法中_________[填“(1)”或“(2)”]更适合用来制取一氯乙烷,原因是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标号为①~⑩的元素,在元素周期表中的位置如下:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
1 | ① | ② | ||||||
2 | ③ | ④ | ⑤ | ⑥ | ||||
3 | ⑦ | ⑧ | ⑨ | ⑩ |
试回答下列问题:
(1)(填写元素符号)① _____③______⑤_____ ⑦_____
(2)①和④号元素形成的化合物的化学式________,用电子式表示其形成过程为__________。
(3)⑦和⑧号元素的最高价氧化物的水化物的碱性是: ______﹥_________ (填化学式)。⑨和⑩号元素的最高价氧化物的水化物的酸性是: ______ ﹥_________ (填化学式)。
(4)①、⑤、⑦号元素形成的一种化合物的电子式是________,在该化合物中既含有________键,又含有________键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3-对甲苯丙烯酸甲酯(E) 是一种用于合成抗血栓药的中间体,其合成部分路线如下:
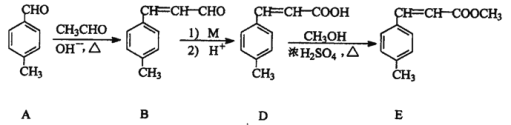
(1)B中含有的官能团名称为_______、__________。
(2)由A转化为B,反应分两步完成,请判断反应类型依次为___________,_________。
(3)D 的分子式为_________________。
(4)1mol E最多能与___________mol 的氢气发生加成反应。
(5)1molB与5mol H2在适当条件下完全加成后,产物分子中含手性碳原子的数目为_____;
(6)D转化为E 的化学反应方程式为________________,
(7)试剂M 可以选用下列中的_________。
A.NaOH 溶液 B.银氨溶液
C.酸性高锰酸钾溶液 D.新制Cu(OH)2 悬浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图回答问题:
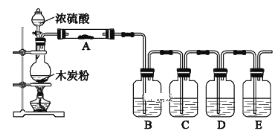
(1)盛装浓硫酸的仪器是___,什么方法证明该装置不漏气?___。
(2)写出浓H2SO4和木炭发生反应的化学方程式:___。如果有0.4mol电子转移,则在标准状况下产生气体___L。
(3)如用图中的装置检验上述反应的全部产物,写出各仪器中应加入的试剂的名称和作用。A中加入的试剂是___,作用是检验产物H2O;B中加入的试剂是品红,褪色现象说明SO2有___性,C中加入的试剂是KMnO4,作用是除去SO2,反应的离子方程式为:___;D中加入的试剂是品红溶液,其作用是___,E中加入的试剂是足量的澄清石灰水,其离子反应方程式是___。
(4)如果将此装置中的木炭粉改为铜,则最左边装置中反应的方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X、Y、Z为前四周期元素,X的基态原子核外电子有21种运动状态,元素Y的原子最外层电子数是其内层的3倍,Z与X、Y不在同一周期,且Z原子核外p电子比s电子多5个。
(1)X基态原子的核外电子排布式为______。
(2)X是石油化工中重要的催化剂之一,如催化异丙苯(![]() )裂化生成苯和丙烯。
)裂化生成苯和丙烯。
①1 mol异丙苯分子中含有σ键的数目为________mol。
②异丙苯分子中碳原子轨道的杂化类型为________。
(3)与Y3分子互为等电子体的阴离子为________。
(4)XZ3易溶于水,熔融状态下能够导电,据此可判断XZ3晶体属于________(填晶体类型)。
(5)元素Ce与Y形成的化合物晶体的晶胞结构如下图,该化合物的化学式为________。
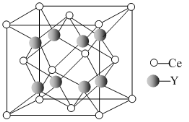
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。请回答:
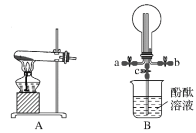
(1)实验室制备氨气的化学方程式为__。
(2)在制取氨气后,如果要干燥氨气,可选用的干燥剂是__。
A.固体氢氧化钠
B.浓硫酸
C.氯化钙
D.五氧化二磷
E.碱石灰
(3)用装置B收集氨气时,氨气的进气口是___(填“a”或“b”)。
(4)待圆底烧瓶中收集满氨气后,关闭a、b,打开装置B中的止水夹c,一段时间后,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是:___、___。
(5)以下装置(盛放的液体均为水)可用于吸收多余氨气的是__(填序号)。
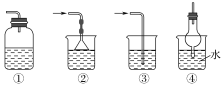
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸镍[(CH3COO)2Ni]是一种重要的化工原料。一种以含镍废料(含NiS、Al2O3、FeO、CaO、SiO2)为原料,制取醋酸镍的工艺流程图如图:
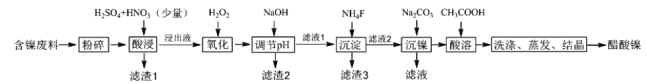
相关离子生成氢氧化物的pH和相关物质的溶解性如表:
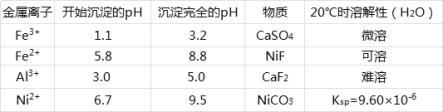
(1)酸浸过程中,1mol NiS失去6NA个电子,同时生成两种无色有毒气体。写出该反应的离子方程式___。
(2)滤渣1和滤渣3主要成分的化学式分别是___、____。
(3)写出氧化步骤中加入过氧化氢发生反应的离子方程式______。
(4)调节pH步骤中,溶液pH的调节范围是____。
(5)沉镍过程中,若c(Ni2+)=2.0 mol/L,欲使100mL该滤液中的Ni2+沉淀完全[c(Ni2+)<10-5mol/L],则需要加入碳酸钠固体的物质的量最少为____mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com