
【题目】Cu与Zn用导线连接后浸入稀硫酸组成原电池装置。下列说法正确的是
A. 锌为负极,铜为正极
B. 铜片溶解,锌片上产生气体
C. 电子由铜极流出经导线流向锌极
D. 溶液中SO42-定向移向铜极
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案科目:高中化学 来源: 题型:
【题目】下列关于元素周期表的叙述中不正确的是( )
A.第ⅡA族中无非金属元素
B.0族中无金属元素
C.第ⅠA族元素单质均能与水反应生成H2
D.金属元素的种类比非金属元素多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,青蒿素为无色针状晶体,难溶于水,易容有机溶剂,熔点为156-157℃。青蒿素是一种有效的抗疟药,某化学兴趣小组对青蒿素的提取和组成进行如下的探究。
Ⅰ.提取青高素的方法之一是乙醚浸取法,提取流程如下:
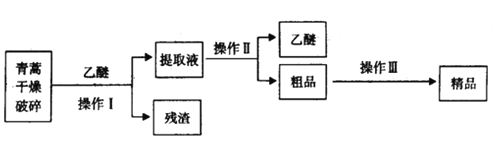
(1)对青蒿进行破碎的目的是___________
(2)操作Ⅰ用到的玻璃仪器是__________,操作Ⅱ的名称是__________
Ⅱ.燃烧法测定青蒿素的最简式:
利用下列实验装置,将28.2g青蒿素放在燃烧管C中充分燃绕,测出生成的CO2和H2O的质量后,计算得出青蒿素的最简式。
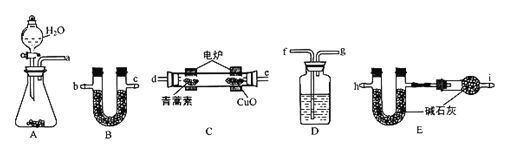
主要实验步骤如下:
①组装仪器,并检查装置的气密性。
②先将A装置的药品反应一会后,再将C装置通电反应。
③称量有关装置的实验前后的质量。
请回答下列问题:
(3)仪器各接口的连接顺序从左到右依次为_____(每个装置限用一次)。
(4)①装置B中的试剂为________,其作用是__________。
②装置C中CuO的作用是__________。
③装置D中的试剂为______,其作用是________________。
④装置E中的试剂为______,其作用是________________。
⑤装置F中的试剂为______,其作用是_________________。
(5)已知青蒿素是烃的含氧衍生物,用合理连接后的装置进行实验,测量数据如表:
装置质量 | 实验前/g | 实验后/g |
B | 22.6 | 42.4 |
E | 80.2 | 146.2 |
则青蒿素的最简式为_____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于取代反应的是
A. 乙烯使酸性KMnO4溶液褪色
B. 乙烯使溴的CCl4溶液褪色
C. 在光照条件下,甲烷与氯气反应
D. 乙醇使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烷在燃烧时能放出大量的热,它也是液化石油气的主要成分,作为能源应用于人们的日常生产和生活。已知:
①2C3H8(g) + 7O2 (g)= 6CO(g) + 8H2O(l) △H1=-2741.8 kJ/mol
②2CO(g)+O2(g)= 2CO2(g) △H2 =-566 kJ/mol
(1) 反应C3H8(g) + 5O2(g)= 3CO2(g) + 4H2O (1) 的△H=_______。
(2) 现有lmol C3H8 在不足量的氧气里燃烧,生成1mol CO 和2mol CO2 以及气态水,将所有的产物通入一个固定体积为1L 的密闭容器中,在一定条件下发生如下可逆反应:CO(g)+ H2O (g) ![]() CO2(g)+H2(g) △H= +4 1.2 kJ/mol
CO2(g)+H2(g) △H= +4 1.2 kJ/mol
①下列事实能说明该反应达到平衡的是______
a.体系中的压强不发生变化
b.v正(H2) = v逆(CO)
c.混合气体的平均相对分子质量不发生变化
d.CO2的浓度不再发生变化
②5min 后体系达到平衡,经测定,H2 为0.8mol,则平衡常数K=_______。
③其他条件不变,向平衡体系中充入少量CO 则平衡常数_____ (填增大、减小或不变)。
(3) 依据(1)中的反应可以设计一种新型燃料电池,一极通入空气,另一极通入丙烷气体;燃料电池内部是熔融的掺杂着氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在其内部可以传导O2-。在电池内部O2-由______极移向______ 极(填“正”或“负”);电池的负极电极反应式为____________。
(4) 用上述燃料电池和惰性电极电解足量Mg(NO3)2 和NaCl 的混合溶液。电解开始后阴极的现象为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光气(COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl2在活性碳催化下合成.
(1)实验室中常用来制备氯气的化学方程式为;
(2)工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,已知CH4、H2、和CO的燃烧热(△H)分别为﹣890.3kJmol﹣1、﹣285.8 kJmol﹣1和﹣283.0 kJmol﹣1 , 则生成1 m3(标准状况)CO所需热量为;
(3)实验室中可用氯仿(CHCl3)与双氧水直接反应制备光气,其反应的化学方程式为;
(4)COCl2的分解反应为COCl2(g)═Cl2(g)+CO(g)△H=+108 kJmol﹣1 . 反应体系平衡后,各物质的浓度在不同条件下的变化状况如下图所示(第10min到14min的COCl2浓度变化曲线未示出): 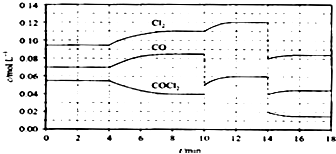
①计算反应在第8min时的平衡常数K=;
②比较第2min反应温度T(2)与第8min反应温度T(8)的高低:T(2) T(8)(填“<”、“>”或“=”);
③若12min时反应于温度T(8)下重新达到平衡,则此时c(COCl2)=molL﹣1
④比较产物CO在2﹣3min、5﹣6min和12﹣13min时平均反应速率[平均反应速率分别以v(2﹣3)、v(5﹣6)、v(12﹣13)表示]的大小;
⑤比较反应物COCl2在5﹣6min和15﹣16min时平均反应速率的大小:v(5﹣6) v(15﹣16)(填“<”、“>”或“=”),原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作: A.用250mL容量瓶等仪器配制成250mL烧碱溶液;
B.用移液管(或碱式滴定管)量取25mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂;
C.在天平上准确称取烧碱样品W g,在烧杯中加蒸馏水溶解;
D.将物质的量浓度为M molL﹣1的标准HCl溶液装入酸式滴定管,调整液面,记下开始刻度数V1 mL;
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点耗酸体积V2 mL.
回答下列问题:
(1)正确的操作步骤是(填写字母)→→→D→
(2)滴定时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视
(3)终点时颜色变化是
(4)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有(填字母序号)
A.滴定终点读数时俯视
B.锥形瓶水洗后未干燥
C.酸式滴定管使用前,水洗后未用盐酸润洗
D.酸式滴定管在滴定前有气泡,滴定后气泡消失
(5)该烧碱样品的纯度计算式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与醋酸有关的反应方程式正确的是
A. 与烧碱反应:OH-+CH3COOH → CH3COO-+H2O
B. 与CaCO3反应:CO32-+2CH3COOH → 2CH3COO-+CO2↑+H2O
C. 乙醛氧化:CH3CHO+O2 ![]() CH3COOH
CH3COOH
D. 制乙酸乙酯:CH3COOH+C2H518OH ![]() CH3COOC2H5+H218O
CH3COOC2H5+H218O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知气态烃A中碳的质量分数为92.3%,C与D互为同分异构体,F含有两个与乙醇相同的官能团,有关物质的转化关系如图:
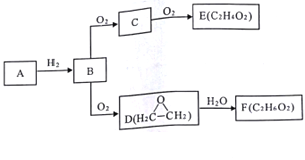
请回答:
(1)写出B的电子式___________________。
(2)C→E的反应类型___________________。
(3)D→F的化学方程式___________________。
(4)下列说法正确的是___________________。
A. 可用燃烧法鉴别A和B
B. C在一定条件下可与氢气发生还原反应
C. E和F在浓硫酸作用下加热反应,产物只有一种
D. 与D的最简式相同,相对分子质量为88的物质可能是E的同系物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com