

| | a | b | c |
| I | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| II | 碱石灰 | 浓硫酸 | 无水氯化钙 |
| III | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:实验题
| 操作 | 现象 |
| 取4 g漂粉精固体,加入100 mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝(约为12),后褪色 |
 | i.液面上方出现白雾; ii.稍后,出现浑浊,溶液变为黄绿色;iii.稍后,产生大量白色沉淀,黄绿色褪去 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.实验室可用加热分解碳酸钙的方法制取二氧化碳气体 |
| B.二氧化硫易溶于水,硫酸工厂的尾气可以直接用水吸收 |
| C.二氧化氮可与水反应而被吸收,故硝酸工业的尾气应该用水吸收 |
| D.配制较高浓度的碘水时,应先将碘溶于酒精中,再加水稀释 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
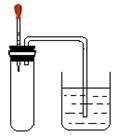
| A.①或③ | B.②或④ | C.①或③或④ | D.③或④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将人群转移到地势较低的地方,等待营救 |
| B.将槽罐车推入附近的水塘中,撒上石灰 |
| C.用高压水枪向空中喷洒大量酸性溶液 |
| D.被转移人群可戴上用NaOH处理过的口罩 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题



| CaCO3用量 | 未加CaCO3时 | 加约四分之一时 | 加一半时 | 全部加完时 |
| 读数/g | 318.3 | 325.3 | 334.5 | 359.5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
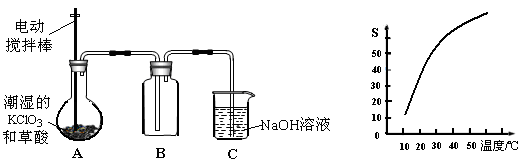
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com