
化学与生活密切相关,以下说法不正确的是
| A.CaO能与SO2反应,可作燃煤的脱硫剂 |
| B.食醋可用于除去暖水瓶中的水垢 |
| C.明矾水解时产生具有吸附性的胶体粒子,可作净水剂 |
| D.铁在空气中易形成致密的氧化膜,可用来运输浓硫酸 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
根据“绿色化学”的思想,某化学家设计了下列化学反应步骤:
该方案的相关叙述正确的是
| A.该实验的目的是制取HBr | B.该过程的副产品是Hg |
| C.该过程得到的气体只有H2 | D.该过程的本质是水的分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
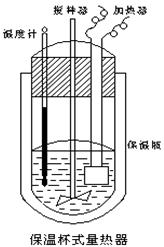
(共14分)(Ⅰ)某化学实验小组为确定过氧化氢分解的最佳催化条件,用如图装置进行实验,反应物用量和反应停止的时间数据如下表:
 MnO2 MnO2时间 H2O2 | 0.1 g | 0.3 g | 0.8 g |
| 10 mL 1.5% | 223 s | 67 s | 56 s |
| 10 mL 3.0% | 308 s | 109 s | 98 s |
| 10 mL 4.5% | 395 s | 149 s | 116 s |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.天然油脂的分子中含有酯基,属于酯类 |
| B.煤经处理变为气体燃料的过程属于物理变化 |
| C.A12O3可以与水反应得到其对应水化物 Al(OH)3 |
| D.可以用加热使蛋白质变性的方法分离提纯蛋白质 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关仪器用途的说法正确的是 ( )
| A.试管、烧杯均可用于给液体、固体加热 |
| B.使食盐水中NaCl结晶析出时,用到的仪器有坩埚、酒精灯、玻璃棒、泥三角 |
| C.区别NaCl、Na2SO4时常用到胶头滴管、试管 |
| D.漏斗可用于过滤及向滴定管中添加溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
废电池造成污染的问题日益受到关注,集中处理废电池的首要目的是
| A.回收石墨电极 |
| B.回收电池外壳的金属材料 |
| C.防止电池中渗泄的电解液腐蚀其他物品 |
| D.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
(16分)以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:
(1)酸溶过程中Fe2O3与稀硫酸反应的化学方程式为 ;
“滤渣A”主要成份的化学式为 。
(2)还原过程中加入FeS2的目的是将溶液中的Fe3 +还原为Fe2 +,而本身被氧化为H2SO4,请完成该反应的离子方程式:FeS2 + 14Fe3 + + H2O="=" 15Fe2 + + SO42- + 。
(3)氧化过程中,O2、NaOH与Fe2+反应的离子方程式为 。
(4)为了确保铁红的质量,氧化过程需要调节溶液的pH的范围是 (几种离子沉淀的pH见下表);滤液B可以回收的物质有(写化学式) 。
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
【化学选修2:化学与技术】(15分)工业上生产高氯酸时,还同时生产了一种常见的重要含氯消毒剂和漂白剂亚氯酸钠(NaClO2),其工艺流程如下:
已知:①NaHSO4溶解度随温度的升高而增大,适当 条件下可结晶析出。
②高氯酸是至今为止人们已知酸中的最强酸,沸点90 ℃。
请回答下列问题:
反应器Ⅰ中发生反应的化学方程式为 ,冷却的目的是 ,能用蒸馏法分离出高氯酸的原因是 。
(2)反应器Ⅱ中发生反应的离子方程式为 。
(3)通入反应器Ⅱ中的SO2用H2O2代替同样能生成NaClO2,请简要说明双氧水在反应中能代替SO2的原因是 。
(4)Ca(ClO)2、ClO2、NaClO2等含氯化合物都是常用的消毒剂和漂白剂,是因为它们都具有 ,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
苯巴比妥是安眠药的成分,化学式为C12H12N2O3,分子结构中有两个六元环:下图是以A为原料合成苯巴比妥的流程示意图。完成下列填空。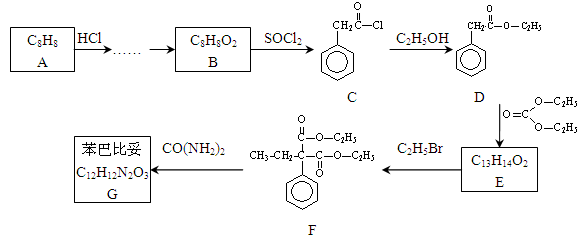
已知:①有机物D、E中亚甲基(—CH2—)的氢原子受羰基影响活性较高,容易发生如下反应:
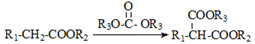
②
(1)芳香烃A与HCl反应后,制取B还需进行反应的类型依次为 。
(2)一种酯与B互为同分异构体,且苯环上只有一个取代基,该酯同分异构体
有 种,写出其中一种结构的系统命名 。
(3)写出D 转化为E的化学方程式:
(4)苯巴比妥G的结构简式:
(5)E与CO(NH2)2在一定条件下合成的高分子结构简式:
(6)已知: ,请设计合理方案以B的同系物
,请设计合理方案以B的同系物 为原料
为原料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com