
【题目】下列叙述错误的是( )
A.阿伏加德罗常数的符号为NA,约为6.02×1023mol-1
B.等物质的量的O2与O3所含氧原子数相同
C.在0.5molNa2SO4中Na+数约为6.02×1023
D.根据微粒数目和阿伏加德罗常数,可计算微粒的物质的量
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值.下列说法正确的是( )
A.16 g O2中含有的氧分子数为NA
B.1 mol Mg变为Mg2+时失去的电子数目为2NA
C.常温常压下,11.2 L H2中含有的氢分子数为0.5NA
D.1 molL﹣1 CaCl2溶液中含有的氯离子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.完全由非金属元素组成的化合物不一定是共价化合物
B.构成分子晶体的粒子一定含有共价键
C.含有离子键的晶体一定是离子晶体
D.含有共价键的化合物一定是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加“碘”食盐较多使用的碘酸钾(KIO3),在工业上可用电解法制取.以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应方程式为:KI+3H2O ![]() KIO3+3H2↑.下列有关说法不正确的是( )
KIO3+3H2↑.下列有关说法不正确的是( )
A.电解时,石墨作阴极,不锈钢作阳极
B.电解时,阳极反应是:I﹣﹣6e﹣+3H2O═IO ![]() +6H+
+6H+
C.溶液调节至强酸性,对生产不利
D.电解后阴极周围溶液的pH升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯是重要的有机化工原料.下列关于苯的说法正确的是( )
A.在通常情况下,为气体
B.能在空气中燃烧,燃烧时冒浓烟
C.能够使酸性高锰酸钾溶液褪色
D.在通常状况下,易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)氨气是重要的化工原料.实验室可用浓氨水和来制取氨气.
a.烧碱 b.生石灰 c.氯化铵
(2)某实验小组设计了下列装置进行氨的催化氧化实验.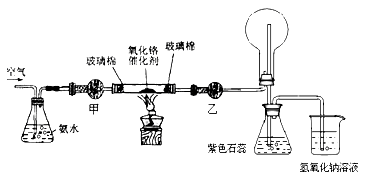
①盛放氨水的实验仪器的名称为;在加热条件下,硬质玻璃管中发生反应的化学方程式为 .
②实验时发现:如果缺少乙处的干燥管,将反应后的气体直接通入烧瓶,则烧瓶中先产生白雾,随即产生白烟,其原因是 .
③烧杯中盛有NaOH溶液的作用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备1,2﹣二溴乙烷的反应原理如下:CH3CH2OH ![]() CH2=CH2 , CH2=CH2+Br2→BrCH2CH2Br.用少量的溴和足量的乙醇制备1,2﹣二溴乙烷的装置如图:
CH2=CH2 , CH2=CH2+Br2→BrCH2CH2Br.用少量的溴和足量的乙醇制备1,2﹣二溴乙烷的装置如图: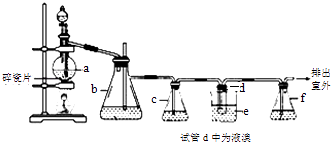
有关数据列表如下:
乙醇 | 1,2﹣二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/gcm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | ﹣130 | 9 | ﹣116 |
回答下列问题:
(1)在装置c中应加入(选填序号),其目的是吸收反应中可能生成的酸性气体.
①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)判断d管中制备二溴乙烷反应已结束的最简单方法是 .
(3)将二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的(填“上”或“下”)层.
(4)若产物中有少量未反应的Br2 , 最好用(填正确选项前的序号)洗涤除去.
①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)反应过程中需用冷水冷却(装置e),其主要目的是;但不用冰水进行过度冷却,原因是:
(6)以1,2﹣二溴乙烷为原料,制备聚氯乙烯,为了提高原料利用率,有同学设计了如下流程:1,2﹣二溴乙烷通过(①)反应制得(②),②通过( ③)反应制得氯乙烯,由氯乙烯制得聚氯乙烯.
①(填反应类型)②(填该物质的电子式)③(填反应类型)写出第一步的化学方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com