
【题目】在恒压密闭容器中,充入一定量的H2和CO2 发生如下可逆反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)ΔH <0,实验测得反应物在不同温度下,反应体系中CO2的平衡转化率与压强的关系曲线如图所示。
CH3OH(g)+H2O(g)ΔH <0,实验测得反应物在不同温度下,反应体系中CO2的平衡转化率与压强的关系曲线如图所示。

(1)该反应的ΔS______0(填>或<),该反应在_______(填“低温”或“高温”)条件下利于自发进行;
(2)比较T1与T2的大小关系:T1__T2(填“<”、“=”或“>”),理由是_______。
(3)在T1和P6的条件下,往密闭容器中充入3 mol H2和1 mol CO2,该反应在第5 min时达到平衡,此时容器的体积为1.8 L;则该反应在此温度下的平衡常数为____;若温度不变,压强恒定在P8的条件下重新达到平衡时,容器的体积变为_____L。
【答案】<低温<反应Ⅲ为放热反应,温度降低,反应正向移动,所以T1<T24/27或0.1488/15或0.533
【解析】
(1)根据方程式可知正反应是体积减小的放热的可逆反应,因此该反应的ΔS<0;由于ΔG=ΔH-TΔS<0时反应自发进行,所以该反应在低温下自发进行;
(2)反应放热反应,温度降低,反应正向移动,二氧化碳的转化率升高,所以T1<T2;
(3)在T1和P6的条件下平衡时二氧化碳的转化率是40%,则根据方程式可知
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
初始量:1mol 3mol 0 0
变化量:0.4mol 1.2mol 0.4mol 0.4mol
平衡量:0.6mol 1.8mol 0.4mol 0.4mol
达到平衡时容器的体积为1.8 L,所以CO2、H2、CH3OH、H2O(g)的浓度分别是(mol·L-1)1/3、1、2/9、2/9,所以平衡常数K=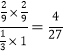 ;若温度不变,压强恒定在P8的条件下重新达到平衡时,二氧化碳的转化率是60%。则
;若温度不变,压强恒定在P8的条件下重新达到平衡时,二氧化碳的转化率是60%。则
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
初始量:1mol 3mol 0 0
变化量:0.6mol 1.8mol 0.6mol 0.6mol
平衡量:0.4mol 1.2mol 0.6mol 0.6mol
温度不变,K不变,则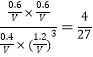
解得V=8/15 L。


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:
【题目】化合物丙由如下反应制得:
C4H10O![]() C4H8
C4H8 ![]() C4H8Br2(丙)
C4H8Br2(丙)
丙的结构简式不可能是
A. CH3CH2CHBrCH2Br B. CH3CH(CH2Br)2
C. CH3CHBrCHBrCH3 D. (CH3)2CBrCH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是重要的资源,可以制备一系列物质。
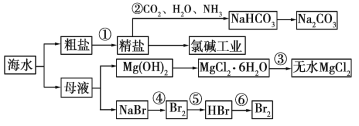
下列说法正确的是
A. 除去粗盐中 SO42-、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH 溶液→BaCl2 溶液→Na2CO3 溶液→过滤→盐酸
B. 步骤②中,应先通 CO2,再通 NH3
C. 步骤③中可将 MgCl2·6H2O 晶体在空气中直接加热脱水
D. 步骤④、⑤、⑥反应中,溴元素均被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 乙烯中碳碳双键的键能是乙烷分子中碳碳单键的两倍
B. 120℃时,乙烯与足量的氧气在密闭中充分燃烧后恢复到原温度,容器内压强不变
C. 1 mol乙烯与氯气完全反应后所得的产物,再与氯气在光照条件下发生取代反应,两个过程中消耗氯气的总物质的量最多为6mol
D. 分子式为C5H12O且能与钠反应放出气体的物质共有6种结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是有机物 A、B、C、D 的有关信息:
A | ①无色无味、难溶于水; ②最简单的有机化合物 | B | ①能使溴的四氯化碳溶液褪色; ②比例模型为: ③能与水在一定条件下反应生成 D |
C | ①由 C、H 两种元素组成; ②球棍模型为: | D | ①能与钠反应,但不能与 NaOH 溶液反应; ②在催化剂条件下能被空气中的氧气氧化为 E |
根据表中信息回答下列问题:
(1)写出B 的结构式_____;D 的官能团名称是_____。
(2)B 能使溴的四氯化碳溶液褪色,反应后生成物的名称_____。
(3)B→D 的化学反应类型为_____。
(4)D 催化氧化生成E 的化学方程式为_____。
(5)C 的分子式是_____,写出在浓硫酸作用下,C 在 50 ~60℃与浓硝酸发生反应的化学方程式:_____。
(6)与A 互为同系物的物质均符合通式 CnH2n+2,当 n=5 时,该有机物有_____种同分异构体, 其中碳链最短的同分异构体的结构简式是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上采用如下反应合成甲醇:CO(g)+2H2(g) ![]() CH3OH(g)
CH3OH(g)
(1)分析该反应并回答下列问题:
①该反应的平衡常数表达式为K=____________。
②下列选项能判断该反应达到平衡状态的依据有__________(填序号)。
A.2v(正)(H2)= v(逆)(CO)
B.一定条件下,单位时间内消耗2molH2的同时生成 1mol CH3OH
C.恒温、恒容时,容器内的压强不再变化
D.恒温、恒容时,容器内混合气体的密度不再变化
E.混合气体的平均相对分子质量不随时间而变化
(2))下图是该反应在不同温度下CO转化率随时间的变化曲线:
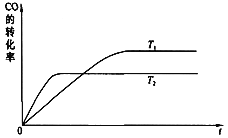
①该反应的△H________0(填“>”、“<”或“=”)。
②T1和T2温度下的平衡常数:K1 ________ K2(填“>”、“<”或“=”)。
(3)某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为________________。
(4)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH1=-1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2=-566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH3=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式________________________。
(5)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如图所示。
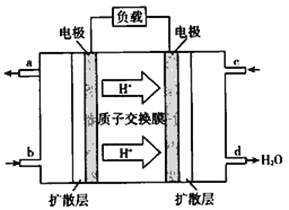
①该电池工作时,b口通入的物质为__________(填 化学式,下同),c 口通入的物质为__________。 ②该电池正极的电极反应式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝氢化钠(NaAlH4)是有机合成的重要还原剂,其合成线路如下图所示。
![]()
(1)铝氢化钠遇水发生剧烈反应,其反应的化学方程式为__________________________。
(2)AlCl3与NaH反应时,需将AlCl3溶于有机溶剂,再将得到的溶液滴加到NaH粉末上,此反应中NaH的转化率较低的原因是__________________________________________。
(3)实验室利用下图装置制取无水AlCl3。
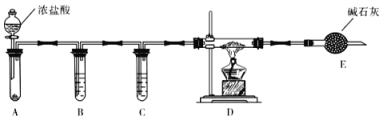
①A中所盛装的试剂是_______________。
②点燃D处酒精灯之前需排除装置中的空气,其操作是____________________________
(4)改变A和D中的试剂就可以用该装置制取NaH,若装置中残留有氧气,制得的NaH中可能含有的杂质为____________ 。
(5)现设计如下四种装置,测定铝氢化钠粗产品(只含有NaH杂质)的纯度。
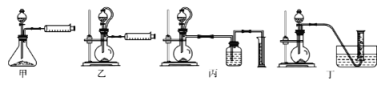
从简约性、准确性考虑,最适宜的装置是_________(填编号)。称取15.6g样品与水完全反应后,测得气体在标准状况下的体积为22.4L,样品中铝氢化钠的质量为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com