
����Ŀ��ij�о���ѧϰС�������ͼװ���Ƽ���������ijЩ���ʡ�
��1����ȡCl2����ʽΪ��MnO2��4HCl(Ũ)![]() MnCl2��Cl2����2H2O��������������Ƿ���Ư���ԡ�
MnCl2��Cl2����2H2O��������������Ƿ���Ư���ԡ�

��Aװ����ʢװŨ����������������� ��
��B��ʢ�б���ʳ��ˮ���������� �� C��ʢװ���Լ��� ��
��ͨ��Cl2��D��E�й۲쵽�������� ����������ɵó��Ľ����� ��
��F��ʢ��NaOH��Һ���������� ��
��2������ȥ�����ƣ�����KMnO4�������� HCl���䷴Ӧ����ʽ���£�
2KMnO4+16HCl(Ũ)��2KCl+2MnCl 2+5Cl 2��+8H2O
�ٸ÷�Ӧ�е��������� ��
�����ֻ�ԭ�Ե�HCl��������Ե�HCl������֮����_________��
��1mol KMnO4��ȫ��Ӧ����������HCl�����ʵ���Ϊ mol��
��8mol HCl��ȫ��Ӧ��������Cl 2�ڱ�״���µ����Ϊ ����
���𰸡���1���ٷ�Һ©��������HCl���壻Ũ�����D�в�������ɫ��E�в�����ɫ�������Cl2 û��Ư���Ԣ�������������ֹ������Ⱦ
��2����KMnO4��5��3��2�֣���5mol��56����2�֣�
��������
�����������1���� ʢװŨ����������������Ƿ�Һ©������A���ų������庬���Ȼ����ˮ����������װ��B��ʢ�ű����Ȼ�����Һ���������е��Ȼ��⣬װ�� C��ʢ��Ũ��������ˮ�������۸��������û��Ư���ԣ�D�й۲쵽�������Dz�������ɫ��������ˮ��Ӧ���ɵĴ��������Ư���ԣ�����E�еIJ�����ɫ����������ɵó��Ľ����Ǹ����Cl2 û��Ư���ԡ��������ж���Ϊ��ֹ������Ⱦ������װ��F��ʢ������������Һ����������
��2�����÷�Ӧ����Ԫ�صĻ��ϼ���+7�۵õ��ӱ�Ϊ+2�ۣ����Ը����������������
����Ӧ2KMnO4+16HCl(Ũ)��2KCl+2MnCl 2+5Cl 2��+8H2O�У�����ԭ���غ�֪�����ϼ۱仯���Ȼ���ļ�������10�����ϼ۲�����Ȼ���ļ�������6�����Ա��ֻ�ԭ�Ե�HCl��������Ե�HCl������֮����10��6=5��3��
���豻�������Ȼ�������ʵ�����x��
2KMnO4��10 HCl��Ũ��������ԭ����
2mol 10mol
1mol x
x=5mol����1mol KMnO4��ȫ��Ӧ����������HCl�����ʵ���Ϊ5mol��
�������������������y��
2KMnO4+16HCl��Ũ��=2KCl+2MnCl2+5Cl2��+8H2O
16mol 112L
8mol y
y=56L����8mol HCl��ȫ��Ӧ��������Cl 2�ڱ�״���µ����Ϊ56L��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�м���BaCl2��Һ���ɰ�ɫ�������ټ���ϡ����������ܽ�Ҳ�������ݳ�����������Һ��
A��һ������SO42�C B��һ������Ag+
C�����ܺ���SO42�C ��Ag+ ��CO32�C D�����ܺ���SO42�C ��Ag+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����캸��ʱ����Ǧ�����������Ҫԭ������ ��
A. ���ӿ���ʴ���� B. ����ǿ��
C. �����۵� D. ������չ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����(����)
A���Ҵ����Ҷ�������������Ϊͬϵ�ͬϵ��֮�䲻����Ϊͬ���칹��
B��������̼�ɱ���Ϊͬ��������
C��C2H5OH��CH3OCH3��Ϊͬ���칹��
D�����ʯ��ʯī��Ϊͬλ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(N2H4)����һ�ֹ�ҵԭ�ϣ�����һ����Ҫ�Ĺ�ҵ��Ʒ��
(1) �����ʵ����İ��������ֱ�����������������Ӧ������Ϊ������ˮ����ת�Ƶĵ�����֮��Ϊ___________��
(2) ������һ�������¿ɰ���ʽ�ֽ�:3N2H4(g)=N2(g)+4NH3(g)����֪����N-H��N-N��N��N��1 mol�����յ���������Ϊ390.8 kJ��193 kJ��946 kJ��������1 mol N2����Ӧ________(�����ų�������������)___ _______kJ��������
(3)NH3-O2ȼ�ϵ�صĽṹ��ͼ��ʾ��
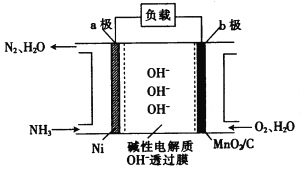
�� a��Ϊ��ص�________(����������������)����
��������1 mol N2ʱ����·���������ӵ����ʵ���Ϊ_____________��
(4)�������Ը�Ч���ѳ��̵����е�NO�Ӷ����� N2���÷�Ӧ�����������뻹ԭ��������ʵ���֮��Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ���������ɻ�����Ⱦ����
A������ȼ�ϵ��
B��п�̵��
C�����ӵ��
D��Ǧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���������ȷ����
A. ����Ͳ��ȡ25 mL����ˮ B. �÷�Һ©�������Ҵ���ˮ
C. ���ձ��ܽ�FeCl3���� D. ��������ƽ����NaCl����5.8g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������нṹ�����ʣ���CH3(CH2)3CH3
��CH3CH2CH2CH2CH3
��CH3CH2CH2CH2CH2CH3
��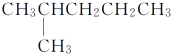
��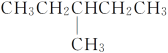
��
��
���У�����ͬϵ�����________������ͬ���칹�����__________������ͬ�����ʵ���________��
A�٢� B�ڢ� C�ۢܢݢޢ� D�٢� E�ۢܢݢ� F�ܢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com