
【题目】某溶液中加入BaCl2溶液生成白色沉淀,再加入稀硝酸沉淀不溶解也无气体逸出,则这种溶液中
A.一定含有SO42– B.一定含有Ag+
C.可能含有SO42– 或Ag+ 或CO32– D.可能含有SO42– 或Ag+
科目:高中化学 来源: 题型:
【题目】海带中碘元素的检验可经过以下几个步骤完成(已知H2O2能将海带中的I﹣氧化成I2,I2遇淀粉变蓝),各步骤中选用的实验用品不能都用到的是( )
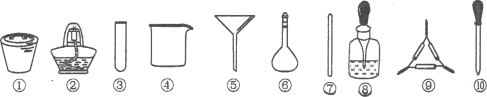
A.将海带剪碎后灼烧成灰,选用①、②和⑨
B.将海带灰加蒸馏水溶解,选用④、⑥和⑦
C.过滤得到滤液,选用④、⑤和⑦
D.取滤液,先加入几滴稀硫酸,再滴加H2O2,最后滴加淀粉溶液,选用③和⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.Al2O3难溶于水,不跟水反应,所以它不是Al(OH)3对应的氧化物
B.因为Al2O3是金属氧化物,所以它是碱性氧化物
C.Al2O3属于两性氧化物
D.Al2O3能与所有的酸、碱溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关元素周期律的叙述中,正确的是
A. 氧化性强弱:F2<Cl2
B. 金属性强弱:K<Na
C. 酸性强弱:H3PO4<H2SO4
D. 碱性强弱:NaOH<Mg(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):

实验序号 | A溶液 | B溶液 |
① | 20 mL 0.1 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |
② | 20 mL 0.2 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |
(1)该反应的离子方程式 。(已知H2C2O4是二元弱酸)
(2)该实验探究的是 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是 < (填实验序号)。
(3)若实验①在2 min末收集了2.24 mL CO2(标准状况下),则在2 min末, c(MnO4-)=__________mol/L(假设混合液体积为50 mL)
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定 来比较化学反应速率。(一条即可)
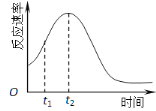 (5)小组同学发现反应速率总是如右图,其中t1~t2时间内速率变快的主要原因可能是:
(5)小组同学发现反应速率总是如右图,其中t1~t2时间内速率变快的主要原因可能是:
① ;② 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X的原子,其M层与K层电子数相同;元素Y的原子,其M层上有7个电子.X和Y所形成的稳定化合物的相对分子质量为( )
A.100
B.95
C.88
D.80
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计如图装置制检验氯气的某些性质。
(1)制取Cl2方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,检验干燥氯气是否有漂白性。
MnCl2+Cl2↑+2H2O,检验干燥氯气是否有漂白性。

①A装置中盛装浓盐酸的仪器的名称是 。
②B中盛有饱和食盐水,其作用是 , C中盛装的试剂是 。
③通入Cl2后,D、E中观察到的现象是 ;根据现象可得出的结论是 。
④F中盛有NaOH溶液,其作用是 。
(2)若撤去酒精灯,改用KMnO4氧化上述 HCl。其反应方程式如下:
2KMnO4+16HCl(浓)=2KCl+2MnCl 2+5Cl 2↑+8H2O
①该反应中的氧化剂是 。
②表现还原性的HCl与表现酸性的HCl的质量之比是_________。
③1mol KMnO4完全反应,被氧化的HCl的物质的量为 mol。
④8mol HCl完全反应,产生的Cl 2在标准状况下的体积为 升。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com