
| m |
| M |
| m |
| M |
| 16g |
| 16g/mol |
| m |
| M |
| 16g |
| 32g/mol |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、常温下HNO2溶液的pH小于7 |
| B、用HNO2溶液做导电实验,灯泡很暗 |
| C、HNO2和NaCl溶液不能发生反应 |
| D、用1L0.1 mol/L HNO2溶液和2L0.1mol/LNaOH溶液做导电实验,后者灯泡更亮 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
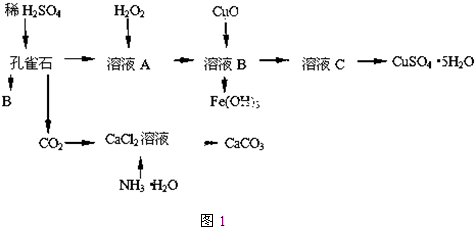
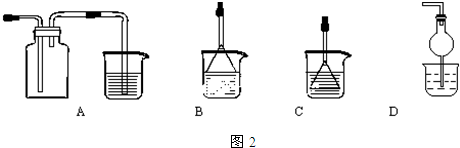
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||


查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ba2+ |
| B、NH4+ |
| C、K+ |
| D、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2、SO3都是极性分子 |
| B、KF是离子化合物,HF为共价化合物 |
| C、在NH4+和[Cu(NH3)4]2+中都存在配位键 |
| D、PCl3和NF3分子中所有原子的最外层都达到8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氮气的摩尔质量等于NA个N2分子的相对分子质量之和 |
| B、含有NA个氦原子的氦气在标准状况下的体积约为11.2 L |
| C、NA个氮气分子与NA个一氧化碳分子的质量比是1:1 |
| D、1.8gNH4+中含有的质子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com