
【题目】下列生成乙酸的方法中,最符合绿色化学思想的是
A. 乙酸乙酯水解:CH3COOC2H5+H2O![]() CH3COOH+C2H5OH
CH3COOH+C2H5OH
B. 乙醛氧化:2CH3CHO+O2![]() 2CH3COOH
2CH3COOH
C. 淀粉发酵:淀粉→葡萄糖→乙醇→乙酸
D. 丁烷氧化:2CH3CH2CH2CH3+5O2![]() 4CH3COOH+2H2O
4CH3COOH+2H2O
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
【题目】过氧化钙可以用于改善地表水质、处理含重金属粒子废水和治理赤潮,也可用于应急供氧等。实验室可用工业碳酸钙(含MgCO3、FeCO3等杂质)制取纯净的碳酸钙,然后再用纯的碳酸钙制取过氧化钙,其主要流程如下:
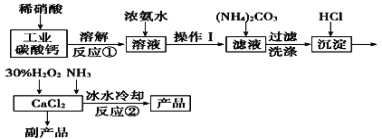
已知:CaO2·8H2O呈白色微溶于水。
(1)写出反应①中氧化还原反应的离子方程式: ______________。
(2)向反应①后的溶液中加浓氨水的目的是: __________________。
(3)反应②常用冰水控制温度在0℃左右,其可能原因是(写出两种):
①__________________;②______________。
(4)测定产品中CaO2的含量的实验步骤是
第一步:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2 mol/L的H2SO4溶液,充分反应。
第二步:向上述锥形瓶中加入几滴淀粉溶液。
第三步:逐滴滴入浓度为c mol·L-1的Na2S2O3标准溶液至反应终点,消耗Na2S2O3溶液V mL。
已知:I2+2S2O![]() ===2I-+S4O
===2I-+S4O![]() 。
。
①滴定终点的现象为____________,产品中CaO2的质量分数为_________________
②某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的CaO2的质量分数可能________ (填“不受影响”“偏低”或“偏高”),原因是_____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将6 molH2和3 molCO充入容积为0.5 L的密闭容器中,进行反应:2H2(g) + CO(g)![]() CH3OH(g),6 s时反应达到平衡,此时容器内压强为开始时的0.6倍,则H2的平均反应速率为________________,CO的转化率为____________________。
CH3OH(g),6 s时反应达到平衡,此时容器内压强为开始时的0.6倍,则H2的平均反应速率为________________,CO的转化率为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 提取溴水中的溴单质的方法:加入酒精后,振荡、静置、分液
B. 除去CO2气体中混有的SO2的方法:通过装有饱和碳酸氢钠溶液的洗气瓶
C. 向铜和浓硫酸反应后的混合液中加水,可以判断有无铜离子生成
D. 金属钠着火可以二氧化碳气体来灭火
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体区别与其他分散系的本质特征是( )
A.能发生丁达尔现象
B.胶体粒子能通过滤纸空隙
C.胶体在一定条件下能稳定存在
D.胶体分散质粒子直径在1nm~100nm之间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关生物体内化合物的叙述,正确的是( )
A. 淀粉、糖原和纤维素水解得到的单体相同
B. 种子从休眠进入萌发状态,结合水/自由水比值上升
C. 人体内的脂肪能贮存能量、调节代谢
D. 无机盐在人体中都以离子状态存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X是一种具有果香味的合成香料,下图为合成X的某种流程:
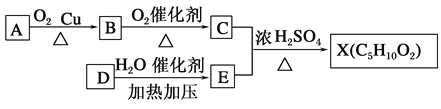
提示:D的产量可以用来衡量一个国家的石油化工水平。
请根据以上信息,回答下列问题:
(1)A分子中官能团的名称是_____________,E的结构简式是_________________。
(2)D→E的化学反应类型为_____________反应。
(3)上述A、B、C、D、E、X六种物质中,互为同系物的是____________________。
(4)C的一种同分异构体F可以发生水解反应,则F的结构简式为________、________。
(5)反应C+E→X的化学方程式为____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有pH均为2的a盐酸、b醋酸两瓶溶液,与足量锌反应放出等体积H2所需时间的长短顺序是a____b(用“>”、“<”、“=”表示,下同);完全中和等物质的量的NaOH溶液需两种酸的体积大小顺序是a____b。
(2)已知水在25℃和95℃时,其电离平衡曲线如下图所示:
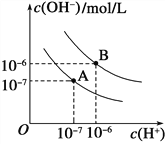
①则25℃时水的电离平衡曲线应为________(填“A”或“B”)。
②95℃时水的离子积KW=___________________。
③25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为____________。
④95℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.实验室用大理石和稀盐酸制取CO2:2H++CO32-=CO2↑+H2O
B.稀盐酸与氢氧化钡溶液反应:H++OH-=H2O
C.硫酸镁溶液与氢氧化钡溶液反应:SO42-+Ba2+==BaSO4↓
D.稀硫酸与氢氧化钡溶液反应:Ba2++OH-+SO42-+H+=BaSO4↓+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com