
【题目】以下实验能获成功的是( )
A.用酒精和稀硫酸混合加热到170℃制乙烯
B.将铁屑、溴水、苯混合制溴苯
C.在苯酚溶液中滴入浓溴水出现白色沉淀
D.将淀粉溶液与稀硫酸共热一段时间,取其溶液直接加入银氨溶液检验其是否发生水解
科目:高中化学 来源: 题型:
【题目】某元素最高正价与负价绝对值之差为4,该元素的离子与跟其核外电子排布相同的离子形成的化合物是( )
A.K2S B.MgO C.MgS D.NaF
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用10mL 0.1mol/L的BaCl2溶液分别和相同体积的硫酸铁、硫酸锌和硫酸钾三种溶液反应,均恰好使三份溶液中的SO42-离子完全转化为BaSO4沉淀,则三种硫酸盐溶液的物质的量浓度之比是( )
A. 3∶2∶2 B. 1∶2∶3 C. 3∶1∶1 D. 1∶3∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活及生产过程直接排放的超细颗粒物是大气中可吸入颗粒物的主要来源。能减少大气中可吸入颗粒物的措施有( )
A. 加高工厂烟囱 B. 推广使用新能源汽车
C. 安装除尘设备 D. 将高污染产业转型升级
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,不符合第ⅦA族元素性质特征的是( )
A. 从上到下元素的非金属性增强 B. 易形成-1价离子
C. 最高价氧化物的水化物显酸性(氟除外) D. 从上到下氢化物的稳定性依次减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列反应中,HCl作还原剂的是( )
A. NaOH + HCl = NaCl + H2O
B. Zn + 2HCl = ZnCl2 + H2↑
C. MnO2 + 4HCl(浓)![]() MnCl2 + 2H2O + Cl2↑
MnCl2 + 2H2O + Cl2↑
D. CuO + 2HCl = CuCl2 + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(18分)Na2S2O3是重要的化工原料,易溶于水。在中性或碱性环境中稳定。
I.制备Na2S2O35H2O
反应原理:Na2SO3(aq)+S(s)![]() Na2S2O3(aq)
Na2S2O3(aq)
实验步骤:
①称取15g Na2SO3加入圆底烧瓶中,再加入80ml蒸馏水。另取5g研细的硫粉,用3ml 乙醇润湿,加入上述溶液中。
②安装实验装置(如图所示,部分加持装置略去),水浴加热,微沸60分钟。

③趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O35H2O,经过滤,洗涤,干燥,得到产品。
回答问题:
(1)硫粉在反应前用乙醇润湿的目的是 。
(2)仪器a的名称是 ,其作用是 。
(3)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是 ,检验是否存在该杂质的方法是 。
(4)该实验一般控制在碱性环境下进行,否则产品发黄,用离子方程式表示其原因:
。
II.测定产品纯度
准确称取Wg产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 molL1碘的标准溶液滴定。
反应原理为:2S2O32+I2=S4O62-+2I
(5)滴定至终点时,溶液颜色的变化: 。
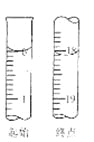
(6)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为 mL。产品的纯度为(设Na2S2O35H2O相对分子质量为M) 。
III.Na2S2O3的应用
(7)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42,常用作脱氧剂,该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不属于自发进行的变化是 ( )
A.红墨水加到清水使整杯水变红B.冰在室温下融化成水
C.NaHCO3 转化为 Na2CO3D.铁器在潮湿的空气中生锈
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂离子电池是新型高能电池,它以质量轻、能量高而受到了普遍重视,目前已研制成功多种锂离子电池,某种锂离子电池的总反应为Li+MnO2=LiMnO2,下列说法中正确的是
A. Li是正极,电极反应式为Lie=Li+
B. Li是负极,电极反应式为Lie=Li+
C. MnO2是负极,电极反应式为MnO2+e=MnO2
D. Li是负极,电极反应式为Li2e=Li2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com