
【题目】某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:
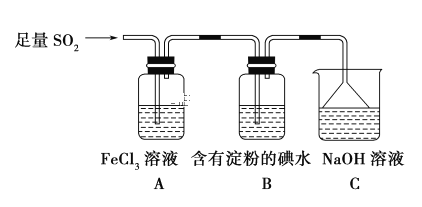
(1)装置C的作用是 ______________________。
(2)在上述装置中通入过量的SO2,请设计实验验证A中SO2与Fe3+发生了氧化还原反应: __________________。
(3)通入气体后B装置中观察到的现象是_____________。
【答案】吸收过量的SO2 在A装置中滴加KSCN溶液若血红色物质消失,则SO2与Fe3+发生了氧化还原反应 溶液蓝色消失
【解析】
SO2具有还原性,可将Fe3+还原成Fe2+,可将I2还原成I-,如图所示A中Fe3+还原成Fe2+,可用KSCN溶液验证,B中I2还原成I-现象为溶液蓝色消失,C为尾气吸收装置,吸收过量的SO2,以此回答。
(1)C为尾气吸收装置,吸收过量的SO2,防止环境污染,故答案为:吸收过量的SO2;
(2)A中Fe3+还原成Fe2+,可在A装置中滴加KSCN溶液若血红色物质消失,则SO2与Fe3+发生了氧化还原反应,故答案为:在A装置中滴加KSCN溶液若血红色物质消失,则SO2与Fe3+发生了氧化还原反应;
(3),B中I2还原成I-,I2遇淀粉显蓝色,故现象为溶液蓝色消失,故答案为:溶液蓝色消失。


科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A. AlCl3溶液中加入过量氨水:Al3++4NH3·H2O===AlO![]() +2H2O+4NH
+2H2O+4NH![]()
B. 硫化钠的水解反应:S2-+2H2O![]() H2S+2OH-
H2S+2OH-
C. 将等体积等物质的量浓度的NaHCO3溶液与Ba(OH)2溶液混合HCO![]() +Ba2++OH-===BaCO3↓+H2O
+Ba2++OH-===BaCO3↓+H2O
D. 单质铜与稀硝酸反应:Cu+2H++2NO![]() ===Cu2++2NO↑+H2O
===Cu2++2NO↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的化学用语表达正确的是( )
A | Mg(HCO3)2溶液与足量的NaOH溶液反应 | Mg2++2HCO |
B | 过量SO2通入到NaClO溶液中: | SO2+H2O+ClO-===HClO+ |
C | 向Al2(SO4)3溶液中加入过量的稀氨水 | Al3 ++4NH3·H2O=AlO2—+4NH4++2H2O |
D | KClO碱性溶液与Fe(OH)3反应制取K2FeO4 | 3ClO﹣+2Fe(OH)3=2FeO42﹣+3Cl﹣+4H++H2O |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙基丹皮酚肟胺基醇醚衍生物(H)具有很好的抗血小板聚集活性,是良好的心脑血管疾病的治疗药物。
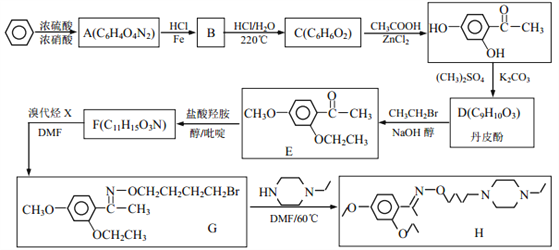
已知:①![]()
②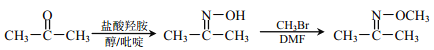
③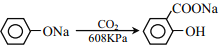
请回答:
(1)E中含有的官能团名称为_________;
(2)丹皮酚的结构简式为_________;
(3)下列说法不正确的是(___)
A.乙基丹皮酚肟胺基醇醚衍生物 H 的分子式为 C21H34O3N3
B.物质B 可能溶于水,且能与盐酸反应生成有机盐
C. D→E 和 G→H 的反应类型均为取代反应
D.物质 C 能使浓溴水褪色,而且 1mol C 消耗 2molBr2
(4)写出 F→G 的化学方程式_________。
(5)写出满足下列条件 F 的所有同分异构体的结构简式_________。
①能发生银镜反应;1molF 与 2molNaOH恰好反应。
②1H-NMR 谱显示分子中含有 5 种氢原子; IR 谱显示有-NH2,且与苯环直接相连。
(6)阿司匹林也具有抑止血小板凝聚的作用。结合题给信息,请以硝基苯和乙酸酐为原料设计合理的路线制备阿司匹林( )。(用流程图表示,无机试剂任选)______。
)。(用流程图表示,无机试剂任选)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图所示。又知AgCl的Ksp=1.8×10-10。下列说法不正确的是( )
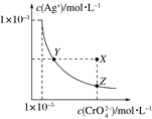
A.t℃时,Ag2CrO4的Ksp为1×10-8
B.饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点
C.t℃时,Y点和Z点时Ag2CrO4的Ksp相等
D.t℃时,将0.01 mol·L-1AgNO3溶液滴入20 mL 0.01 mol·L-1KCl和0.01 mol·L-1K2CrO4的混合溶液中,Cl-先沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值。下列说法正确的是
A.常温下,1 L pH=9的CH3COONa溶液中,发生电离的水分子数为1×10-9NA
B.常温下,10 mL 5.6 mol/L FeC13溶液滴到100 mL沸水中,生成胶粒数为0.056NA
C.向Na2O2通入足量的水蒸气,固体质量增加bg,该反应转移电子数为![]()
D.6.8 g KHSO4晶体中含有的离子数为0.15 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家设计了一种将电解饱和食盐水与电催化还原CO2相耦合的电解装置如图所示。下列叙述错误的是
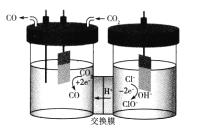
A.理论上该转化的原子利用率为100%
B.阴极电极反应式为![]()
C.Na+也能通过交换膜
D.每生成11.2 L(标况下)CO转移电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M可用作消毒剂、抗氧化剂、医药中间体。实验室由芳香烃A制备M的一种合成路线如图:
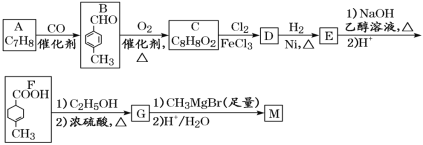
已知:R1COOR2
请回答:
(1)C的化学名称为___;D中含氧官能团的结构简式为___。
(2)由B转化为C的反应类型为___;G的分子式为___。
(3)由E转化为F的第一步反应的化学方程式为___。
(4)M的结构简式为___。
(5)芳香化合物Q为C的同分异构体,Q能发生银镜反应,其核磁共振氢谱有4组吸收峰。写出符合要求的Q的一种结构简式___。
(6)参照上述合成路线和信息,以苯甲酸甲酯和CH3MgBr为原料(无机试剂任选),设计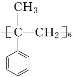 制备的合成路线___。
制备的合成路线___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往锅炉注入Na2CO3溶液浸泡,将水垢中的CaSO4转化为CaCO3,再用盐酸去除,下列叙述正确的是
A. 温度升高Na2CO3溶液的Kw和c(H+)均会增大
B. CaSO4能转化为CaCO3,说明Ksp(CaCO3)>Ksp(CaSO4)
C. CaCO3溶解于盐酸而CaSO4不溶,是因为硫酸酸性强于盐酸
D. 沉淀转化的离子方程式为CO32(aq)+CaSO4(s)![]() CaCO3(s)+SO42(aq)
CaCO3(s)+SO42(aq)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com