
| A、在碳酸氢钠溶液中加入过量的氢氧化钙溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| B、向明矾溶液中加入少量的Ba(OH)2溶液:Al3++3OH-+Ba2++SO42-=BaSO4↓+Al(OH)3↓ |
| C、向Fe2(SO4)3溶液中加入过量的Na2S:2Fe3++S2-=2Fe2++S↓ |
| D、向含有1molFeBr2溶液中通入标准状况下22.4L的Cl2:2Br-+Cl2=Br2+2Cl- |


科目:高中化学 来源: 题型:
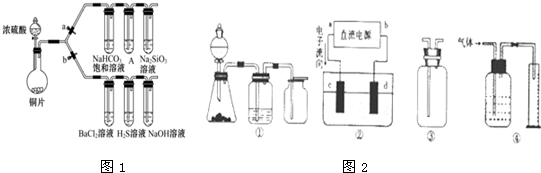
| 滴加的溶液 | 氯 水 | 氨 水 |
| 沉淀的化学式 |
查看答案和解析>>
科目:高中化学 来源: 题型:
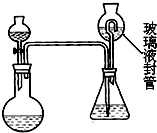
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 3 |
| A、①④⑤⑦⑧ | B、①③⑤⑧ |
| C、④⑤⑥⑦⑧ | D、①③⑤⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1000mL,212g |
| B、950mL,543.4g |
| C、950mL,572g |
| D、500mL,286g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、目前使用的燃料液化石油气,其主要成分均属于烃 |
| B、油脂、纤维素、蛋白质都是高分子化合物 |
| C、石油裂解、煤的气化、海水制镁都包含化学变化 |
| D、食用白糖的主要成分是蔗糖,小苏打的主要成分是碳酸氢钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com