
| ||
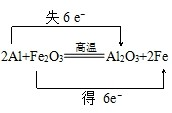 ,反应在工业上的用途是焊接铁轨;
,反应在工业上的用途是焊接铁轨; ;Fe2O3;Al;0.3;焊接铁轨;
;Fe2O3;Al;0.3;焊接铁轨;


科目:高中化学 来源: 题型:
| A、在碳酸氢钠溶液中加入过量的氢氧化钙溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| B、向明矾溶液中加入少量的Ba(OH)2溶液:Al3++3OH-+Ba2++SO42-=BaSO4↓+Al(OH)3↓ |
| C、向Fe2(SO4)3溶液中加入过量的Na2S:2Fe3++S2-=2Fe2++S↓ |
| D、向含有1molFeBr2溶液中通入标准状况下22.4L的Cl2:2Br-+Cl2=Br2+2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
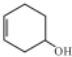 )能发生多种不同反应;回答下列问题:
)能发生多种不同反应;回答下列问题: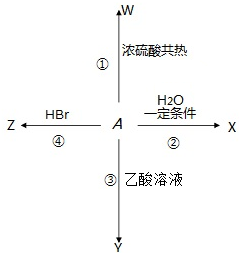
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K只随温度的改变而改变 |
| B、K>Q(Q为浓度熵)平衡正向移动 |
| C、正、逆反应的平衡常数数值相同,符号相反 |
| D、K值变化平衡一定发生移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡向正向移动 |
| B、重新达到平衡时PCl5转化率增大 |
| C、重新达到平衡后PCl3体积分数减小 |
| D、反应速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大力发展电动车,减少燃油汽车的尾气排放量 |
| B、燃煤时加入适量石灰石,可减少废气中SO2的排放量 |
| C、多环芳烃是强致癌物,能吸附在PM2.5的表面进入人体 |
| D、PM2.5含有的铅、镉、铬、钒、砷等对人体有害的元素均是金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化 |
| B、NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道 |
| C、二者均是sp3杂化,NH3分子中有一对孤对电子,它对成键电子的排斥作用较强 |
| D、氨气分子是极性分子而甲烷是非极性分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com