

| A.AgO/Ag电极是负极 |
| B.当电极上析出1.08 g Ag时,电路中转移的电子为0.02mol |
| C.Al电极的反应式为:Al—3e-+4OH-= AlO2-+2H2O |
| D.在电解质溶液中OH-由Al电极移向AgO/Ag电极 |


科目:高中化学 来源:不详 题型:单选题
| A.只有AgI沉淀生成 |
| B.AgCl和AgI沉淀等量生成 |
| C.AgCl和AgI沉淀都有,但以AgCl沉淀为主 |
| D.AgCl和AgI沉淀都有,但以AgI沉淀为主 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
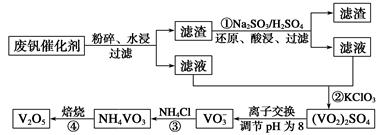
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
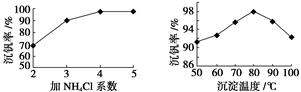
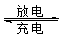 VO2++H2O+V3+,电池充电时阳极的电极反应式为 。
VO2++H2O+V3+,电池充电时阳极的电极反应式为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2PbSO4+2H2O。下列说法正确的是
2PbSO4+2H2O。下列说法正确的是| A.放电时,负极的电极反应式是PbO2+4H++SO42一+2e一=PbSO4+2H2O |
| B.充电时,电解液中H2SO4的浓度将变小 |
| C.放电时,PbO2发生氧化反应 |
| D.充电时,蓄电池的正极和外接电源的正极相连 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.化学电源有一次电池、可充电电池和燃料电池等,一次电池只能放电,不能充电 |
| B.铅蓄电池应用广泛,主要优点是单位重量的电极材料释放的电能大 |
| C.燃料电池具有能量利用率高、可连续使用和污染轻等优点 |
| D.锂电池是一种高能电池,体积小、重量轻,单位质量能量比高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.通入CH4的电极为负极 | B.正极发生氧化反应 |
| C.燃料电池工作时,溶液中的OH-向负极移动 | D.该电池使用一段时间后应补充KOH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 )是重要的能源物质,研究甲醇具有重要意义。
)是重要的能源物质,研究甲醇具有重要意义。 可制取甲醇,其反应为:
可制取甲醇,其反应为:

 的
的  晶体,在高温下它能传导
晶体,在高温下它能传导 离子。电池工作时正极反应为 。
离子。电池工作时正极反应为 。
 氧化成
氧化成 ,然后以
,然后以 做氧化剂把水中的甲醇氧化成
做氧化剂把水中的甲醇氧化成 而净化。实验室用下图装置模拟上述过程:
而净化。实验室用下图装置模拟上述过程:
 ,该过程中被氧化的元素是 ,当产生标准状况下2.24L
,该过程中被氧化的元素是 ,当产生标准状况下2.24L 时,共转移电子 mol。
时,共转移电子 mol。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该电池负极的电极反应为:Al–3e-=Al3+ |
| B.电池工作时,溶液中铝离子向正极移动 |
| C.消耗相同质量金属时,用锂作负极产生电子的物质的量比用铝时多 |
| D.当导线中有3.612×1024个电子通过时,电池负极质量减少27 g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com