
阿伏加德罗常数为NA,下列说法中正确的是( )
A.62 g Na2O溶于水后所得溶液中含有的O2-数为NA
B.在含Al3+总数为NA的AlCl3溶液中,Cl-总数大于3NA
C.常温常压下,16 g甲基(—13CH3)所含的中子数为10NA
D.0.5 mol Cu和足量浓硝酸反应可以生成22.4 L NO2
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源: 题型:
化学与人类生活、社会可持续发展密切相关,下列措施有利于节能减排、保护环境的是①加快化石燃料的开采与使用;②研发易降解的生物农药;③应用高效洁净的能源转换技术;④田间焚烧秸秆;⑤推广使用节能环保材料 ⑥废电池进行集中回收处理 ( )
A. ①③⑤⑥ B. ②③⑤⑥ C. ①②④ D. ②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)已知:①Fe(s)+ O2(g)===FeO(s) ΔH1=-272.0 kJ·mol-1;
O2(g)===FeO(s) ΔH1=-272.0 kJ·mol-1;
②2Al(s)+ O2(g)===Al2O3(s) ΔH2=-1 675.7 kJ·mol-1。
O2(g)===Al2O3(s) ΔH2=-1 675.7 kJ·mol-1。
Al和FeO发生铝热反应的热化学方程式是_____________________________某同学认为,铝热反应可用于工业炼铁,你的判断是______________(填“能”或“不能”),
你的理由是________________________________
(2)发射卫星用N2H4为燃料,NO2为氧化剂,两者反应生成N2和水蒸气, 已知N2(g)+2O2(g)=2NO2(g), 1= +67.7KJ/mol
1= +67.7KJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(l), 2 = —622KJ/mol
2 = —622KJ/mol
H2O(l) = H2O(g) ΔH3 = +44 kJ·mol-1
试写出N2H4与 NO2反应生成N2和水蒸气的热化学方程式__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
 某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是
某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是
A.a点是负极,b点是正极
B.铂片一端发生还原反应
C.铅笔端有少量的氯气产生
D.铅笔端作阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(如图1),一段时间后换成蒸馏装置(如图2)进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品,请回答下列问题:

(1)在图1烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入________,目的是________。
冷凝管的作用是_____________________。
(2)图2中冷凝水应从________口进。
(3)现设计分离以上粗产品的操作步骤如下图。已知a为饱和碳酸钠溶液,①为分液。请回答:

试剂b是________;分离方法③是________。
(4)某化学课外小组设计了下图所示的制取乙酸乙酯的装置(图中的铁架台、铁夹、加热装置已略去),与图1装置相比,主要优点有(写一点):___________________________
_______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.除去Cl2中少量的HCl,可将混合气体通过盛有饱和NaCl溶液的洗气瓶
B.向久置于空气的FeCl2溶液中滴入KSCN溶液,会产生Fe(SCN)3血红色沉淀
C.向某溶液中滴入稀盐酸产生使澄清石灰水变浑浊的气体,该溶液一定含有CO
D.实验室可采用分液法直接分离乙酸乙酯和乙醇的混合液
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3 、FeCO3、MgO、CaO等,生产工艺流程示意如图下:
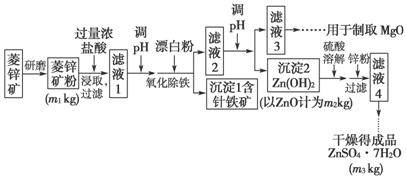
(1)将菱锌矿研磨成粉的目的是____________________________________。
(2)完成“氧化除铁”步骤中反应的离子方程式:
□Fe(OH)2+□______+□______===□Fe(OH)3+□Cl-
(3)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O和H,化学式量为89,化学式是________________。
(4)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为___。
| Mg(OH)2 | Zn(OH)2 | MgCO3 | CaCO3 | |
| 开始沉 淀的pH | 10.4 | 6.4 | ||
| 沉淀完全 的pH | 12.4 | 8.0 | ||
| 开始溶 解的pH | 10.5 | |||
| Ksp | 5.6×10-12 | 6.8×10-6 | 2.8×10-9 |
(5)工业上从“滤液3”制取MgO过程中,合适的反应物是________(选填序号)。
a.大理石粉 b.石灰乳
c.纯碱溶液 d.烧碱溶液
(6)“滤液4”之后的操作依次为________、________、过滤、洗涤、干燥。
(7)分析图中数据,菱锌矿粉中ZnCO3 的质量分数不低于________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用 NA表示阿伏加德罗常数的值。下列说法正确的是( )
A.1 mol Na2O2晶体中共含有4NA个离子
B.0.1 mol AlCl3完全水解转化为氢氧化铝胶体,生成0.1 NA个胶粒
C.常温常压下,16 g O2和O3的混合气体中含有NA个氧原子
D.电解精炼铜时每转移NA个电子,阳极溶解32 g铜
查看答案和解析>>
科目:高中化学 来源: 题型:
氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如下图所示。常温下S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体。下列说法错误的是( )
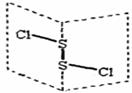 A.S2Cl2的结构式为Cl-S-S-Cl
A.S2Cl2的结构式为Cl-S-S-Cl
B. S2Cl2为含有极性键和非极性键的非极性分子
C.S2Br2与S2Cl2结构相似,熔沸点:S2Br2>S2Cl2
D.S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com