
【题目】盐酸在不同的反应中,可以分别表现出酸性、氧化性和还原性。现在有如下三个反应,有关判断正确的是( )
①Zn+2HCl![]() ZnCl2+H2↑;②NaOH+HCl
ZnCl2+H2↑;②NaOH+HCl![]() NaCl+H2O;
NaCl+H2O;
③2HCl![]() H2↑+Cl2↑
H2↑+Cl2↑
选项 | 有关判断 |
A | 反应①是置换反应,HCl表现还原性 |
B | 反应②是复分解反应,HCl表现氧化性 |
C | 反应③中HCl既表现氧化性也表现还原性 |
D | 反应①中氢原子失去电子 |
A. A B. B C. C D. D
科目:高中化学 来源: 题型:
【题目】已知:CH4(g)+2O2(g)==CO2(g)+2H2O(l) △H=-Q1kJ·mol-1①
2H2(g)+O2(g)=2H2O(g) △H=-Q2kJ·mol-1②
2H2(g)+O2(g)=2H2O(l) △H=-Q3kJ·mol-1③
常温下,取体积比为4∶1的甲烷和氢气的混合气体11.2 L(标准状况),经完全燃烧后恢复到常温,放出的热量(单位:kJ)( )
A. 0.4Q1+0.05Q3 B. 0.4Q1+0.05Q2 C. 0.4Q1+0.lQ3 D. 0.4Q1+0.2Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由Na、Mg、Al、Fe四种金属单质中的两种组成的混合物共12g,跟足量盐酸反应,产生5.6L H2(标准状况下),由此可判断混合物中必定含有( )
A. Na B. Mg C. Al D. Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一定温度和压强下,1体积X2(g)和3体积Y2(g)化合生成2体积Z(g),则Z气体的化学式是 。
(2)A、B两种气体组成的混合气体8.6 g,在标准状况下体积为8.96 L。已知A与B的物质的量之比为3∶1,相对分子质量之比为14∶1,由此可推断A可能是 ,B可能是 。
(3)在标准状况下,CO和CO2的混合气体质量为36 g,体积为22.4 L,则CO所占的体积是 L,质量是 g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.葡萄糖和蔗糖互为同分异构体
B.铁和浓硫酸在常温下反应
C.明矾可用作饮用水的消毒剂
D.32gO2中含有的氧原子数是2×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H4)是一种重要的化工原料,既可用于制药,又可用作火箭燃料。回答下列问题:
(1)已知反应的热化学方程式如下:
①N2H4(g)![]() N2(g)+2H2(g) △H1;
N2(g)+2H2(g) △H1;
②N2(g)+3H2(g)![]() 2NH3(g) △H2。
2NH3(g) △H2。
反应热△H1 _____(填“大于”或“小于”) △H2。向2 L的恒容密闭容器中充入1 mol N2H4,发生反应①,![]() (用x表示)与时间的关系如图1所示,则该温度下,反应①的平衡常数K=___________________。
(用x表示)与时间的关系如图1所示,则该温度下,反应①的平衡常数K=___________________。

(2)肼在另一条件下也可达到分解平衡,同时生成两种气体,且其中一种气体能使湿润的红色石蕊试纸变蓝。图2为平衡体系中肼的体积分数与温度、压强的关系。
①该反应的化学方程式为________________________________________。
②p2_______ (填“大于”或“小于”) p1。
③图中N2H4的平衡体积分数随温度升高而降低,其原因是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲基丙烯酸甲酯——CH2=C(CH3)COOCH3是合成有机玻璃的单体.
旧法合成的反应是:①(CH3)2C=O+HCN→(CH3)2C(OH)CN
②(CH3)2C(OH)CN+CH3OH+H2SO4→CH2=C(CH3)COOCH3+NH4HSO4
新法合成的反应是:CH3C≡CH+CO+CH3OH→CH2=C(CH3)COOCH3,与旧法相比,新法的突出优点是
A. 原料无爆炸危险 B. 原料都是无毒物质
C. 没有副产物,原料利用率高 D. 对设备腐蚀性较小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO和KClO3,且![]() 的值与温度高低有关.当n(KOH)=amol时,下列有关说法错误的是( )
的值与温度高低有关.当n(KOH)=amol时,下列有关说法错误的是( )
A. 若某温度下,反应后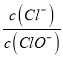 =2,则溶液中
=2,则溶液中 =0.2
=0.2
B. 参加反应的氯气的物质的量等于0.5a mol
C. 改变温度,反应中转移电子的物质的量ne的范围: ![]() a mol≤ ne ≤
a mol≤ ne ≤![]() a mol
a mol
D. 改变温度,产物中KClO3的最大理论产量为![]() mol
mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中可以提取溴,但得到的液溴中常常溶有少量氯气,除去氯气应该采用的方法是
A. 加适量的KI溶液
B. 通入溴蒸气
C. 加入适量的NaOH溶液
D. 加入适量的NaBr溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com