
可逆反应2A(g)+3B(g) 
 2C(g)+D(g)在四种不同条件下的反应速率分
2C(g)+D(g)在四种不同条件下的反应速率分
别为:①v(A)=0.5 mol/(L·min) ②v(B)=0.6 mol/(L·min)
③v(C)=0.35 mol/(L·min) ④v(D)=0.4 mol/(L·min)
则该反应在不同条件下反应速率最快的是( )
A.① B.② C.③ D.④
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
(1)现有以下物质:①NaCl晶体 ②干冰 ③液态的醋酸 ④铜 ⑤BaSO4固体⑥蔗糖⑦酒精 ⑧熔融的KNO3 ⑨浓HNO3 回答下列问题(填序号)以上物质能导电的是_________________________________;
以上物质属于非电解质的是___________________________;
以上物质属于电解质的是________________________ ___;
查看答案和解析>>
科目:高中化学 来源: 题型:
在带有活塞的密闭容器中发生反应:Fe2O3+3H2===2Fe+3H2O(g),采取下列措施能改变反应速率的是( )
A.增加Fe2O3的量 B.保持容器体积不变,增加H2输入量
C.减少Fe的量 D.保持容器体积不变,增加H2O(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
银氨溶液可用于检测CO气体,实验室研究的装置如图:
|
| 已知:银氨溶液制备反应为 Ag++2NH3·H2O=[Ag(NH3)2]++2H2O。 反应结束后试管C底部有黑色沉淀生成,分离出上层清液和底部黑色固体备用。 |
(1)甲酸(HCOOH)遇浓硫酸分解生成CO和H2O,该反应体现浓硫酸的 (填“强氧化性”或“脱水性”)。
(2)装置A中软管的作用是 。
(3)为验证上层清液中产物的成分,进行如下实验:
a.测得上层清液pH为10。
b.向上层清液中滴加几滴Ba(OH)2溶液,发现有白色浑浊出现,同时产生能使湿润
红色石蕊试纸变蓝的气体。
c.取新制的银氨溶液滴加几滴Ba(OH)2溶液,无明显现象。
①实验c的目的是 。
②根据上述实验现象判断,上层清液中产物成分为 (填化学符号)。
(4)设计实验证明黑色固体的成分是Ag:
可供选择的试剂有:浓硫酸、浓硝酸、NaOH溶液、NaCl溶液。
取少量上述黑色固体,用蒸馏水洗净, ,说明黑色固体是Ag单质。(补充必要的实验内容及实验现象)
(5)从银氨溶液中回收银的方法是:向银氨溶液中加入过量盐酸,过滤,向沉淀AgCl
中加入羟氨(NH2OH),充分反应后可得银,羟氨被氧化为N2。
①写出生成AgCl沉淀的离子反应 。
②若该反应中消耗6.6 g羟氨,理论上可得银的质量为 g。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
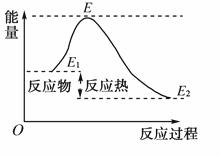
A.反应物分子间的有效碰撞是反应的先决条件
B.反应物的分子的每次碰撞都能发生化学反应
C.活化分子具有比普通分子更高的能量
D.如图所示正反应的活化能为E-E 1
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,反应2SO2 + O2  2SO3达到平衡时,n(SO2)∶n(O2)∶n(SO3) =
2SO3达到平衡时,n(SO2)∶n(O2)∶n(SO3) =
2∶3∶4。缩小体积,反应再次达到平衡时,n(O2)=0.8mol,n(SO3)=1.4mol,
此时SO2的物质的量应是( )
A.0.4mol B.0.6mol C.0.8mol D.1.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中进行如下反应: X2(气) + Y2(气) 
 2Z(气), 已知 X2、Y2、
2Z(气), 已知 X2、Y2、
Z的起始浓度分别为 0.1 mol/L, 0.3 mol/L, 0.2 mol/L, 在一定的条件下, 当
反应达到平衡时, 各物质的浓度有可能是( )
A.Y2为0.2 mol/L B.Y2 为0.35 mol/L
C.X2 为0.2 mol/L D. Z为 0.4 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
配制0.1mol/L盐酸溶液480mL,用量筒量取密度为1.19g/cm3质量分数为37%的浓盐酸约(取整数)( )mL注入烧杯中。用蒸馏水洗涤烧杯2~3次,将洗涤液注入容量瓶中。
A 3.5 B 3.8 C 2.5 D 4.2
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学反应 2A 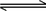 B+D 在四个不同条件下进行.B、D起始为0.反应物A的浓度(mol/L)随反应时间(min)变化情况如下表:
B+D 在四个不同条件下进行.B、D起始为0.反应物A的浓度(mol/L)随反应时间(min)变化情况如下表:
| 实验序号 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 1 | 800℃ | 1.0 | 0.8 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据表中数据完成下列填空:
(1)在实验1,反应在10至20min内的平均速率为 mol/(L.min)
(2)在实验2,A的初始浓度C2= 1.0 mol/L,反应经20min就达到平衡,可推测实验2中还隐含的条件是 .
(3)设实验3的反应速率为υ3,实验1的反应速率为υ1,则υ3 υ1(填“<“,“=“,“>“),且C3 1.0mol/L (填“<“,“>“或“=“).
(4)比较实验4和实验1,可推测该反应 吸热 反应(填“吸热“或”放热“),理由是: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com