
在密闭容器中进行如下反应: X2(气) + Y2(气) 
 2Z(气), 已知 X2、Y2、
2Z(气), 已知 X2、Y2、
Z的起始浓度分别为 0.1 mol/L, 0.3 mol/L, 0.2 mol/L, 在一定的条件下, 当
反应达到平衡时, 各物质的浓度有可能是( )
A.Y2为0.2 mol/L B.Y2 为0.35 mol/L
C.X2 为0.2 mol/L D. Z为 0.4 mol/L
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
已知反应:
①101kPa时,2C(s)+O2(g)=2CO(g);ΔH=-221 kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O;ΔH=-57.3 kJ/mol
下列结论正确的是( )
A.碳的燃烧热大于110.5 kJ/mol
B.①的反应热为221 kJ/mol
C.稀硫酸与稀NaOH溶液反应的中和热为114.6 kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3 kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
稀土是工业味精,邓小平同志说过“中东有石油,我们有稀土”。稀土元素铈(Ce)主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法正确的是 ( )
A.电解熔融CeO2制Ce,铈在阳极获得
B.铈有四种稳定的核素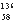 Ce、
Ce、 Ce、
Ce、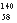 Ce、
Ce、 Ce,它们互为同素异形体
Ce,它们互为同素异形体
C.用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++Fe2+=Ce3++Fe3+
D.由于氧化性:Ce4+>Fe3+,而I—有强还原性,所以铈溶于氢碘酸的化学方程式可表示为:2Ce+6HI=2CeI3+3H2↑。
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应2A(g)+3B(g) 
 2C(g)+D(g)在四种不同条件下的反应速率分
2C(g)+D(g)在四种不同条件下的反应速率分
别为:①v(A)=0.5 mol/(L·min) ②v(B)=0.6 mol/(L·min)
③v(C)=0.35 mol/(L·min) ④v(D)=0.4 mol/(L·min)
则该反应在不同条件下反应速率最快的是( )
A.① B.② C.③ D.④
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒容密闭容器中A(g)+3B(g)
 2C(g) ΔH<0,达平衡后,将气体混
2C(g) ΔH<0,达平衡后,将气体混
合物的温度降低,下列叙述中不正确的是 ( )
A.容器中混合气体的平均相对分子质量增大
B.正反应速率增大,逆反应速率减小,平衡向正反应方向移动
C.正反应速率和逆反应速率都变小,C的百分含量增加
D.混合气体密度的变化情况不可以作为判断反应是否再次达平衡的依据
查看答案和解析>>
科目:高中化学 来源: 题型:
根据反应4FeS2+11O2 ═ 2Fe2O3+8SO2,试回答下列问题:
(1)常选用哪些物质来表示该反应的化学反应速率 、 ;
(2)当生成SO2的速率为0.64 mol/(L·s)时,则氧气减少的速率为 ;
(3)如测得4 s后O2的浓度为2.8 mol/L,此时间内SO2的速率为0.4 mol/(L·s),
则开始时氧气的浓度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作均要用玻璃棒,其中玻璃棒的作用及其目的相同的是 ( )
① 过滤 ② 蒸发 ③ 溶解 ④ 向容量瓶转移液体
A.①和② B.①和④ C.③和④ D.①和③
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式中正确的是 ( )
A. 铜片插入硝酸银溶液中: Cu + Ag+ = Cu2+ + Ag
B.氢氧化钡溶液与稀硫酸混合:Ba2++ OH-+H++SO42- =BaSO4↓+ H2O
C.石灰乳与Na2CO3溶液混合:Ca2++CO32-==CaCO3↓
D.碳酸钙溶于稀盐酸中: CaCO3+2H+=Ca2++H2O+CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子在给定的条件下一定能大量共存的是
A.加入Al粉放出H2的溶液中:Na+、K+、Fe3+、NO3—
B.c(Fe3+)=0.1mol/L的溶液中:NH4+、AlO2—、SO42—、HCO3—
C.水电离出的c(H+)=1×10-13mol/L的溶液中:Mg2+、K+、NO3—、Cl—
D.c(H+)=1×10-13mol/L的溶液中:K+、Cl-、AlO2-、CO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com