
下列实验操作均要用玻璃棒,其中玻璃棒的作用及其目的相同的是 ( )
① 过滤 ② 蒸发 ③ 溶解 ④ 向容量瓶转移液体
A.①和② B.①和④ C.③和④ D.①和③
科目:高中化学 来源: 题型:
下列叙述中,不能用平衡移动原理解释的是( )
A.红棕色的NO2,加压后颜色先变深后变浅
B.高压比常压有利于合成SO3的反应
C.由H2(g)、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深
D.黄绿色的氯水光照后颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
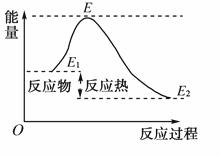
A.反应物分子间的有效碰撞是反应的先决条件
B.反应物的分子的每次碰撞都能发生化学反应
C.活化分子具有比普通分子更高的能量
D.如图所示正反应的活化能为E-E 1
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中进行如下反应: X2(气) + Y2(气) 
 2Z(气), 已知 X2、Y2、
2Z(气), 已知 X2、Y2、
Z的起始浓度分别为 0.1 mol/L, 0.3 mol/L, 0.2 mol/L, 在一定的条件下, 当
反应达到平衡时, 各物质的浓度有可能是( )
A.Y2为0.2 mol/L B.Y2 为0.35 mol/L
C.X2 为0.2 mol/L D. Z为 0.4 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
测定稀硫酸和稀氢氧化钠中和热的实验装
置如右图所示.
(1)写出该反应的热化学方程式(中和热为57.3 kJ/mol):
__________________________________________;
(2) 装置图中碎泡沫塑料所起作用为: ;
(3) ①取50 mL NaOH溶液和30 mL硫酸溶液进行实验,
实验数据如下表.请填写下表中的空白:
| 温度 实验次数 | 起始温度T1/℃ | 终止温度T2/℃ | 温度差平均值(T2-T1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | ________ |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 |
②若上述实验所测中和热数值偏小,产生偏差的原因可能是( )
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
配制0.1mol/L盐酸溶液480mL,用量筒量取密度为1.19g/cm3质量分数为37%的浓盐酸约(取整数)( )mL注入烧杯中。用蒸馏水洗涤烧杯2~3次,将洗涤液注入容量瓶中。
A 3.5 B 3.8 C 2.5 D 4.2
查看答案和解析>>
科目:高中化学 来源: 题型:
将a%的某物质的水溶液加热蒸发掉m g水(溶质不挥发、且蒸发过程无溶质析出),所得溶液体积为V L,溶质的质量分数为蒸发前的2倍,设溶质的相对分子质量为M,则蒸发后所得溶液的物质的量浓度为( )mol/L
A ma/2VM B ma/100VM C 20ma/2VM D ma/50VM
查看答案和解析>>
科目:高中化学 来源: 题型:
反应P(g)+Q(g)⇌M(g)+N(s)△H<0,达到平衡时,下列说法正确的是( )
|
| A. | 减小容器体积,平衡不移动 | B. | 加入催化剂,M的产率增大 |
|
| C. | 增大c(P),P的转化率增大 | D. | 降低温度,Q的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。请回答:
(1)用化学符号表示下列4种微粒:
A:________;B:________;C:________;D________。
(2)写出A、B、E三种微粒反应的离子方程式: ___________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com