
| A、用托盘天平称取10.50g的干燥的NaC1固体 |
| B、蒸馏时温度计水银球应插入混合液中且不与烧瓶底部接触 |
| C、配制浓硫酸和浓硝酸的混酸时,应将浓硫酸慢慢加到浓硝酸中,及时搅拌和冷却 |
| D、测溶液的pH需先用蒸馏水润湿pH试纸,再用干燥洁净的玻璃棒蘸溶液滴在试纸上,并与标准比色卡对照 |


科目:高中化学 来源: 题型:
| A、在硫氢化钠溶液中加入稀硫酸溶液:S2-+2H+→H2S↑ |
| B、用氢氧化钠溶液除去镁粉中的铝粉:2Al+2OH-→AlO2-+H2↑ |
| C、向碳酸氢钠溶液中加入少量氢氧化钙溶液:2HCO3-+Ca2++2OH-→CaCO3↓+CO32-+2H2O |
| D、偏铝酸钠溶液中通入少量二氧化碳:2AlO2-+CO2+3H2O→2Al(OH)3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蔗糖水解只生成葡萄糖 |
| B、含有碳碳双键的有机物均存在顺反异构现象 |
| C、向混有苯酚的苯中加入金属Na有无色气体生成 |
| D、用酸性高锰酸钾溶液检验CH2=CHCHO中是否含有醛基放电充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
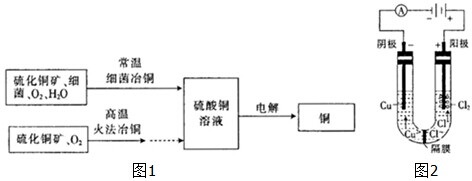
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=+890kJ/mol |
| B、CH4+2O2═CO2+2H2O△H=-890kJ/mol |
| C、CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ/mol |
| D、CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com