
 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:


 2H2O+O2↑
2H2O+O2↑ 2H2O+O2↑
2H2O+O2↑查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 高温高压 |
| 催化剂 |
| ||
| 高温高压 |
| 催化剂 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
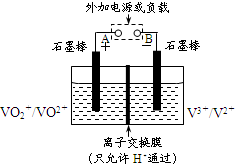 全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能的相互转化,其原理如图所示.(已知V2+呈紫色,V3+呈绿色;VO2+呈蓝色,VO2+呈黄色.溶液中c(H+)=2.0mol/L,阴离子为SO42-.)
全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能的相互转化,其原理如图所示.(已知V2+呈紫色,V3+呈绿色;VO2+呈蓝色,VO2+呈黄色.溶液中c(H+)=2.0mol/L,阴离子为SO42-.)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com