
科目:高中化学 来源: 题型:选择题

| A. | 反应物的总键能量低于生成物的总键能 | |
| B. | 该反应是放热反应 | |
| C. | 当A的正反应速率与C的逆反应速率相同时处于平衡状态 | |
| D. | 当A、B、C、D的浓度相同时,反应处于平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将0.l mol•L-1醋酸溶液加水稀释,溶液中所有离子的浓度都减小 | |
| B. | 0.1 mol/L的一元弱酸HA加水稀释过程中,$\frac{c({A}^{-})}{c(HA)•c(O{H}^{-})}$ 不变 | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 | |
| D. | 中和10 mL 0.1mol•L-1醋酸与中和100 mL 0.01mol•L-1的醋酸所需同种碱液的量不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “水乳交融,火上浇油”前者包含物理变化,而后者包含化学变化 | |
| B. | “曾青得铁化为铜”发生了化学变化 | |
| C. | “滴水石穿、绳锯木断”不包含化学变化 | |
| D. | “卤水点豆腐,一物降一物”的前半句话与胶体知识有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
| 离子 | Cu2+ | Al3+ | NO3- | Cl- |
| 物质的量浓度/ (mol•L-1) | 2 | 1 | 4 | x |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
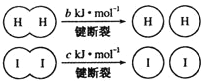
| A. | 向密闭容器中加入1 mol H2(g)和2mol I2(g),充分反应后放出的热量有可能等于a kJ | |
| B. | 反应物的总能量低于生成物的总能量 | |
| C. | 断开2 mol H-I键所需能量约为(c+b+a)kJ | |
| D. | 断开1 mol I-I键的同时形成2mol H-I键,说明反应已达到平衡状态 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com