
【题目】完成下列反应方程式,有机物必须写结构简式,并配平,有特殊条件注明条件.
(1)实验室制备乙炔
(2)淀粉水解
(3)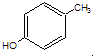 对甲基苯酚与溴水反应
对甲基苯酚与溴水反应
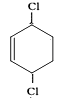
(4)![]() 环已二烯与氯气1,4加成
环已二烯与氯气1,4加成
(5)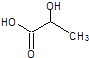 乳酸自酯化生成六元环状有机物
乳酸自酯化生成六元环状有机物
(6)军事工业生产TNT烈性炸药 .
【答案】
(1)CaC2+2H2O→Ca(OH)2+CH≡CH↑
(2)(C6H10O5)n+nH2O ![]() n C6H12O6
n C6H12O6
(3)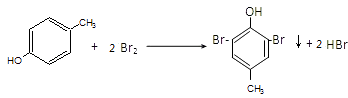
(4)![]() +Cl2
+Cl2 ![]()
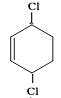
(5)CH3CH(OH)COOH ![]()
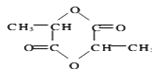 +2H2O
+2H2O
(6)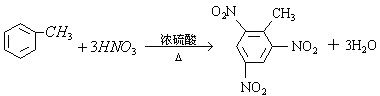
【解析】解:(1.)实验室制备乙炔,利用碳化钙与水反应生成乙炔、氢氧化钙,反应为CaC2+2H2O→Ca(OH)2+CH≡CH↑,所以答案是:CaC2+2H2O→Ca(OH)2+CH≡CH↑;
(2.)淀粉在酸性环境下水解的最终产物是葡萄糖,化学方程式为:(C6H10O5)n+nH2O ![]() n C6H12O6 , 所以答案是:(C6H10O5)n+nH2O
n C6H12O6 , 所以答案是:(C6H10O5)n+nH2O ![]() n C6H12O6;
n C6H12O6;
(3.)对甲基苯酚与浓溴水反应,是苯酚分子中羟基对苯环影响,邻位氢原子活泼,易于取代,反应的化学方程式为 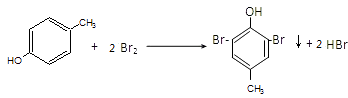 ,
,
所以答案是: 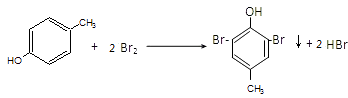 ;
;
(4.) ![]() 环已二烯与氯气1,4加成,生成3,6﹣二氯环己烯,反应方程式为:
环已二烯与氯气1,4加成,生成3,6﹣二氯环己烯,反应方程式为: ![]() +Cl2
+Cl2 ![]()
 ,所以答案是:
,所以答案是: ![]() +Cl2
+Cl2 ![]()
 ;
;
(5.)乳酸[CH3CH(OH)COOH]含有羟基和羧基两种官能团,所以乳酸能够在浓硫酸作用下生成六元环状化合物,反应的化学反应方程式为:CH3CH(OH)COOH ![]()
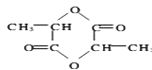 +2H2O,所以答案是:CH3CH(OH)COOH
+2H2O,所以答案是:CH3CH(OH)COOH ![]()
 +2H2O;
+2H2O;
(6.)甲苯在浓硫酸作用下可与浓硝酸反应生成TNT,反应的化学方程式为 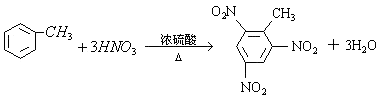 ,
,
所以答案是: 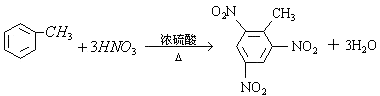 .
.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.摩尔是含有6.02×1023个微粒的集体
B.0.012kg12C所含的原子数精确值是6.02×1023
C.1molH2SO4的质量是98g
D.1molH2的体积为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由基本有机化工原料A(C2H2)制备有机物D和聚异戊二烯的合成路线如图所示: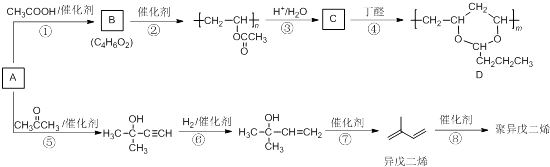
完成下列填空:
(1)上述转化步骤中与反应①的反应类型相同的是(填编号).
(2)m与n的关系为 .
(3)异戊二烯分子中最多有个原子共平面.
(4)在异戊二烯的同分异构体中,与A具有相同官能团且分子中有支链的有机物的名称是 .
(5)参照流程图中异戊二烯的合成路线,若把步骤⑤中的反应物丙酮改为乙醛,则经过反应⑤、⑥、⑦后得到的有机物是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列叙述正确的是
①lmolCH3CH2C(CH3)3所含甲基个数为4NA
②2.8g乙烯和2.8g聚乙烯中含碳原子数均为0.2NA
③1.0L1.0mol/LCH3COOH溶液中,CH3COOH分子数为NA
④8.8g乙酸乙酯中含共用电子对数为1.4NA
⑤标准状况下,22.4L乙醇完全燃烧后生成CO2的分子数为2NA
⑥常温常压下,17g甲基(一14CH3)所含的中子数为9NA
⑦标准状况下,11.2L氯仿中含有C—Cl键的数目为1.5NA
⑧lmolC15H32分子中含碳碳键数目为14NA
A.①③⑤⑦ B.①②④⑧ C.②③⑥⑧ D.①②⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.化工工业中常用乙苯脱氢的方法制备苯乙烯.
已知某温度下:
反应①:CO2(g)+H2(g)→CO(g)+H2O(g),△H=+41.2kJ/mol;
反应②: ![]() (g)→
(g)→ ![]() (g)+H2(g),△H=+117.6kJ/mol;
(g)+H2(g),△H=+117.6kJ/mol;
①②的化学反应平衡常数分别为K1、K2 ,
(1)请写出二氧化碳氧化乙苯制备苯乙烯的热化学反应方程式
该反应的化学平衡常数K=(用K1、K2表示)
(2)恒温恒容条件下,反应①达到平衡后;t1时刻通入少量CO2;请在图中画出t1之后的正逆反应曲线,并作出标注. 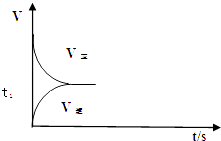
(3)Ⅱ.一定的条件下,合成氨反应为:N2(g)+3H2(g)2NH3(g).图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线.图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响. 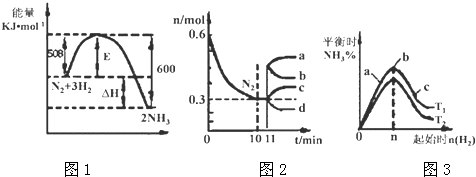
升高温度,该反应的平衡常数(填“增大”或“减小”或“不变”).
(4)由图2信息,计算10min内该反应的平均速率v(H2)= , 从11min起其它条件不变,压缩容器的体积,则n(N2)的变化曲线为(填“a”或“b”或“c”或“d”)
(5)图3 a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是点,温度T1T2(填“>”或“=”或“<”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气在生产和科研中有重要应用。
(1)若发生大量氯气泄漏事故,下列措施中正确的是__________。
a. 立即通报相关部门,迅速撤离事故现场
b. 用蘸有NaOH溶液的毛巾捂住口鼻
c. 逆风疏散
d. 顺风疏散
(2)事故发生后,可用NaOH稀溶液处理泄漏的氯气,反应的离子方程式是__________。
(3)某学生用下图装置制备氯气并与潮湿的![]() 反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:
反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:
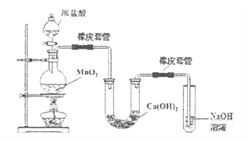
①圆底烧瓶中发生反应的化学方程式是__________。
②此实验结果所得![]() 产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
i温度较高时氯气与![]() 反应生成
反应生成![]() ,为避免此副反应的发生,可采取的措施是___________。
,为避免此副反应的发生,可采取的措施是___________。
ii试判断另一个副反应(写出此反应方程式):___________。为避免此副反应发生,应采取的措施是____________。
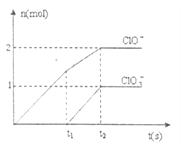
(4)在一定量的NaOH溶液中通入一定量![]() ,二者恰好完全反应。生成物中含有
,二者恰好完全反应。生成物中含有![]() 、
、![]() 、
、![]() 三种含氯元素的离子,其中
三种含氯元素的离子,其中![]() 、
、![]() 两种离子的物质的量(n)与反应时间(t)的曲线如下图所示。则
两种离子的物质的量(n)与反应时间(t)的曲线如下图所示。则![]() 时被氧化的氯元素和被还原的氯元素质量之比为__________。
时被氧化的氯元素和被还原的氯元素质量之比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己烯醛(D)是一种重要的合成香料,下列合成路线是制备D的方法之一,根据该合成路线回答下列问题: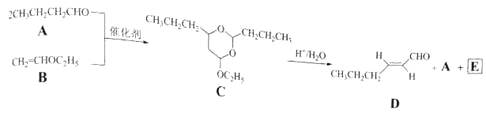
已知 ![]()
![]() RCHO+R′OH+R″OH
RCHO+R′OH+R″OH
(1)A的名称是;B分子中的共面原子数目最多为;C分子中与环相连的三个基团中,不同化学环境的氢原子共有种.
(2)D中含氧官能团的名称是 . 写出检验该官能团的化学反应方程式: .
(3)E为有机物,能发生的反应有:
a.聚合反应 b.加成反应 c.消去反应 d.取代反应
(4)B的同分异构体F与B有完全相同的官能团,写出F所有可能的结构:
(5)以D为主要原料制备己醛(目标化合物),在方框中将合成路线的后半部分补充完整.
(6)问题(5)的合成路线中的第一步反应的目的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学史上每一次重大发现都极大的推进了科学的发展,俄国科学家门捷列夫对化学的突出贡献在于( )
A.提出了元素周期律
B.开发了合成氨的生产工艺
C.揭示了燃烧的本质
D.提取了治疟药物青蒿素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2.0mol PCl3和1.0mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3+Cl2PCl5 . 达平衡时,PCl5为0.40mol,如果此时移走1.0mol PCl3和0.50mol Cl2 , 在相同温度下再达平衡时PCl5的物质的量是( )
A.0.40mol
B.0.20mol
C.小于0.20mol
D.大于0.20mol,小于0.40mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com