
【题目】A、B、C、D均为中学化学常见物质,且均含有同一种元素,其中A是单质,它们之间存在如图转化关系
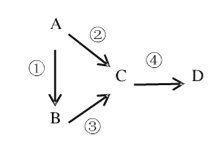
Ⅰ.若D是红棕色气体;B气体溶于水后,溶液为碱性。
(1)请写出A的化学式__________,反应③的化学反应方程式为_____________。
(2)D溶于水形成的稀溶液与铜反应的离子方程式为__________,该反应的实验现象为____________(写出两条)。
Ⅱ若B、D既能与强酸溶液反应,又能与强碱溶液反应,反应②③均为强酸条件。
(1)反应④可以通过滴加氨水实现,该反应的离子方程式为____________。
(2)请写出A用于焊接铁轨的化学方程式________________。
【答案】N2 4NH3 + 5O2 ![]() 4NO + 6H2O 3Cu + 8H+ + 2NO3- = 3Cu2+ + 2NO↑ + 4H2O 红色固体溶解、溶液变为蓝色、有无色气泡生成、在试管口有红棕色气体生成 Al3+ + 3NH3·H2O = Al(OH)3↓+ 3NH4+ 2Al + Fe2O3
4NO + 6H2O 3Cu + 8H+ + 2NO3- = 3Cu2+ + 2NO↑ + 4H2O 红色固体溶解、溶液变为蓝色、有无色气泡生成、在试管口有红棕色气体生成 Al3+ + 3NH3·H2O = Al(OH)3↓+ 3NH4+ 2Al + Fe2O3 ![]() Al2O3 + 2Fe
Al2O3 + 2Fe
【解析】
根据题干中部分物质的性质及图示中给出的转化关系推测各物质的组成,进而书写相关化学方程式及离子方程式。
Ⅰ.根据图示的转化关系,若D是红棕色气体,则D为二氧化氮;B气体溶于水后,溶液为碱性,则B为氨气;A为单质,则A为氮气;C为一氧化氮;
(1)A的化学式N2,反应③的化学反应方程式为4NH3 + 5O2 ![]() 4NO + 6H2O;
4NO + 6H2O;
(2)D溶于水形成的稀溶液为硝酸,与铜反应的离子方程式为3Cu + 8H+ + 2NO3- = 3Cu2+ + 2NO↑ + 4H2O,该反应的实验现象为红色固体溶解、溶液变为蓝色、有无色气泡生成、在试管口有红棕色气体生成;
故答案为:N2 ; 4NH3 + 5O2 ![]() 4NO + 6H2O;3Cu + 8H+ + 2NO3- = 3Cu2+ + 2NO↑ + 4H2O;红色固体溶解、溶液变为蓝色、有无色气泡生成、在试管口有红棕色气体生成;
4NO + 6H2O;3Cu + 8H+ + 2NO3- = 3Cu2+ + 2NO↑ + 4H2O;红色固体溶解、溶液变为蓝色、有无色气泡生成、在试管口有红棕色气体生成;
Ⅱ若B、D既能与强酸溶液反应,又能与强碱溶液反应,结合图示中转化关系,则推测A为铝,B为氧化铝,C为铝盐,D为氢氧化铝;
(1)反应④离子方程式为Al3+ + 3NH3·H2O = Al(OH)3↓+ 3NH4+;
(2)A用于焊接铁轨的化学方程式为:2Al + Fe2O3 ![]() Al2O3 + 2Fe,
Al2O3 + 2Fe,
故答案为:Al3+ + 3NH3·H2O = Al(OH)3↓+ 3NH4+;2Al + Fe2O3 ![]() Al2O3 + 2Fe。
Al2O3 + 2Fe。


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
【题目】已知碳碳单键可以绕键轴自由旋转,结构简式为如下图所示的烃,下列说法中正确的是( )

A. 分子中处于同一直线上的碳原子最多有6个
B. 分子中至少有12个碳原子处于同一平面上
C. 该烃苯环上的一氯代物共有 3种
D. 该烃苯环上一氯代物共有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)系统命名: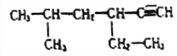 的名称为:_______________________。
的名称为:_______________________。
(2)![]() 的键线式:_____________________________。
的键线式:_____________________________。
(3)下列关于糖类的说法正确的是_______。(填标号)
a.糖类都有甜味,具有CnH2mOm的通式
b.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
c.用银镜反应不能判断淀粉水解是否完全
d.淀粉和纤维素都属于多糖类天然高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由乙烯和其他无机原料合成环状酯E和高分子化合物H的示意图如下所示:
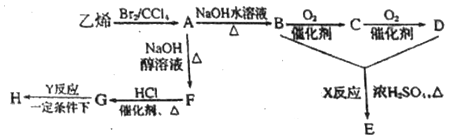
请回答下列问题:
(1)写出以下物质的结构简式:A____________,H_____________,C的化学名称_____________。
(2)写出以下反应的反应类型:X_____________,Y_______________。
(3)写出以下反应的化学方程式:
A→B:___________________________________________;
G→H:_________________________________。
B+D→E:________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下,足量的铝分别与下列酸反应时,放出H2最多的是 ( )
A. 600 mL 18.4mol·L-1的硫酸 B. 100 mL 1.0mol·L-1的盐酸
C. 200 mL 12 mol·L-1的浓硝酸 D. 600mL 0.1 mol·L-1的硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知:N2(g)+3H2(g)![]() 2NH3(g)ΔH=﹣92.4 kJ
2NH3(g)ΔH=﹣92.4 kJ![]() ,
,
2H2(g)+O2(g)====2H2O(l)ΔH=﹣571.6 kJ![]() ,
,
则2N2(g)+6H2O(l)![]() 4NH3(g)+3O2(g) ΔH=_______。
4NH3(g)+3O2(g) ΔH=_______。
(2)20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量过渡态。分析图中信息,回答下列问题:
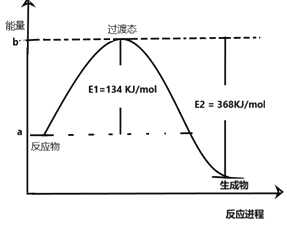
上图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出CO2和NO反应生成NO2和CO的热化学方程式:__________________________________。在反应体系中加入催化剂,E1和E2的变化是:E1__,E2__(填“增大”“减小”或“不变”),对反应热是否有影响?__(填“是”或“否”),原因是________________________________________。
(3)常温常压下断裂1 mol气体分子化学键所吸收的能量或形成1 mol气体分子化学键所放出的能量称为键能(单位为kJ·mol-1)。下表是一些键能数据(kJ·mol-1):请完成下列问题。
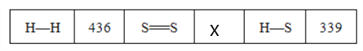
热化学方程式2H2(g)+S2(g)===2H2S(g) ΔH=-229 kJ·mol-1,则X=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类正确的是
碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
A | Na2CO3 | H2SO4 | NaOH | SO2 | CO2 |
B | NaOH | HCl | NaCl | Na2O | CO |
C | NaOH | CH3COOH | CaF2 | CO | SO2 |
D | KOH | HNO3 | CaCO3 | CaO | SO2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是向MgCl2和AlCl3的混合溶液中加入一定量NaOH溶液,紧接着再加入一定量稀盐酸,生成沉淀的物质的量y与加入溶液的体积x的关系图。根据图示判断,下列结论中不正确的是

A. N点时溶液中的溶质只有NaCl
B. M点之前加入的是NaOH溶液,M点之后加入的是盐酸
C. c(NaOH)=c(HCl)
D. 原混合溶液中c(MgCl2)∶c(AlCl3)=1∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com