
��������п��һ�ֶ���Ե����������ϣ��������СԼ��1-100���ס�ij����ұ���о�������ʪ��ѧ��(NPP-��)�Ʊ�������������п�����ø��ֺ�п����Ϊԭ�ϣ����������п��������ξ�����ȥԭ���е����ʣ�Ȼ�������ü�ʽ̼��п������û�������п����ѧ�����������£�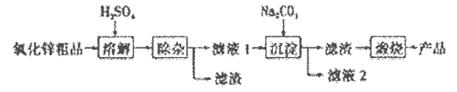
��1��ͨ��__________����������ƣ����Լ�����������Һ2�к���Na����
��2������������ͼ��Na2CO3��Һ��pH��12������˵����ȷ����___________��
A����Һ��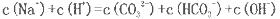
B������Һ��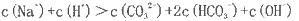
C������Һ��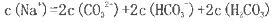
D����������Һϡ����100������pH��10��
��3�����ܽ⡱��õ���������Һ�к���Zn2����SO42����������Fe2����Cu2�������ʡ�ȡ0.5L����Һ�ȼ���___________���Na2CO3����H2SO4����������Һ��pH��5.4��Ȼ���������KMnO4��Fe2��ת��ΪFe(OH)3��ͬʱKMnO4ת��ΪMnO2���������Һ��Fe2����Ũ��Ϊ0 009 mol/L�������Һ������Ӧ����_______molKMnO4 .
��1����ɫ��Ӧ��2��BC��3��Na2CO3��0.0015
���������������ʵ�����̿�֪����п����Ϊԭ�ϣ������������п�����˳��ӣ��õ���Һ�к�п���ӣ�������Na2CO3��Һ��Ӧ���ɼ�ʽ̼��п������û�������п����1��Na����ɫΪ��ɫ���������Һ�к���Na+��������ɫ��Ӧ����2�����ݵ���غ�֪B��ȷ�����������غ�֪C��ȷ����Ϊ̼����ˮ���Լ��ԣ�ϡ��ʱ�ٽ�ˮ�⣬��������Ũ�ȱ仯С��100����pH��10��D����3��Fe2+��Cu2+�����ʣ�������̼���Ʒ�Ӧ������KMnO4��Fe2+ת��ΪFe��OH��3���ɵ����غ���㡣
���㣺�������ӵļ��顢��Һ������Ũ�ȹ�ϵ��������ԭ�����֪ʶ��


 ���ſ����ϵ�д�
���ſ����ϵ�д� ���Ŀ����ϵ�д�
���Ŀ����ϵ�д� ������ӱ������ͯ������ϵ�д�
������ӱ������ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��Ӧ�ٺ͢ڷֱ��ǴӺ���Һ�ij�ֿ�ʯ����ȡ�����Ҫ��Ӧ��
��2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2
��2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2������˵����ȷ����
| A��������Ӧ�о�Ϊ��Ԫ�ر����� |
| B����Ԫ���ڷ�Ӧ���б���ԭ���ڷ�Ӧ���б����� |
| C�������ԣ�MnO2>SO42->IO3->I2 |
| D����Ӧ�١��������ɵ�����I2ʱת�Ƶ�������Ϊ1�U5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�ж������йػ�ѧ���������������ȷ����
| A�����壺������ʵ�ֱ���Ƿ���1nm��100nm֮�� |
| B��������ԭ��Ӧ����Ӧǰ��Ԫ�صĻ��ϼ��Ƿ����˱仯 |
| C�����ۻ������ɻ������Ԫ���Ƿ�ȫ�����Ƿǽ���Ԫ�� |
| D����ѧ�仯���Ƿ�����ЧӦ����ɫ�仯�������������ɵ�����ʵ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��8�֣���0��08mol KMnO4���壨����Ϊ12��64g������һ��ʱ����ռ���a molO2����Ӧ������Ĺ����м���������Ũ���ᣬ���ռ���b molCl2����ʱMnԪ��ȫ����Mn2+����ʽ��������Һ�С�
��1������ƽ���з���ʽ��
KMnO4+ HCl �� KCl+ MnCl2+ Cl2��+ H2O
��2����ʽ��Ӧ�еĻ�ԭ���� ������ԭ��ʧȥ1mol����ʱ��������������ʵ���Ϊ ��
��3��a +b�����ֵΪ ��a +b��СֵΪ ��
��4���� a +b ��0��18ʱ���������������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��16�֣�MnO2���������KOH��KClO3�ڸ����·�Ӧ����������أ�K2MnO4����KCl��K2MnO4��Һ���ữ��ת��ΪMnO2��KMnO4��һ��MnO2�Ʊ�KMnO4�ķ������£�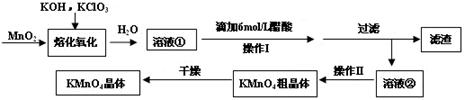
��1��д�����ܻ��������Ļ�ѧ��Ӧ����ʽ�� ��
��2������Һ���еõ�KMnO4�־���ķ����� ��
��3�����������п���ѭ��ʹ�õ������� ��
��4�������ϣ����������Ʊ������е���ʧ������ѭ����1mol MnO2���Ƶ� mol KMnO4��
��5����֪293Kʱ����ص��ܽ��Ϊ217g������ص��ܽ��Ϊ11.1g��������ữ�����в��ô��������������������ԭ��
�ٲ����������ԭ�� ��
�ڲ����������ԭ�� ��
��6���������������Ʊ�KMnO4���ʲ����ߣ�Ϊ��߲��ʣ������Բ����������ַ�����
����K2MnO4��Һ��ͨ��������д���÷�Ӧ�����ӷ���ʽ ��
�ڵ��K2MnO4��Һ�������ܷ�Ӧ���ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��14�֣�����һ��ʮ����Ҫ����ɫ����,��������һ�㺬��Fe��Cu�������ᡢ����Һ��Ӧ�IJ��������ʶ�Ӱ��ʹ�á��ֶԴ��������ᴿ������ķ�Ӧ�������£�
��֪��
��2Ni2O3(��ɫ)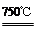 4NiO(����ɫ) + O2��
4NiO(����ɫ) + O2��
��
| ���� | CuS | Cu(OH)2 | Ni(OH)2 | NiS |
| Ksp | 8.8��10��36 | 2.2��10��20 | 5.48��10-16 | 3.2��10-19 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
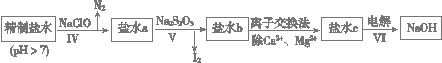
(14��)���ռ�������ˮ�����ξ��ơ���һ�ξ�����Ҫ���ó�������ȥ����ˮ��Ca2����Mg2����SO42�������ӣ��������£�
��. �����ˮ�м������BaCl2��Һ�����ˣ�
��. ��������Һ�м������Na2CO3��Һ�����ˣ�
��. ��Һ���������pH����õ�һ�ξ�����ˮ��
��1�����̢��ȥ��������______��
��2�����̢����ɵIJ��ֳ��������ܽ��(20 ��/g)���±��������ݱ������ݽ����������⣺
| CaSO4 | Mg2(OH)2CO3 | CaCO3 | BaSO4 | BaCO3 |
| 2.6��10��2 | 2.5��10��4 | 7.8��10��4 | 2.4��10��4 | 1.7��10��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(15��)2012��4��15�գ������ع�ӱ�һҩ�ý��ҳ���Ƥ�����������������ԭ�ϡ���Щ��ҵ����ʯ�Ҵ���Ƥ����Ͻ�����ɫƯ����ϴ������Ƴɹ�ҵ�����������㽭�²���ҩ�ý���������ҵ����������ҩƷ��ҵ�����������߸��С����ߵ��鷢��9��ҩ����13������ҩƷ���ý����ؽ������������ꡣ�ظ������׳ƺ췯��(Na2Cr2O7��2H2O)����Ҫ�Ļ�����Ʒ��ǿ����������ҵ�Ʊ����������£�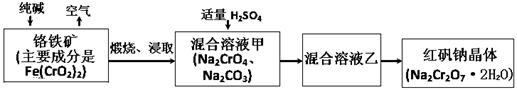
��1����ѧ�Ͽɽ�ijЩ��д�����������ʽ����Na2SiO3��д��Na2O��SiO2����Fe(CrO2)2��д�� ��
��2�����ո�����ʱ����ʯ�����ܵ�Fe(CrO2)2���ɿ�����ˮ��Na2CrO4����Ӧ��ѧ����ʽ���£�4Fe(CrO2)2+8Na2CO3+7O2 = 2Fe2O3+8Na2CrO4+8CO2Ϊ�˼ӿ�÷�Ӧ�ķ�Ӧ���ʣ��ɲ�ȡ�Ĵ�ʩ�� ����дһ�ּ��ɣ�
��3����֪CrO42-�ڲ�ͬ��������Һ���в�ͬ�ķ�Ӧ���磺2CrO42-+2H+= Cr2O72-+H2O ;
3CrO42-+4H+= Cr3O102-+2H2O �� �������Һ���м����������������ԭ���� ��
�� �����Һ�������ʵĻ�ѧʽ�� ��
��4���ں�Cr2O72-��ˮ�д�����ƽ�⣺Cr2O72-+H2O  2CrO42-+2H+����д����ƽ���ƽ�ⳣ������ʽK= ����������ˮϡ�ͣ�ƽ�⽫ �ƶ�(���������������)��
2CrO42-+2H+����д����ƽ���ƽ�ⳣ������ʽK= ����������ˮϡ�ͣ�ƽ�⽫ �ƶ�(���������������)��
��5������ƽ������Һ��ԭ���з��������ӷ�Ӧ����Cr2O72-+��S2-+��H2O - ��Cr(OH)3+��S2O32-+��OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(1)��ⱥ��ʳ��ˮ֮ǰʳ��ˮ��Ҫ���ƣ�Ŀ���dz�ȥ�����е�Ca2����Mg2����SO42�����������ӣ�ʹ�õ��Լ��Ͳ�����a.Na2CO3��Һ��b.Ba(OH)2��Һ��c.ϡ���ᣬd.���ˣ�������ļ���˳��Ϊ________(����ĸ����)��
(2)��ⱥ��ʳ��ˮʱ���ӽ���Ĥ��������_____________________________
(3)��ⱥ��ʳ��ˮʱ��������ݻ�Ϊ10 L�����ӽ���Ĥ�����У�1 min�������ɲ���11.2 L(��״��)Cl2����ʱ��Һ��pH��(�����ά�ֲ���)________��
(4)Cl2����������ˮ��ɱ������������һ������������ClO2����������ɱ�������л�ԭ�����ΪCl������������������ˮ������Cl2��ClO2�����ʵ���֮��Ϊ________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com