
H2S废气资源化利用途径之一是回收能量并得到单质硫。反应原理为:2H2S(g) + O2(g) = S2(s) + 2H2O(l)  H=-632kJ·mol-1。右图为质子膜H2S燃料电池的示意图。下列说法正确的是
H=-632kJ·mol-1。右图为质子膜H2S燃料电池的示意图。下列说法正确的是
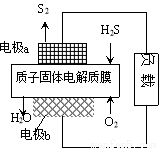
A.电极a为电池的正极
B.电极b上发 生的电极反应为:O2+2H2O+4e
生的电极反应为:O2+2H2O+4e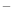 = 4 OH
= 4 OH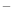
C.电路中每流过4mol电子,电池内部释放632kJ热能
D.每17gH2S参与反应,有1mol H+经质子膜进入正极区
 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源:2015-2016学年宁夏银川第九中学高二上学期期中测试化学试卷(解析版) 题型:选择题
密闭容器中,用等物质的量A和B发生如下反应:A(g)+2B(g)  2C(g),反应达到平衡时,若混合气体中A和B的物质的量之和与C的物质的量相等,则这时A的转化率为
2C(g),反应达到平衡时,若混合气体中A和B的物质的量之和与C的物质的量相等,则这时A的转化率为
A.70% B.60% C.50% D.40%
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省高一上学期期中测试化学试卷(解析版) 题型:填空题
某待测液中可能含有大量Mg2+、Cu2+、Fe3+、K+、H+、NO3-、OH-离子中的一种或几种,现通过以下实验进行检验:
(1)取少量待测液,仔细观察,呈无色;
(2)向上述待测液中滴加NaOH溶液,先无明显现象,后有白色沉淀生成,
(3)向上述溶液中加入BaCl2溶液,无现象。
据此可以判断该待测液中一定大量存在的离子是 ,一定不能大量存在的离子是 ,不能确定是否存在的离子是 ,依次写出(2)中加入氢氧化钠后的离子反应: , 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二上学期期中测试化学试卷(解析版) 题型:选择题
三氧化二镍 (Ni2O3)可用于制造高能电池,其电解法
(Ni2O3)可用于制造高能电池,其电解法 制备过程如下:用NaOH调NiCl2溶液pH至7.5,加入适量硫酸钠后进行电解。电解过程中产生的Cl2 在弱碱性条件下生成ClO-,把二价镍氧化为三价镍。以下说法正确的是
制备过程如下:用NaOH调NiCl2溶液pH至7.5,加入适量硫酸钠后进行电解。电解过程中产生的Cl2 在弱碱性条件下生成ClO-,把二价镍氧化为三价镍。以下说法正确的是
A.可用铁作为阳极材料
B.电解过程中阳极附近溶液的pH升高
C.阳极反应方程式为:2Cl- -2e-===Cl2↑
D.1 moL 二价镍全部转化为三价镍时,外电路中通过了0.5 moL电子
查看答案和解析>>
科目:高中化学 来源:2016届福建省四地六校高三上学期第二次联考化学试卷(解析版) 题型:选择题
下列有关物质的应用与性质相对应的说法正确的有几个
 ①明矾能用于净水是因为铝离子水解生成的氢氧化铝胶体具有强氧化性
①明矾能用于净水是因为铝离子水解生成的氢氧化铝胶体具有强氧化性
②氯化铁溶液可用于制作印刷电路板是因为其能氧化单质铜
③浓硫酸可用作干燥剂是因为其具有脱水性
④光导纤维可用作通讯材料是因为其具有导电性
⑤MgO、Al2O3的熔点很高,可制作耐高温材料
⑥NaHCO3能与碱反应,因此食品工业上用作焙制糕点的膨松剂
⑦Al具有良好的延展性和抗腐蚀性,可制成铝箔包装物品
A.3个 B.2个 C.5个 D.4个
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二上学期期中测试化学试卷(解析版) 题型:选择题
下列事实,不能用勒夏特列原理解释的是
A.实验室常用排饱和食盐水的方法收集氯气
B.工业合成氨控制温度在较高温度(500℃)进行
C.在浓氨水中加入烧碱可用于实验室快速生氨
D.工业上将二氧化硫转化为三氧化硫常通入过量空气
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省宜昌市高二上期中测试化学试卷(解析版) 题型:选择题
下列变化过程,属于放热反应的是
① 水蒸气变成液态水 ② 生石灰与水反应
③ 浓H2SO4稀释 ④ 醋酸电离
⑤ Na投入水中 ⑥ 反应物的键能总和小于生成物的键能总和
A、②③④⑤ B、②⑤⑥
C、②③④ D、①②⑤⑥
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期第二次月考化学试卷(解析版) 题型:推断题
下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是由第三周期元素组成的单质中熔点最高的金属, K是一种红棕色气体。

请填写下列空白:
(1) 在周期表中,组成单质I的元素位于第__________周期_________族。
(2) 在反应⑦中氧化剂与还原剂的物质的量之比为___________________。
(3) 在②、③、⑥、⑨中既属于化合反应又属于非氧化还原反应的是__________(填序号)
(4) 反应④的离子方程式是__________________________________。
(5) 将化合物D与KNO3、KOH共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾), 同时还生成KNO2和H2O。该反应的化学方程式是 _________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省太原市高一上学期阶段测化学试卷(解析版) 题型:实验题
右图为某浓盐酸试剂瓶标签上的部分内容,请回答下列问题。

(1)该浓盐酸中HCl 的物质的量浓度为 mol/L;
(2)某同学欲用此浓盐酸和蒸馏水配置480mL 浓度为0.4mol/L 的稀盐酸。
①配置稀盐酸时,可供选用的仪器有:
A胶头滴管 B玻璃棒 C烧杯 D药匙 E量筒 F托盘天平 G容量瓶
完成该实验所需的仪器是 (填序号),期中所需G 的规格是 mL;
②操作步骤包括:计算、 、稀释、转移、 、定容、摇匀,此过程中玻璃棒的作用是 、 ;
③实验结束后,发现所配置的溶液浓度偏小,可能的原因是 (填序号)。
A.配置前容量瓶中有少量水
B.定容时仰视观察液面
C.摇匀后液面下降,又加入少量水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com