
ЁОЬтФПЁПNaClO2 ЪЧвЛжжживЊЕФЩБОњЯћЖОМСЃЌвВГЃгУРДЦЏАзжЏЮяЕШЃЌвЛжжЩњВњNaClO2 ЕФЙЄвеШчЯТЃК
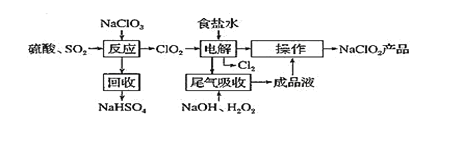
вбжЊЃКЂйClO2ЪЧвЛжжЧПбѕЛЏадЦјЬхЃЌХЈЖШДѓЪБвзЗжНтБЌеЈЁЃдкЩњВњЪЙгУЪБвЊгУЯЁгаЦјЬхЛђПеЦјЕШНјааЯЁЪЭЃЌЭЌЪББмУтЙтееЁЂе№ЖЏЕШЁЃЂкNaClO2БЅКЭШмвКдкЮТЖШЕЭгк38ЁцЪБЮіГіЕФОЇЬхЪЧNaClO2ЁЄ33H2OЃЌИпгк38ЁцЪБЮіГіЕФОЇЬхЪЧNaClO2ЃЌИпгк60ЁцЪБNaClO2ЗжНтГЩNaClO3КЭNaClЁЃЛиД№ЯТСаЮЪЬтЃК
(1)зюНќПЦбЇМвгждкЁАЗДгІЁБВНжшЕФЛљДЁЩЯбаОПГігУH2C2O4ДњЬцSO2жЦБИClO2ЕФаТЗНЗЈЃЌИУЗНЗЈЕФЛЏбЇЗНГЬЪНЮЊ______________________ЁЃ
(2)ЛёЕУВњЦЗNaClO2ЕФЁАВйзїЁБАќРЈвдЯТВНжшЃК
ЂйМѕбЙЃЌ55ЁцеєЗЂНсОЇЃЛЂкГУШШЙ§ТЫЃЛЂл___________________________ЂмЕЭгк60ЁцИЩдяЃЌЕУЕНВњЦЗЁЃ
(3)ЮЊСЫВтЖЈВњЦЗNaClO2ЕФДПЖШЃЌШЁЩЯЪіЫљЕУВњЦЗ12.5gШмгкЫЎХфГЩ1LШмвКЃЌШЁГі10.00mLШмвКгкзЖаЮЦПжаЃЌдйМгШызуСПЫсЛЏЕФKIШмвКЃЌГфЗжЗДгІКѓ(ClO2ЃБЛЛЙдЮЊClЃдгжЪВЛВЮМгЗДгІ)ЃЌМгШы2~3ЕЮЕэЗлШмвКЃЌгУ0.25molLЉ1Na2S2O3БъзМвКЕЮЖЈЃЌДяЕНЕЮЖЈжеЕуЪБгУШЅБъзМвК20.00mLЃЌЪдМЦЫуВњЦЗNaClO2ЕФДПЖШ_________________________(ЬсЪОЃК2Na2S2O3+I2=Na2S4O6+2NaI)

(4)NaClO2ШмвКжаДцдкClO2ЁЂHClO2ЁЂClO2ЃЁЂClЃЫФжжКЌТШЮЂСЃЁЃОВтЖЈ 25ЁцИїКЌТШЮЂСЃХЈЖШЫц pH ЕФБфЛЏЧщПіШчЭМЫљЪО(ClЃУЛгаЛГі)
ЂйЫсадЬѕМўЯТNaClO2ШмвКжаДцдкClЃЕФдвђЪЧ_______________________(гУРызгЗНГЬЪННтЪЭ)ЁЃ
ЂкpH=5ЪБЃЌNaClO2ШмвКжаClO2ЁЂHClO2ЁЂClO2ЃЁЂClЃЫФжжКЌТШЮЂСЃЕФХЈЖШгЩДѓЕНаЁЕФЫГађЪЧ___________________________________________________ЁЃ
ЁОД№АИЁП2NaClO3+H2C2O4+H2SO4=Na2SO4+2H2O+2CO2Ёќ+2ClO2Ёќ гУ38Ёц~60ЁцЕФЮТЫЎЯДЕг 90.5% 5ClO2-+4H+![]() 4ClO2+Cl-+2H2O c(HClO2)>c(ClO2Ѓ)>c(ClO2)>c(ClЃ)
4ClO2+Cl-+2H2O c(HClO2)>c(ClO2Ѓ)>c(ClO2)>c(ClЃ)
ЁОНтЮіЁП
гЩжЦБИСїГЬПЩжЊЃЌNaClO3КЭSO2дкСђЫсЫсЛЏЕФЬѕМўЯТЗДгІЩњГЩClO2ЃЌЦфжаNaClO3ЪЧбѕЛЏМСЃЌЛиЪеВњЮяЮЊNaHSO4ЃЌЫЕУїЩњГЩСђЫсЧтФЦЃЌЧвЩњГЩClO2ЃЌИљОнЕчКЩЪиКуПЩЕУЗДгІЕФЗНГЬЪНЮЊ2NaClO3+SO2+H2SO4=2NaHSO4+2ClO2ЃЌбЁдёNaOHГ§ШЅЪГбЮЫЎжаЕФMg2+бЁдёЬМЫсФЦГ§ШЅCa2+ЃЌЕчНтзАжУжавѕМЋClO2ЕУЕчзгЩњГЩClO2-ЃЌбєМЋCl-ЪЇЕчзгЩњГЩCl2ЃЌКЌH2O2ЕФNaOHШмвКЮќЪеClO2ЃЌВњЮяЮЊClO2-ЃЌзюКѓNaClO2ШмвКНсОЇЁЂИЩдяЕУЕНВњЦЗЃЌвдДЫЗжЮізїД№ЁЃ
ЃЈ1ЃЉгУСђЫсЫсЛЏЕФВнЫсШмвКЛЙдТШЫсФЦЃЌЗДгІЩњГЩСђЫсФЦЁЂCO2ЁЂClO2КЭЫЎЃЌЗДгІЗНГЬЪНЮЊЃК2NaClO3+H2C2O4+H2SO4=Na2SO4+2H2O+2CO2Ёќ+2ClO2ЁќЃЌ
ЃЈ2ЃЉЛёЕУВњЦЗNaClO2ЃЌгЩЬтИЩаХЯЂПЩжЊгІгУ38Ёц~60ЁцЕФЮТЫЎЯДЕгЃЛ
ЃЈ3ЃЉNaClO2гызуСПЫсЛЏЕФKIШмвКЗДгІЃЌЗНГЬЪНЮЊЃКClO2-+4I-+4H+=2H2O+2I2+Cl-ЃЌдђИљОнЙиЯЕNaClO2~2I2~4S2O32-ПЩжЊNaClO2ЕФЮяжЪЕФСПЮЊ![]() =1.25ЁС10-3molЃЌ10mlбљЦЗжаm(NaClO2)= 1.25ЁС10-3molЁС90.5g/molЃЌвђДЫдбљЦЗжаNaClO2ЕФжЪСПЗжЪ§ЮЊ
=1.25ЁС10-3molЃЌ10mlбљЦЗжаm(NaClO2)= 1.25ЁС10-3molЁС90.5g/molЃЌвђДЫдбљЦЗжаNaClO2ЕФжЪСПЗжЪ§ЮЊ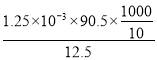 ЁС100%=90.5%ЃЛ
ЁС100%=90.5%ЃЛ
ЃЈ4ЃЉЂйЫсадШмвКжаNaClO2ЗЂЩњЦјЛЏЗДгІЩњГЩNaClКЭClO2ЃЌРызгЗНГЬЪНЮЊЃК5ClO2-+4H+![]() 4 ClO2+Cl-+2H2OЃЛ
4 ClO2+Cl-+2H2OЃЛ
ЂкгЩЭМЯѓПЩжЊЃЌpH=5ЪБЃЌЗЂЩњЕФЗДгІЮЊЃК5ClO2-+4H+![]() 4 ClO2+Cl-+2H2OЃЌNaClO2ШмвКжаКЌТШдЊЫиЕФЮЂСЃХЈЖШЕФДѓаЁЙиЯЕЮЊЃКc(HClO2)>c(ClO2Ѓ)>c(ClO2)>c(ClЃ)
4 ClO2+Cl-+2H2OЃЌNaClO2ШмвКжаКЌТШдЊЫиЕФЮЂСЃХЈЖШЕФДѓаЁЙиЯЕЮЊЃКc(HClO2)>c(ClO2Ѓ)>c(ClO2)>c(ClЃ)


 Н№ХЦПЮЬУСЗЯЕСаД№АИ
Н№ХЦПЮЬУСЗЯЕСаД№АИ Ш§аТПьГЕН№ХЦжмжмСЗЯЕСаД№АИ
Ш§аТПьГЕН№ХЦжмжмСЗЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЮТЖШЯТдк2LУмБеШнЦїжаМгШывЛЖЈСПAЃЌЗЂЩњвдЯТЛЏбЇЗДгІЃК
2A(g)![]() B(g)+C(g)ЃЛІЄH =Ѓ48.25 kJЁЄmolЃ1ЃЌЗДгІЙ§ГЬжаBЁЂAЕФХЈЖШБШгыЪБМфtгаЯТЭМЫљЪОЙиЯЕЃЌШєВтЕУЕк15minЪБc(B)=1.6 molЁЄLЃ1ЃЌЯТСаНсТле§ШЗЕФЪЧ
B(g)+C(g)ЃЛІЄH =Ѓ48.25 kJЁЄmolЃ1ЃЌЗДгІЙ§ГЬжаBЁЂAЕФХЈЖШБШгыЪБМфtгаЯТЭМЫљЪОЙиЯЕЃЌШєВтЕУЕк15minЪБc(B)=1.6 molЁЄLЃ1ЃЌЯТСаНсТле§ШЗЕФЪЧ
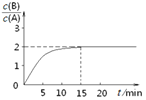
A.ИУЮТЖШЯТДЫЗДгІЕФЦНКтГЃЪ§ЮЊ3.2
B.AЕФГѕЪМЮяжЪЕФСПЮЊ4 mol
C.ЗДгІЕНДяЦНКтЪБЃЌЗХГіЕФШШСПЪЧ193kJ
D.ЗДгІДяЦНКтЪБЃЌAЕФзЊЛЏТЪЮЊ80%
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвЛЖЈЬѕМўЯТЃЌдкЬхЛ§ЮЊ10LЕФУмБеШнЦїжаЃЌ2molXКЭ2molYНјааШчЯТЗДгІЃК2X(g)+Y(g)Z(g)ЃЌО2minДяЕНЦНКтЃЌЩњГЩ0.6molZЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ
A.вдXХЈЖШБфЛЏБэЪОЕФЗДгІЫйТЪЮЊ0.06mol/(Lmin)
B.НЋШнЦїЬхЛ§БфЮЊ20LЃЌZЕФЦНКтХЈЖШЮЊдРДЕФ![]()
C.ЦНКтЪБЃЌXЕФзЊЛЏТЪЮЊ30%
D.Ц№ЪМзДЬЌКЭЦНКтЪБШнЦїФкЕФЦјЬхбЙЧПБШЮЊ2ЁУ1
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГбаОПадбЇЯАаЁзщЕФЭЌбЇЮЊдкЪЕбщЪвдйЯжЖўбѕЛЏСђДпЛЏбѕЛЏЕФЙ§ГЬЃЌВЂжЦШЁЩйСПШ§бѕЛЏСђОЇЬхЃЌЩшМЦСЫШчЭМЫљЪОЕФзАжУЁЃвбжЊШ§бѕЛЏСђгіЫЎЩњГЩСђЫсВЂЗХГіДѓСПШШЃЌШнвзаЮГЩЫсЮэЁЃЪдЛиД№ЃК
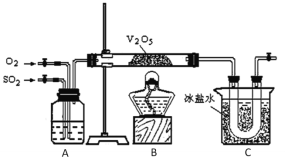
ЃЈ1ЃЉвбжЊ450ЁцЪБЃЌЗДгІ2SO2(g)ЃЋO2(g)![]() 2SO3(g)ЕФЦНКтГЃЪ§KЃН25ЃЌдђдк450ЁцЪБЃЌ2SO3(g)
2SO3(g)ЕФЦНКтГЃЪ§KЃН25ЃЌдђдк450ЁцЪБЃЌ2SO3(g)![]() 2SO2(g)ЃЋO2(g)ЕФЛЏбЇЦНКтГЃЪ§ЮЊ___ЁЃ
2SO2(g)ЃЋO2(g)ЕФЛЏбЇЦНКтГЃЪ§ЮЊ___ЁЃ
ЃЈ2ЃЉAжаЕФЪдМСЪЧ___ЁЃ
ЃЈ3ЃЉдкЪЕбщЙ§ГЬжаВЛБиГжајМгШШЃЌЫЕУїИУЦНКтЕФЁїH___0ЃЈЬюЁА>ЁБЛђЁАЃНЁБЛђЁА<ЁБЃЉ,CзАжУгУРДЪеМЏШ§бѕЛЏСђЃЌЦфжаБљбЮЫЎЕФзїгУЪЧ___ЃЛШєгУ32gЭИњзуСПХЈСђЫсЗДгІжЦШЁЖўбѕЛЏСђЃЌЪЕбщНсЪјЪБЕУЕН20gШ§бѕЛЏСђЃЌИУЪЕбщжаЖўбѕЛЏСђЕФзЊЛЏТЪВЛаЁгк___ЁЃ
ЃЈ4ЃЉЧыжИГіБОЬзЪЕбщзАжУЕФУїЯдШБЯнЪЧЃК___ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПШчЯТЭМЫљЪОЃЌЭМЂёЪЧКубЙУмБеШнЦїЃЌЭМЂђЪЧКуШнУмБеШнЦїЁЃЕБЦфЫќЬѕМўЯрЭЌЪБЃЌдкЂёЁЂЂђжаЗжБ№МгШы2mol![]() КЭ2mol
КЭ2mol![]() ЃЌПЊЪМЪБШнЦїЕФЬхЛ§ОљЮЊVLЃЌЗЂЩњШчЯТЗДгІВЂДяЕНЦНКтзДЬЌ
ЃЌПЊЪМЪБШнЦїЕФЬхЛ§ОљЮЊVLЃЌЗЂЩњШчЯТЗДгІВЂДяЕНЦНКтзДЬЌ![]() ЬсЪОЃКЮяжЪXЃЌYЕФзДЬЌОљЮДжЊЃЌЮяжЪZЕФзДЬЌЮЊЦјЬЌ)ЃЌ2X(?)+Y(?)
ЬсЪОЃКЮяжЪXЃЌYЕФзДЬЌОљЮДжЊЃЌЮяжЪZЕФзДЬЌЮЊЦјЬЌ)ЃЌ2X(?)+Y(?)![]() aZ(g)ДЫЪБЂёжаXЃЌYЃЌZЕФЮяжЪЕФСПжЎБШЮЊ1:3:2ЁЃЯТСаХаЖЯе§ШЗЕФЪЧ
aZ(g)ДЫЪБЂёжаXЃЌYЃЌZЕФЮяжЪЕФСПжЎБШЮЊ1:3:2ЁЃЯТСаХаЖЯе§ШЗЕФЪЧ![]()
![]()
Ђё Ђђ
Ђђ Ђѓ
Ђѓ
A.ЮяжЪZЕФЛЏбЇМЦСПЪ§ a= 2
B.ШєXЁЂYОљЮЊЦјЬЌЃЌдђдкЦНКтЪБXЕФзЊЛЏТЪЃКЂё<Ђђ
C.ШєЂђжаЦјЬхЕФУмЖШШчЭМЂѓЫљЪОЃЌдђXЁЂYжажЛгавЛжжЮЊЦјЬЌ
D.ШєXЮЊЙЬЬЌЁЂYЮЊЦјЬЌЃЌдђЂёЁЂЂђжаДгПЊЪМЕНЦНКтЫљашЕФЪБМфЃКЂё>Ђђ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПОнБЈЕРЃЌдк300ЁцЁЂ70MPaЯТгЩЖўбѕЛЏЬМКЭЧтЦјКЯГЩввДМвбГЩЮЊЯжЪЕЃК2CO2ЃЈgЃЉ+6H2ЃЈgЃЉ![]() CH3CH2OHЃЈgЃЉ+3H2OЃЈgЃЉЃЌЯТСаа№ЪіДэЮѓЕФЪЧ
CH3CH2OHЃЈgЃЉ+3H2OЃЈgЃЉЃЌЯТСаа№ЪіДэЮѓЕФЪЧ
A.ЪЙгУCu-Zn-FeДпЛЏМСПЩДѓДѓЬсИпЩњВњаЇТЪ
B.ЗДгІашдк300ЁцНјааПЩЭЦВтИУЗДгІЪЧЮќШШЗДгІ
C.ГфШыДѓСПCO2ЦјЬхПЩЬсИпH2ЕФзЊЛЏТЪ
D.ДгЦНКтЛьКЯЦјЬхжаЗжРыГіCH3CH2OHКЭH2OПЩЬсИпCO2КЭH2ЕФРћгУТЪ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЮЊСЫЪЕЯжзЪдДРћгУзюДѓЛЏЃЌФГЛЏЙЄГЇНЋКЯГЩАБЁЂжЦДПМюКЭЩњВњФђЫи![]() ЙЄвеСЊКЯЃЌМђвзСїГЬШчЯТЃК
ЙЄвеСЊКЯЃЌМђвзСїГЬШчЯТЃК
![]() ЪБ101kPaЪБЃЌВтЕУЩњГЩ17g
ЪБ101kPaЪБЃЌВтЕУЩњГЩ17g![]() ЃЌЗХГі
ЃЌЗХГі![]() ШШСПЃЌаДГіКЯГЩ
ШШСПЃЌаДГіКЯГЩ![]() ЕФШШЛЏбЇЗНГЬЪН ______ ЃЎ
ЕФШШЛЏбЇЗНГЬЪН ______ ЃЎ
![]() КЯГЩАБдСЯЦјжаЕФдгжЪСђЛЏЧтгУЯЁАБЫЎЮќЪеЃЌИБВњЦЗЪЧЫсЪНбЮЃЎИУИБВњЦЗЕФЛЏбЇЪНЮЊ ______ ЃЎ
КЯГЩАБдСЯЦјжаЕФдгжЪСђЛЏЧтгУЯЁАБЫЎЮќЪеЃЌИБВњЦЗЪЧЫсЪНбЮЃЎИУИБВњЦЗЕФЛЏбЇЪНЮЊ ______ ЃЎ
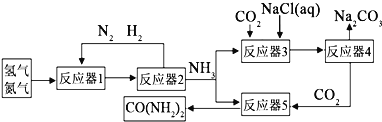
![]() ЗДгІЦї2ЗжРыГіРДЕФЕЊЦјКЭЧтЦјдйЭЈШыЗДгІЦї1ЃЌЦфФПЕФЪЧ ______
ЗДгІЦї2ЗжРыГіРДЕФЕЊЦјКЭЧтЦјдйЭЈШыЗДгІЦї1ЃЌЦфФПЕФЪЧ ______ ![]() ЯђЗДгІЦї3ГфШыдСЯЕФЫГађЪЧЃКЯШМгТШЛЏФЦШмвКЃЌЭЈШыАБЦјжСБЅКЭЃЌдйЭЈШызуСПЕФЖўбѕЛЏЬМПЩжЦЕУ
ЯђЗДгІЦї3ГфШыдСЯЕФЫГађЪЧЃКЯШМгТШЛЏФЦШмвКЃЌЭЈШыАБЦјжСБЅКЭЃЌдйЭЈШызуСПЕФЖўбѕЛЏЬМПЩжЦЕУ![]() ЗДгІЦї3жаЕФЛЏбЇЗНГЬЪНЮЊ ______ ЃЎ
ЗДгІЦї3жаЕФЛЏбЇЗНГЬЪНЮЊ ______ ЃЎ
![]() ЙЄвЕЩЯПЩгУЬМЁЂМзЭщгыЫЎеєЦћЗДгІжЦЧтЦј
ЙЄвЕЩЯПЩгУЬМЁЂМзЭщгыЫЎеєЦћЗДгІжЦЧтЦј
![]() ЃЌ
ЃЌ![]() ЃЌДЫЗДгІЕФЛЏбЇЦНКтГЃЪ§БэДяЪНЮЊ
ЃЌДЫЗДгІЕФЛЏбЇЦНКтГЃЪ§БэДяЪНЮЊ![]() ______ ЃЌЮЊСЫЬсИпЬМЕФзЊЛЏТЪЃЌвЫВЩгУЯТСаДыЪЉжаЕФ
______ ЃЌЮЊСЫЬсИпЬМЕФзЊЛЏТЪЃЌвЫВЩгУЯТСаДыЪЉжаЕФ![]() ЬюзжФИБрКХ
ЬюзжФИБрКХ![]() ______ ЃЎ
______ ЃЎ
A.діДѓбЙЧП![]() діМгЬМЕФСП
діМгЬМЕФСП![]() Щ§ИпЮТЖШ
Щ§ИпЮТЖШ![]() діМгЫЎЕФСП
діМгЫЎЕФСП![]() ЪЙгУДпЛЏМС
ЪЙгУДпЛЏМС![]() МАЪБвЦГіCOЁЂ
МАЪБвЦГіCOЁЂ![]()
![]() гааЉЙњМвЫЎЕчЗсИЛЃЌВЩгУЖшадЕчМЋЕчНтСђЫсФЦШмвКжЦЧтЦјЃЌЕчНтЪБбєМЋЩЯЕФЕчМЋЗДгІЪНЮЊ ______ ЃЎ
гааЉЙњМвЫЎЕчЗсИЛЃЌВЩгУЖшадЕчМЋЕчНтСђЫсФЦШмвКжЦЧтЦјЃЌЕчНтЪБбєМЋЩЯЕФЕчМЋЗДгІЪНЮЊ ______ ЃЎ
![]() ШєНівд
ШєНівд![]() ЁЂПеЦјЁЂ
ЁЂПеЦјЁЂ![]() ЮЊдСЯжЦФђЫи
ЮЊдСЯжЦФђЫи ЃЌБъзМзДПіЯТ
ЃЌБъзМзДПіЯТ![]()
![]() ЃЌРэТлЩЯзюЖрФмжЦ ______
ЃЌРэТлЩЯзюЖрФмжЦ ______ ![]() ФђЫиЃЎ
ФђЫиЃЎ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЫЎУКЦјЃЈCOКЭH2ЃЉЪЧКЯГЩМзДМЕФживЊдСЯЃЌЫќПЩгУЫЎеєЦјЭЈЙ§ГуШШЕФЬПВужЦЕУЃКCЃЈsЃЉ+H2OЃЈgЃЉ![]() COЃЈgЃЉ+H2ЃЈgЃЉ ІЄH=+131.3 kJЁЄmol-1
COЃЈgЃЉ+H2ЃЈgЃЉ ІЄH=+131.3 kJЁЄmol-1
ЃЈ1ЃЉИУЗДгІЕФЦНКтГЃЪ§ЕФБэДяЪНЮЊ_________________ЃЛЩ§ИпЮТЖШЃЌKжЕНЋ________ЃЛШнЦїжаЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПНЋ________ЁЃЃЈЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБЃЉЁЃ
ЃЈ2ЃЉЩЯЪіЗДгІДяЕНЦНКтКѓЃЌНЋЬхЯЕжаЕФCЃЈsЃЉВПЗжвЦзпЃЌЦНКтНЋ________ЃЈЬюзжФИЃЉЁЃ
A.ЯђзѓвЦ B.ЯђгввЦ C.ВЛвЦЖЏ
ЃЈ3ЃЉЯТСаЪТЪЕФмЫЕУїИУЗДгІдквЛЖЈЬѕМўЯТвбДяЕНЦНКтзДЬЌЕФга________ЃЈЬюзжФИЃЉЁЃ
A.ЕЅЮЛЬхЛ§ФкУПЯћКФ1 mol COЕФЭЌЪБЩњГЩ1 mol H2
B.ЛьКЯЦјЬхзмЮяжЪЕФСПБЃГжВЛБф
C.ЩњГЩH2OЃЈgЃЉЕФЫйТЪгыЯћКФCOЕФЫйТЪЯрЕШ
D.H2OЃЈgЃЉЁЂCOЁЂH2ЕФХЈЖШЯрЕШ
ЃЈ4ЃЉФГЮТЖШЯТЃЌНЋ4.0 mol H2OЃЈgЃЉКЭзуСПЕФЬПГфШы2 LЕФУмБеШнЦїжаЃЌЗЂЩњШчЯТЗДгІЃЌCЃЈsЃЉ+H2OЃЈgЃЉ![]() COЃЈgЃЉ+H2ЃЈgЃЉЃЌДяЕНЦНКтЪБВтЕУK=1ЃЌдђДЫЮТЖШЯТH2OЃЈgЃЉЕФзЊЛЏТЪЮЊ________ЁЃ
COЃЈgЃЉ+H2ЃЈgЃЉЃЌДяЕНЦНКтЪБВтЕУK=1ЃЌдђДЫЮТЖШЯТH2OЃЈgЃЉЕФзЊЛЏТЪЮЊ________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЫЕЗЈгыбЮРрЕФЫЎНтгаЙиЕФЪЧ![]()
ЂйУїЗЏКЭ![]() ПЩзїОЛЫЎМСЃЛ
ПЩзїОЛЫЎМСЃЛ
ЂкЪЕбщЪвЪЂЗХ![]() ЁЂ
ЁЂ![]() ЕШШмвКЕФЪдМСЦПгІгУЯ№ЦЄШћЃЌЖјВЛФмгУВЃСЇШћЃЛ
ЕШШмвКЕФЪдМСЦПгІгУЯ№ЦЄШћЃЌЖјВЛФмгУВЃСЇШћЃЛ
ЂлГЄЦкЪЉгУСђЫсяЇЃЌЭСШРЫсаддіЧПЃЛ
Ђм![]() гы
гы![]() ШмвКПЩзїКИНгжаЕФГ§атМСЃЛ
ШмвКПЩзїКИНгжаЕФГ§атМСЃЛ
ЂнВнФОЛвгыяЇЬЌЕЊЗЪВЛФмЛьКЯЪЉгУЃЛ
ЂогУ![]() гы
гы![]() СНжжШмвКПЩзїХнФУ№Л№МСЁЃ
СНжжШмвКПЩзїХнФУ№Л№МСЁЃ
A.ЂйЂмB.ЂкЂоC.ЂлЂнD.ШЋВП
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com