
����Ŀ��ij�¶�����2L�ܱ������м���һ����A���������»�ѧ��Ӧ��
2A(g)![]() B(g)+C(g)����H =��48.25 kJ��mol��1����Ӧ������B��A��Ũ�ȱ���ʱ��t����ͼ��ʾ��ϵ������õ�15minʱc(B)=1.6 mol��L��1�����н�����ȷ����
B(g)+C(g)����H =��48.25 kJ��mol��1����Ӧ������B��A��Ũ�ȱ���ʱ��t����ͼ��ʾ��ϵ������õ�15minʱc(B)=1.6 mol��L��1�����н�����ȷ����
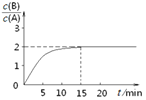
A.���¶��´˷�Ӧ��ƽ�ⳣ��Ϊ3.2
B.A�ij�ʼ���ʵ���Ϊ4 mol
C.��Ӧ����ƽ��ʱ���ų���������193kJ
D.��Ӧ��ƽ��ʱ��A��ת����Ϊ80%
���𰸡�D
��������
����c��B��=1.6 mol/L��n��B��=3.2mol����ͼ����֪n��A��=1.6mol�����������������֪��
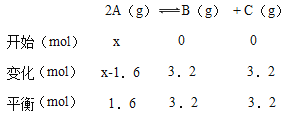
���Լ����x=8mol������ƽ��ʱA��B��C��Ũ�ȷֱ�Ϊ0.8mol/L��1.6mol/L��1.6mol/L��
A.ƽ�ⳣ��K=![]() =4������
=4������
B.A��ʼΪ8mol������
C.����ƽ������3.2mol B���ų���������3.2��48.25=154.4kJ��C����
D.��Ӧ��ƽ��ʱ��A��ת����Ϊ![]() ��100%=80����D��ȷ��
��100%=80����D��ȷ��
��ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£�ˮ�����ӻ�ԼΪ1��10��12����VaL pH��2��������Һ��VbL pH��11��NaOH��Һ��ϣ��������Һ��pH��10�������(Va��Vb) L����Va��VbΪ ( )
A. 2��11B. 2��9C. 11��2D. 9��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������������ʴ��ÿ����ʴ����ʧ�ĸ���ռ���������������ķ�֮һ����ش�����ڸ�ʴ�����������е��й����⡣
��1�������ĸ�װ�ÿɷ�ֹ��������ʴ________________��
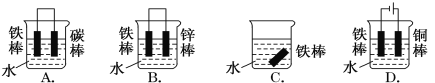
��2����ʵ�������У����������ı����ͭ��ֹ������ʴ��װ��ʾ��ͼ��ͼ����ش�
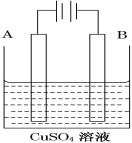
������Ӧ���Դ��________��������д������B�缫�ĵ缫��Ӧʽ��______��
�������ǰA��B������Ƭ������ͬ�������ɺ�����ȡ��ϴ������ɡ�����������������Ϊ10.24 g������ʱ��·��ͨ���ĵ���Ϊ________mol��
�۵�ƽ�����CuSO4��Һ��Ũ��______������С�����䣩
�ܶƲ�����������ױ���ʴ����___________������ţ���
A ��ͭ�� B ��п�� C ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ļ�ԭ��CO���ɽ�̿��CO2��Ӧ���á��ֽ���̿��CO2�������Ϊ2L���ܱ������У������½������з�Ӧ��C(s)��CO2(g)![]() 2CO(g) ��H��Q kJ/mol��ͼΪCO2��CO�����ʵ���n��ʱ��t�ı仯��ϵͼ������˵����ȷ����
2CO(g) ��H��Q kJ/mol��ͼΪCO2��CO�����ʵ���n��ʱ��t�ı仯��ϵͼ������˵����ȷ����
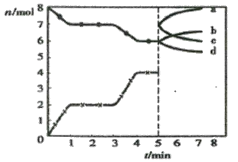
A.0��1min��v(CO)��1 mol/(L��min)��1��3minʱ��v(CO)��v(CO2)
B.�������ڵ�ѹǿ����ʱ����Ӧһ���ﵽƽ��״̬����![]()
C.3minʱ�¶���T1���ߵ�T2����Q��0���ٴ�ƽ��ʱ![]()
D.5minʱ�ٳ���һ������CO��a��d���߷ֱ��ʾn(CO)��n(CO2)�ı仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��˵��������������ʣ�ijͬѧ���������ʵ�鷽��֤�������д�����ǣ�������
A.����0.10 mol/L CH3 COOH��Һ������Һ��pH����pH����1�����֤������Ϊ�������
B.��pH�Ʒֱ��0.01 mol/L��0.10 mol/L�Ĵ�����Һ��pH�������ߵ�pH���С��1�����֤���������������
C.ȡ�������Ũ�ȵ�CH3 COOH��������Һ���ֱ����Na2CO3���壬��������Һ��������֤࣬������Ϊ�������
D.����ͬŨ������ʹ���ĵ����ԣ�������Һ�ĵ�����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦA(g)+B(g)![]() C(g) +D(g)���������е������仯��ͼ����H ��ʾ��Ӧ���ʱ䡣����˵����ȷ����
C(g) +D(g)���������е������仯��ͼ����H ��ʾ��Ӧ���ʱ䡣����˵����ȷ����
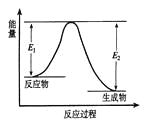
A. ��Ӧ��ϵ�м����������Ӧ��������E1��С��E2����
B. ��Ӧ��ϵ�м����������Ӧ����������H����
C. ��H < 0����Ӧ�ﵽƽ��ʱ�������¶ȣ�A��ת��������
D. ��H > 0����Ӧ�ﵽƽ��ʱ�������¶ȣ�A��ת���ʼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��T��ʱ����1 L���ܱ������г���2 mol CO2��6mol H2��һ�������·�����Ӧ��CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ��H=��49.0kJ/mol�����H2��CH3OH(g)��Ũ����ʱ��仯����ͼ��ʾ������˵������ȷ���� �� ��
CH3OH(g)+H2O(g) ��H=��49.0kJ/mol�����H2��CH3OH(g)��Ũ����ʱ��仯����ͼ��ʾ������˵������ȷ���� �� ��
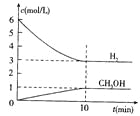
A.0~10min��v(H2)=0.3mol/(L��min)
B.T��ʱ��ƽ�ⳣ��K=![]() ��CO2��H2��ת�������
��CO2��H2��ת�������
C.T��ʱ��������Ӧ����64g CH3OH���ɣ�ͬʱ�ų�98.0kJ������
D.�ﵽƽ��������¶Ȼ��ٳ���CO2���壬���������H2��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NaClO2 ��һ����Ҫ��ɱ����������Ҳ������Ư��֯��ȣ�һ������NaClO2 �Ĺ������£�
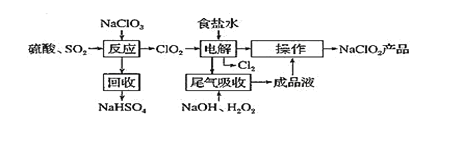
��֪����ClO2��һ��ǿ���������壬Ũ�ȴ�ʱ�ֽⱬը��������ʹ��ʱҪ��ϡ�����������Ƚ���ϡ�ͣ�ͬʱ������ա��ȡ���NaClO2������Һ���¶ȵ���38��ʱ�����ľ�����NaClO2��33H2O������38��ʱ�����ľ�����NaClO2������60��ʱNaClO2�ֽ��NaClO3��NaCl���ش��������⣺
(1)�����ѧ����������Ӧ������Ļ������о�����H2C2O4����SO2�Ʊ�ClO2���·������÷����Ļ�ѧ����ʽΪ______________________��
(2)��ò�ƷNaClO2�����������������²��裺
����ѹ��55�������ᾧ�������ȹ��ˣ���___________________________������60������õ���Ʒ��
(3)Ϊ�˲ⶨ��ƷNaClO2�Ĵ��ȣ�ȡ�������ò�Ʒ12.5g����ˮ���1L��Һ��ȡ��10.00mL��Һ����ƿ�У��ټ��������ữ��KI��Һ����ַ�Ӧ��(ClO2������ԭΪCl�����ʲ��μӷ�Ӧ)������2~3�ε�����Һ����0.25molL��1Na2S2O3��Һ�ζ����ﵽ�ζ��յ�ʱ��ȥ��Һ20.00mL���Լ����ƷNaClO2�Ĵ���_________________________(��ʾ��2Na2S2O3+I2=Na2S4O6+2NaI)

(4)NaClO2��Һ�д���ClO2��HClO2��ClO2����Cl�����ֺ����������ⶨ 25����������Ũ���� pH �ı仯�����ͼ��ʾ(Cl��û�л���)
������������NaClO2��Һ�д���Cl����ԭ����_______________________(�����ӷ���ʽ����)��
��pH=5ʱ��NaClO2��Һ��ClO2��HClO2��ClO2����Cl�����ֺ�������Ũ���ɴ�С��˳����___________________________________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com