
【题目】一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如右图所示,下列判断正确的是

A. 50min时,pH=2和pH=7时R的降解百分率相等
B. 溶液酸性越强,R的降解速率越小
C. R的起始浓度越小,降解速率越大
D. 在20~25 min之间,pH=10时R的平均降解速率为0.04mol·L-1·min-1
科目:高中化学 来源: 题型:
【题目】下列实验的反应原理用离子方程式表示正确的是( )
A. 室温下,测的氯化铵溶液pH<7,证明一水合氨的是弱碱:NH4++2H2O=NH3·H2O+H3O+
B. 用氢氧化钠溶液除去镁粉中的杂质铝:2Al+2OH-+2H2O=2AlO2-+3H2↑
C. 用碳酸氢钠溶液检验水杨酸中的羧基:
 +2HCO3-→
+2HCO3-→ +2H2O+2CO2↑
+2H2O+2CO2↑
D. 用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通过反应“SiO2+2C![]() Si+2CO↑”制取单质硅,下列说法正确的是
Si+2CO↑”制取单质硅,下列说法正确的是
A. 自然界中硅元素均以SiO2形式存在
B. 高纯度晶体Si可用于制造光导纤维
C. 该反应条件下C的还原性比Si强
D. 标准状况下生成4.48 L CO时转移电子数为0.4×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定放置已久的小苏打样品中纯碱的质量分数.
(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算.实验中加热至恒重的目的是 .
(2)方案二:按如图装置进行实验.并回答以下问题: 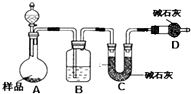
①分液漏斗中应该装(填“盐酸”或“稀硫酸盐”),D装置的作用是 .
②实验中除称量样品质量外,还需称装置反应前后质量的变化(用装置的字母代号);
③根据此实验得到的数据,测定结果有较大误差,因为实验装置还存在一个明显缺陷,该缺陷是 .
(3)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液,过滤洗涤,干燥沉淀,称量固体质量,计算:
①实验中判断沉淀已完全的方法是 .
②若加入试剂改为氢氧化钡,已知称得样品9.5g,干燥的沉淀质量为19.7g,则样品中碳酸钠的质量分数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组将纯净的SO2气体通入0.1molL﹣1的Ba(NO3)2溶液中,得到了BaSO4沉淀.为探究上述溶液中何种微粒能氧化通入的SO2 , 该小组提出了如下假设:
假设一:溶液中的NO3﹣
假设二:溶液中溶解的O2;
(1)验证假设一
该小组设计实验验证了假设一,请在下表空白处填写相关实验现象.
实验步骤 | 实验现象 | 结论 |
实验1:在盛有不含O2的25mL0.1molL﹣1BaCl2溶液的烧杯中,缓慢通入纯净的SO2气体 | 假设一成立 | |
实验2:在盛有不含O2的25mL0.1molL﹣1Ba(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体 |
(2)为深入研究该反应,该小组还测得上述两个实验中溶液pH随通入SO2体积的变化曲线如图: 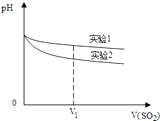
实验1中溶液pH变小的原因是;V1时,实验2中溶液pH小于实验1的原因是(用离子方程式表示).
(3)该小组还设计了实验验证假设二,请在实验4横线处写出实验步骤.
实验步骤 | 实验现象 | 结论 |
实验3:在盛有不含O2的25m10.1mol/LBaCl2溶液的烧杯中,缓慢通入纯净的SO2气体 | ||
实验4: |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个2L的密闭容器中,加入4mo1A和2molB进行如下反应:
3A(g)+2B(g)![]() 4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6molC,且反应的前后的压强之比为5:4 (相同的温度下测量), 则下列说法正确的是
4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6molC,且反应的前后的压强之比为5:4 (相同的温度下测量), 则下列说法正确的是
A. 该反应的化学平衡常数表达式是![]()
B. 此时,B 的平衡转化率是35%
C. 增大该体系的压强,平衡向右移动化学平衡常数增大
D. 增加C的量,B的平衡转化率不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA.下列说法正确的是( )
A. 1L0.1molL﹣1NH4Cl溶液中,NH4+的数量为0.1NA
B. 2.4gMg与H2SO4完全反应,转移的电子数为0.1NA
C. 标准状况下,2.24LN2和O2的混合气体中分子数为0.2NA
D. 0.1mol H2和0.1mol I2于密闭容器中充分反应后,其分子总数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com