
【题目】下列有关反应的离子方程式书写正确的是
A.氯气溶于水:Cl2+H2O=2H++Cl-+ClO-
B.钠与CuSO4溶液反应:2Na+Cu2+=Cu+2Na+
C.碳酸钙中滴加盐酸:CaCO3+2H+=Ca2++CO2↑+H2O
D.稀硫酸和氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓
【答案】C
【解析】
A. 氯气溶于水,反应生成盐酸和次氯酸,次氯酸为弱酸必须写化学式,反应的离子方程式为:Cl2+H2O![]() H++Cl-+HClO,选项A错误;
H++Cl-+HClO,选项A错误;
B. 钠为很活泼的金属,与CuSO4溶液反应不能置换出铜,而是先直接与水反应,反应的离子方程式为:2Na+Cu2++2H2O=Cu(OH)2↓+2Na++H2↑,选项B错误;
C. 碳酸钙中滴加盐酸,反应生成氯化钙、二氧化碳和水,反应的离子方程式为:CaCO3+2H+=Ca2++CO2↑+H2O,选项C正确;
D. 稀硫酸和氢氧化钡溶液反应生成硫酸钡沉淀和水,反应的离子方程式为:SO42-+2H++Ba2++2OH-=BaSO4↓+2H2O,选项D错误;
答案选C。


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,C(s)+CO2(g)![]() 2CO (g) ΔH>0。下列有关叙述正确的是
2CO (g) ΔH>0。下列有关叙述正确的是
A. 升高温度,v(正)增大,v(逆)减小
B. 增大压强,v(正)增大,v(逆)增大
C. 恒温恒压,再充入N2,反应速率不变
D. 增加炭的用量,v(正)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应速率是描述化学反应进行快慢程度的物理量。下面是某同学测定化学反应速率并探究其影响因素的实验。

Ⅰ.测定化学反应速率
该同学利用如图装置测定化学反应速率。
(1)写出该反应的离子方程式 ___________________________________________________;为保证实验准确性、可靠性,利用该装置进行实验前应先进行的步骤是______________;除如图所示的实验用品、仪器外,还需要的一件实验仪器是__________________。
(2)若在2 min时收集到224 mL(已折算成标准状况)气体,可计算出该2 min内H+的反应速率,而该测定值比实际值偏小,其原因是____________________________________________。
(3)试简述测定该反应的化学反应速率的其他方法:_______________________________________________(写一种)。
Ⅱ.为探讨化学反应速率的影响因素,某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mol·L-1、2.00 mol·L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K,每次实验HNO3的用量为25.0 mL、大理石用量为10.00 g。
(4)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
实验编号 | T/K | 大理石规格 | HNO3浓度/mol·L-1 | 实验目的 |
① | 298 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和______探究温度对该反应速率的影响; (Ⅲ)实验①和______探究大理石规格(粗、细)对该反应速率的影响。 |
② | _______ | 粗颗粒 | ______ | |
③ | ____ | ___ | 2.00 | |
④ | 298 | ________ | _____ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的短周期主族元素。Y的单质经常作为保护气;由Z、W形成的一种化合物可与X、W形成的化合物反应,生成淡黄色固体。下列推断正确的是
A. Y的最简单氢化物的热稳定性比Z的强
B. 在同周期元素中,W的最高价氧化物对应的水化物的酸性最强
C. 离子半径:X<Y<Z<W
D. 含W的盐溶液可能呈碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂—铜空气燃料电池(如图)容量高、成本低,该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为:2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法错误的是

A. 整个反应过程中,氧化剂为O2
B. 放电时,正极的电极反应式为:Cu2O+H2O+2e-=2Cu+2OH-
C. 放电时,当电路中通过0.1 mol电子的电量时,有0.1 mol Li+透过固体电解质向Cu极移动,有标准状况下1.12 L氧气参与反应
D. 通空气时,铜被腐蚀,表面产生Cu2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,所含分子数相同的是
A.l0g H2和l0g O2B.9g H2O和0.5mol Br2
C.224mL H2(标准状况)和0.1mol N2D.5.6L N2(标准状况)和22g CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池能有效提高能源利用率,具有广泛的应用前景。下列物质均可用作燃料电池的燃料,其中最环保的是( )
A. 甲醇 B. 天然气 C. 液化石油气 D. 氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉煤气是炼铁厂排放的尾气,含有H2、N2、CO、CO2及O2,其中N2约为55%、CO约为25%、CO2约为15%、O2约为1.64%(均为体积分数)。某科研小组对尾气的应用展开研究:
(1)直接作燃料
已知:C(s)+O2(g)![]() CO2 (g) ΔH=-393.5kJ/mol
CO2 (g) ΔH=-393.5kJ/mol
2C(s)+O2(g)![]() 2CO (g) ΔH=-221kJ/mol
2CO (g) ΔH=-221kJ/mol
CO燃烧热的热化学方程式为__________。
(2)生产合成氨的原料
高炉煤气经过下列步骤可转化为合成氨的原料气:
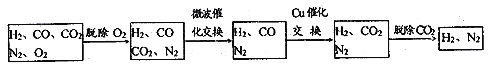
在脱氧过程中仅吸收了O2,交换过程中发生的反应如下,这两个反应均为吸热反应:
CO2+CH4![]() CO+H2(未配平) CO+H2O
CO+H2(未配平) CO+H2O![]() CO2+ H2
CO2+ H2
①气体通过微波催化交换炉需要较高温度,试根据该反应特征,解释采用较高温度的原因____________________________________________。
②通过铜催化交换炉后,所得气体中V(H2):V(N2)=__________。
(3)合成氨后的气体应用研究
①氨气可用于生产硝酸,该过程中会产生大气污染物NOx。为了研究对NOx的治理,该科研小组在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,发生如下反应:2NO(g)+Cl2(g)![]() 2ClNO(g) ΔH<0。10min时反应达平衡,测得10min内v(ClNO)=7.5×10-3mol/(L·min),则平衡后n(Cl2)=__________mol。设此时NO的转化率为α1,若其它条件不变,上述反应在恒压条件下进行,平衡时NO的转化率为α2,则α1__________α2 (填“>”、“<”或“=”);平衡常数K__________(填增大”“减小 ”或“不变”)
2ClNO(g) ΔH<0。10min时反应达平衡,测得10min内v(ClNO)=7.5×10-3mol/(L·min),则平衡后n(Cl2)=__________mol。设此时NO的转化率为α1,若其它条件不变,上述反应在恒压条件下进行,平衡时NO的转化率为α2,则α1__________α2 (填“>”、“<”或“=”);平衡常数K__________(填增大”“减小 ”或“不变”)
②氨气还可用于制备NCl3,NCl3发生水解产物之一具有强氧化性,该水解产物能将稀盐酸中的NaClO2氧化成ClO2,该反应的离子方程式为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com