
【题目】下列实验过程不能达到实验目的的是( )
实验目的 | 实验过程 | |
A | 探究维生素C的还原性 | 向盛有2mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化 |
B | 配制100mL1.0mol/L CuSO4溶液 | 将25.0gCuSO4·5H2O配成100mL溶液 |
C | 验证X溶液中是否含有Fe2+ | 向X溶液中滴加几滴新制氯水,振荡,再加入少量KSCN溶液,观察溶液颜色变化 |
D | 除去固体KNO3中少量的NaCl | 将混合物制成热的饱和溶液,冷却结晶,过滤、洗涤、干燥 |
A.AB.BC.CD.D
【答案】C
【解析】
A、Fe3+显黄色,维生素C滴加到FeCl3溶液中,如果黄色变为浅绿色,说明Fe3+被还原成Fe2+,即维生素C表现还原性,故A能达到实验目的;
B、用25.0gCuSO4·5H2O配成100mL溶液,此时c(CuSO4)=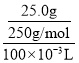 =1mol·L-1,故B能达到实验目的;
=1mol·L-1,故B能达到实验目的;
C、先滴加新制氯水,再滴加少量的KSCN溶液,如果原溶液中含有Fe3+,对Fe2+的检验产生干扰,因此检验Fe2+:先加入KSCN溶液,观察现象,如果无现象,再滴加新制氯水或双氧水,溶液显红色,说明原溶液中含有Fe2+,故C不能完成实验目的;
D、KNO3溶解度受温度的影响较大,NaCl溶解度受温度影响较小,因此除去固体KNO3中少量的NaCl,采用溶解,加热浓缩,冷却结晶,过滤、洗涤、干燥,故D能完成实验目的;
答案为C。


科目:高中化学 来源: 题型:
【题目】常温下,向20mL0.1mol L-1HB溶液中逐滴滴入 0.1mol L-1NaOH溶液,所得 PH变化曲线如图所示。下列说法错误的是

A.OA各点溶液均存在:c(B-) >c(Na+)
B.C至 D各点溶液导电能力依次增强
C.点 O时,pH>1
D.点 C时,X约为 10.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚维酮碘的水溶液是一种常用的碘伏类缓释消毒剂,聚维酮通过氢键与HI3形成聚维酮碘,其结构表示如图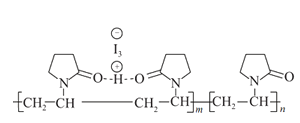 ,下列说法不正确的是( )
,下列说法不正确的是( )
A.聚维酮的单体是![]() B.聚维酮分子由(m+n)个单体聚合而成
B.聚维酮分子由(m+n)个单体聚合而成
C.聚维酮碘是一种水溶性物质D.聚维酮在一定条件下能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:
(1) NaClO2的化学名称为_______。
(2)在鼓泡反应器中通入含有含有SO2和NOx的烟气,反应温度为323 K,NaClO2溶液浓度为5×103mol·L1。反应一段时间后溶液中离子浓度的分析结果如下表》
离子 | SO42 | SO32 | NO3 | NO2 | Cl |
c/(mol·L1) | 8.35×104 | 6.87×106 | 1.5×104 | 1.2×105 | 3.4×103 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式__________。增加压强,NO的转化率______(填“提高”“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐______ (填“提高”“不变”或“降低”)。
③由实验结果可知,脱硫反应速率______脱硝反应速率(填“大于”或“小于”)。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是___________。
(3)在不同温度下,NaClO2溶液脱硫、脱硝的反应中,SO2和NO的平衡分压px如图所示。
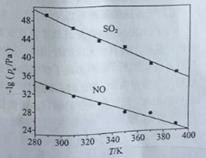
①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均______________(填“增大”“不变”或“减小”)。
②反应ClO2+2SO32===2SO42+Cl的平衡常数K表达式为___________。
(4)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。
①从化学平衡原理分析,Ca(ClO)2相比NaClO具有的有点是_______。
②已知下列反应:
SO2(g)+2OH(aq) ===SO32(aq)+H2O(l) ΔH1
ClO(aq)+SO32(aq) ===SO42(aq)+Cl(aq) ΔH2
CaSO4(s) ===Ca2+(aq)+SO42(aq) ΔH3
则反应SO2(g)+ Ca2+(aq)+ ClO(aq) +2OH(aq) ="==" CaSO4(s) +H2O(l) +Cl(aq)的ΔH=______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如图所示)。下列说法错误的是
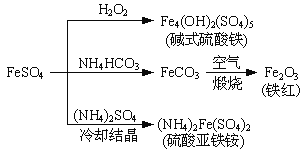
A. 碱式硫酸铁水解能产生Fe(OH)3胶体,可用作净水剂
B. 为防止NH4HCO3分解,生产FeCO3需在较低温度下进行
C. 可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化
D. 常温下,(NH4)2Fe(SO4)2在水中的溶解度比FeSO4的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨晶体结构中的某一种的某一部分。

(1)代表金刚石的是________(填字母编号,下同),其中每个碳原子与______个碳原子最近且距离相等;金刚石属于________晶体。
(2)代表石墨的是_______,每个正六边形占有的碳原子数平均为_______个;
(3)代表NaCl的是_______,每个Na+周围与它最近且距离相等的Na+有_______个;
(4)代表CsCl的是_______,它属于_______晶体,每个Cs+与个_______Cl-紧邻;
(5)代表干冰的是_______,它属于_______晶体,每个CO2分子与_______个CO2分子紧邻;
(6)则上述五种物质熔点由高到低的排列顺序为______________(用字母编号回答)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气态反应A(g)+3B(g)=2C(g)+2D(g),在四种不同条件下的反应速率如下,其中反应速率最快的是( )
A.vA=0.15mol/(L·min)B.vB=0.6mol/(L·min)
C.vC=0.4mol/(L·min)D.vD=0.6mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钕铁硼磁铁是目前为止具有最强磁力的永久磁铁。生产钕铁硼磁铁的主要原材料有稀土金属钕、纯铁、铝、硼以及其他稀土原料。
(1)写出三价铁离子的外围电子排布图:___,在短周期元素中,与Al的化学性质最相似的元素符号是:___。
(2)实验测得AlCl3的蒸气以二聚分子Al2Cl6的形式存在,已知Al2Cl6分子中Al与Cl交替排列,为非极性分子,Al与Cl均满足8电子稳定结构,则Al2Cl6分子中Al原子采取___杂化,Al2Cl6分子的结构式为:___。
(3)硼(B)元素及与其同周期相邻的两种元素第一电离能由小到大的顺序为:___(用元素符号表示)。
(4)已知AlCl3的熔点为194℃,易升华,AlF3的熔点为1040℃,其原因为:___。
(5)已知立方氮化硼(BN)其晶胞结构类似于金刚石(如图所示),则N的配位数是___,与N原子距离最近的B原子构成的立体构型是___。

若图中b号原子的坐标为(![]() ,
,![]() ,0)写出a原子的坐标___,设晶胞中B、N原子半径分别为pnm、qnm,晶胞边长为rnm,则以a原子为中心形成的最小立方体的空间利用率为___(写代数式即可,不必化简);设晶胞中最近的B、N原子之间的距离为a nm,晶体的密度为bg·cm-3,则阿伏加德罗常数为___mol-1(用含a、b的代数式表示)。
,0)写出a原子的坐标___,设晶胞中B、N原子半径分别为pnm、qnm,晶胞边长为rnm,则以a原子为中心形成的最小立方体的空间利用率为___(写代数式即可,不必化简);设晶胞中最近的B、N原子之间的距离为a nm,晶体的密度为bg·cm-3,则阿伏加德罗常数为___mol-1(用含a、b的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将0.1000mol·L-1盐酸滴入20.00 mL未知浓度的某一元碱MOH溶液中,溶液pH随加入盐酸体积变化曲线如图所示。下列有关说法不正确的是

A.该一元碱溶液浓度为0.1000mol·L-1
B.a点:c(M+)>c(Cl-)>c(OH-)>c(H+)
C.b点:c(M+)+c(MOH)=c(Cl-)
D.室温下,MOH的电离常数Kb=1×10-5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com