
| A. | $\frac{125a}{72V}$ mol•L-1 | B. | $\frac{125a}{36V}$ mol•L-1 | C. | $\frac{250a}{36V}$ mol•L-1 | D. | $\frac{250a}{48V}$ mol•L-1 |
分析 根据n=$\frac{m}{M}$计算出agSO42-的物质的量,再根据硫酸铁的化学式组成计算出铁离子的物质的量,再计算出$\frac{1}{2}$VmL溶液中铁离子的物质的量,最后根据c=$\frac{n}{V}$计算出稀释后溶液中铁离子的物质的量浓度.
解答 解:ag SO42-离子的物质的量为:n(SO42-)=$\frac{ag}{96g/mol}$=$\frac{a}{96}$mol,
V mL Fe2(SO4)3溶液中含有Fe3+离子的物质的量为:n(Fe3+)=$\frac{2}{3}$×n(SO42-)=$\frac{a}{96}$mol×$\frac{2}{3}$=$\frac{a}{144}$mol,
$\frac{1}{2}$V mL溶液中含有Fe3+的物质的量为:n(Fe3+)=$\frac{a}{144}$mol×$\frac{1}{2}$=$\frac{a}{288}$mol,
稀释后溶液体积为2VmL,则溶液中Fe3+的浓度为:c(Fe3+)=$\frac{\frac{a}{288}mol}{2V×1{0}^{-3}L}$=$\frac{125a}{72V}$mol/L,
故选A.
点评 本题考查了物质的量浓度的相关计算,题目难度中等,要求学生熟练掌握物质的量浓度的计算公式,试题侧重考查学生的分析能力及化学计算能力.


 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:选择题
| A. | ①⑤⑦ | B. | ②⑤ | C. | ⑤⑦ | D. | 除③④外 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
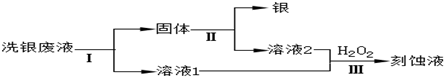
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{16(b+a)}{b-a}$ | B. | $\frac{16(b-a)}{b+a}$ | C. | $\frac{8(b+a)}{b-a}$ | D. | $\frac{8(b-a)}{b+a}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石英玻璃是以纯碱、石灰石和二氧化硅为原料制成的 | |
| B. | 氮的固定是指将空气中游离的氮转变为氮的化合物的方法 | |
| C. | 绿色食品是指不含任何化学物质的食品 | |
| D. | 纳米材料是指一种称为“纳米”的新物质制成的材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 24% | B. | 30% | C. | 40% | D. | 19% |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
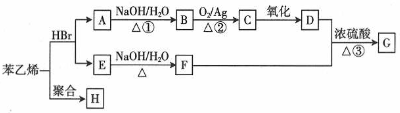
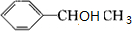 ;H的结构简式
;H的结构简式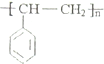 .
.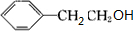 +O2$→_{△}^{Ag}$2
+O2$→_{△}^{Ag}$2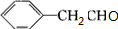 +2H2O ③
+2H2O ③ +
+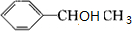 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$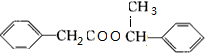 +H2O
+H2O .(任写一种)
.(任写一种)查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 实验Ⅰ:导管口气体可被点燃,产生淡蓝色火焰 | |
| B. | 实验Ⅱ:振荡后静置,溶液分层,且两层均接近无色 | |
| C. | 实验Ⅲ:试管中有气泡冒出,溶液颜色无明显变化 | |
| D. | 实验Ⅳ:试管内气体颜色逐渐变浅,试管壁出现油状液滴 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com